Тема: Вычисление объемных отношений газов по уравнениям химических реакций.
Учащиеся должны знать: объемы реагирующих и полученных газов относятся друг к другу, как количество вещества одного газа относится к количеству вещества другого газа (получено из закона Авогадро):
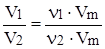
 .
.
Пример: Смесь CO и CO2 объемом 12 мл смешали с избытком кислорода и сожгли, после чего общий объем всей газовой смеси уменьшился на 4 мл. Найдите объемы CO и CO2 в исходной смеси.
Решение:
2CO + O2 = 2CO2.
2 моль 1 мл 2 моль
n(CO) = n(CO2), то есть V(CO) = V(CO2),
значит, объем мог измениться только за счет расхода O2 (CO2 не горит),
отсюда V(O2) = 4 мл.
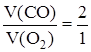 , V(CO) = 2V(O2) = 8 мл, V(CO2) = 12 мл – 8 мл = 4 мл.
, V(CO) = 2V(O2) = 8 мл, V(CO2) = 12 мл – 8 мл = 4 мл.
Кроме рассмотренных типов задач могут быть задачи комбинированного типа, например:
Плотность газа равна 1.25 г/л. Определите его молярную массу. Какой это
газ?
| Дано: | |
| r = 1.25 г/л | |
| M = ? |
Решение: Начинаем, как всегда, с вопроса.
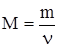 (1)
(1)
так как это газ, то 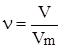 (2)
(2)
Подставим (2) в (1), получим:
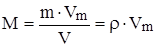 M = r · Vm.
M = r · Vm.
M = 1.25 г/л · 22.4 л/моль = 28 г/моль - это N2.
Дата добавления: 2015-08-21; просмотров: 1246;
