Рак шейки матки
Рак шейки матки — самое частое злокачественное заболевание женских половых органов: от 20 до 40 на 100 000 женского населения. Совершенствование профилактической работы в женских консультациях позволило уменьшить частоту этой патологии у женщин и повысить ее выявляемость в ранних стадиях. Особую значимость при этом имеет учение о фоновых и предраковых состояниях, позволяющее диагностировать рак шейки матки (РШМ) на стадиях преинвазии и микроинвазии. И все же, несмотря на эти достижения, сохраняется высокая частота выявляемости больных РШМ в запущенных стадиях (III—IV).
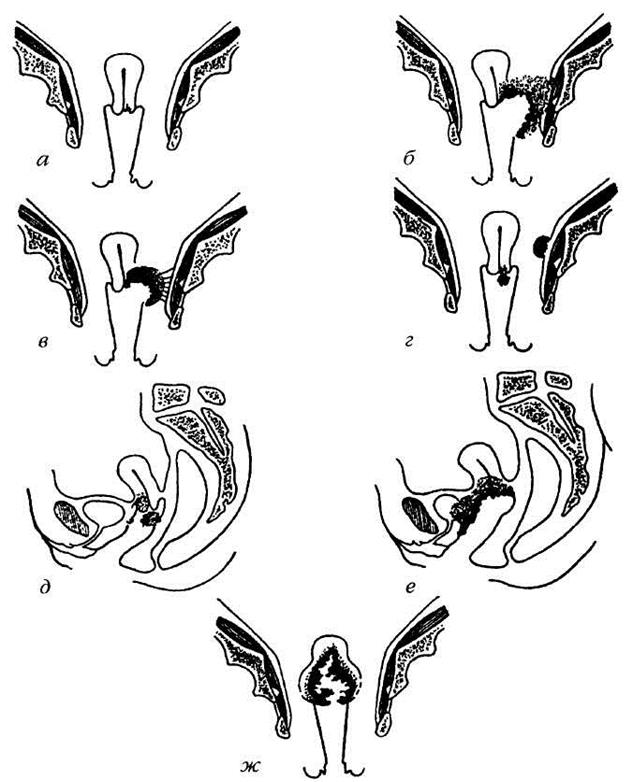
Рис. 38. Стадии рака шейки матки:
а — I стадия;
б — II стадия (параметральный вариант);
в — II стадия (влагалищный вариант);
г — II стадия (маточный вариант);
д — II стадия (параметрально-вагинальный вариант);
е — III стадия (с поражением лимфатических узлов таза);
ж — IV стадия (с поражением мочевого пузыря).
Классификация патологических состояний шейки матки по клинико-морфологическим признакам представлена выше (см. «Патология шейки матки»).
Согласно клинико-анатомической классификации, различают четыре стадии инвазивного РШМ (рис. 38):
• I стадия — опухоль ограничена только шейкой матки.
• II стадия РШМ имеет три варианта: а — опухоль распространяется на параметрий одной или обеих сторон (параметральный вариант); б — опухоль переходит на влагалище, не захватывая нижнюю треть его (влагалищный вариант); в — опухоль захватывает и тело матки (маточный вариант).
• III стадия также имеет три варианта: а — опухоль поражает параметрий, переходя на стенки таза (параметральный вариант); б — опухоль доходит до нижней трети влагалища (влагалищный вариант); в — опухоль распространяется в виде изолированных очагов в малом тазу при отсутствии отдаленных метастазов (тазовый метастатический вариант).
• IV стадия проявляется следующими вариантами: а — опухоль поражает мочевой пузырь (мочепузырный вариант); б — опухоль поражает прямую кишку (ректальный вариант); в — опухоль переходит за пределы органов малого таза (отдаленный метастатический вариант).
По характеру роста опухоли выделяется еще ряд типов каждого варианта всех четырех стадий. С учетом роста опухоли различают экзофитную (рост наружу в виде цветной капусты) и эндофитную (рост внутрь с инфильтрацией тканей) формы РШМ (рис. 39).
Классификация по системе TNM характеризует размеры и состояние первичного опухолевого очага (T-tumor), регионарных лимфатических узлов (N-nodules) и наличие отдаленных метастазов (M-metastases). Согласно этой классификации, могут быть различные сочетания по поражению опухолью органов и ее распространению: от T1N0M0 до T4NxM1.
Отдельно рассматриваются преинвазивный (интраэпителиальный, карцинома in situ) и микроинвазивный РШМ.
Преинвазивный рак(Са in situ) шейки матки — это патология покровного эпителия шейки матки с признаками рака, при отсутствии инвазии в подлежащую строму. Как и дисплазии, пре-инвазивному раку может предшествовать койлоцитарная атипия.
 Ca in situ может быть в нескольких вариантах зрелый (дифференцированный), незрелый (недифференцированный), переходный и смешанный. Соответственно он может переходить в плоскоклеточный ороговевающий, недифференцированный и низкодифференцированный инвазивный рак. Начинается преинвазивныи рак обычно в зоне трансформации (вокруг наружного зева), а затем распространяется на эндо- или эктоцервикс. Преинвазивныи рак, как и дисплазии, может прогрессировать в инвазивный рак, сохраняться в течение нескольких лет или даже регрессировать. С учетом латентного периода между преинвазивным и инвазивным раком своевременная диагностика и адекватное лечение первого являются важнейшими звеньями снижения частоты инвазивного РШМ. Существенные затруднения представляет дифференциальная диагностика преинвазивного и микроинвазивного РШМ.
Ca in situ может быть в нескольких вариантах зрелый (дифференцированный), незрелый (недифференцированный), переходный и смешанный. Соответственно он может переходить в плоскоклеточный ороговевающий, недифференцированный и низкодифференцированный инвазивный рак. Начинается преинвазивныи рак обычно в зоне трансформации (вокруг наружного зева), а затем распространяется на эндо- или эктоцервикс. Преинвазивныи рак, как и дисплазии, может прогрессировать в инвазивный рак, сохраняться в течение нескольких лет или даже регрессировать. С учетом латентного периода между преинвазивным и инвазивным раком своевременная диагностика и адекватное лечение первого являются важнейшими звеньями снижения частоты инвазивного РШМ. Существенные затруднения представляет дифференциальная диагностика преинвазивного и микроинвазивного РШМ.
Микроинвазивный ракшейки матки — ранняя форма инвазивного — это поражение раковой опухолью слизистой до 1 см в диаметре. Однако и при таких размерах опухоли могут выявляться лимфогенные метастазы. Частота их связывается с глубиной инвазии. До 1 мм она считается минимальной, а уже с 5 мм — клинически значимой с частыми лимфогенными метастазами. Микроинвазивный рак шейки матки может быть обнаружен на фоне дисплазии, преинвазивного рака и их сочетаний. Клиническая характеристика и исходы при микроинвазивном РШМ позволяют считать его формой, более близкой и преинвазивному раку, чем к инвазивному.
Клиническая картина РШМ характеризуется вариабельностью от почти бессимптомного течения до многочисленной симптоматики. Зависит от стадии, характера роста опухоли и ее локализации. Ранние стадии РШМ протекают фактически бессимптомно. Могут отмечаться местные изменения, выявляемые при осмотрах или специальными методами исследования. Появление кровянистых выделений из половых путей, «контактных кровотечений» не следует рассматривать как ранние симптомы. Они возникают при значительном распространении опухоли. Кровянистые выделения появляются раньше, при экзофитных формах РШМ, когда опухоль растет наружу что повышает вероятность механического ее повреждения. Болевой симптом нередко сопровождает раковое поражение шейки матки. Более частым симптомом считаются бели, появляющиеся в связи с повышением секреторной активности шейки матки и влагалища.
Боли, бели и кровянистые выделения чаще наблюдаются при РШМ в поздних стадиях (II—IV). При этом наряду с указанными возникают симптомы, характеризующие нарушение функции смежных органов (мочевой пузырь, прямая кишка и т.д.). Возникают они по мере распространения опухоли.
 Распространение опухоли на окружающие ткани и органы имеет определенные закономерности. Чаще и раньше опухоль распространяется на параметральную клетчатку и регионарные лимфатические узлы. Из соседних органов РШМ чаще поражает мочевой пузырь (при локализации опухоли на передней губе шейки матки) и прямую кишку (при локализации опухоли на задней губе шейки матки). Метастазы в отдаленные органы по частоте их возникновения происходят в следующем порядке печень, легкие, брюшина, кости, желудочно-кишечный тракт, почки, селезенка. Распространяется РШМ лимфогенным и гематогенным путями, а также путем прорастания прилежащих тканей. В отдельных случаях метастазирование сопровождается клинической картиной общей инфекции с повышением температуры, выраженными изменениями в крови, анемией. Непосредственной причиной смерти при РШМ являются местная инфекция, переходящая в сепсис, перитонит, уремия, тромбоз сосудов, анемия вследствие обильных кровотечений при распаде опухоли (рис. 40).
Распространение опухоли на окружающие ткани и органы имеет определенные закономерности. Чаще и раньше опухоль распространяется на параметральную клетчатку и регионарные лимфатические узлы. Из соседних органов РШМ чаще поражает мочевой пузырь (при локализации опухоли на передней губе шейки матки) и прямую кишку (при локализации опухоли на задней губе шейки матки). Метастазы в отдаленные органы по частоте их возникновения происходят в следующем порядке печень, легкие, брюшина, кости, желудочно-кишечный тракт, почки, селезенка. Распространяется РШМ лимфогенным и гематогенным путями, а также путем прорастания прилежащих тканей. В отдельных случаях метастазирование сопровождается клинической картиной общей инфекции с повышением температуры, выраженными изменениями в крови, анемией. Непосредственной причиной смерти при РШМ являются местная инфекция, переходящая в сепсис, перитонит, уремия, тромбоз сосудов, анемия вследствие обильных кровотечений при распаде опухоли (рис. 40).
Диагностика осуществляется в основном с помощью вспомогательных методов исследования. Из последних наряду с клиническими данными и результатами осмотра широко используются следующие: цитология, кольпоскопия во всех ее вариантах, УЗИ, гистология. Распространенность опухолевого процесса оценивается с помощью рентгенографии цервикального канала и полости матки, лимфографии, УЗИ, ангиографии, компьютерной томографии, ядерно-магнитного резонанса. Характеристика указанных методов обследования приведена выше (см. «Патология шейки матки»).
При проведении профилактических осмотров на основании клинико-цитологических данных отбирается контингент женщин для более углубленного обследования по принципу «от простого к сложному»: цитология—кольпоскопия—расширенная кольпоскопия и кольпомикроскопия—гистология—повторные исследования в динамике. Это отражено в представленной схеме взаимодействия специалистов в процессе диагностики РШМ (рис.41).
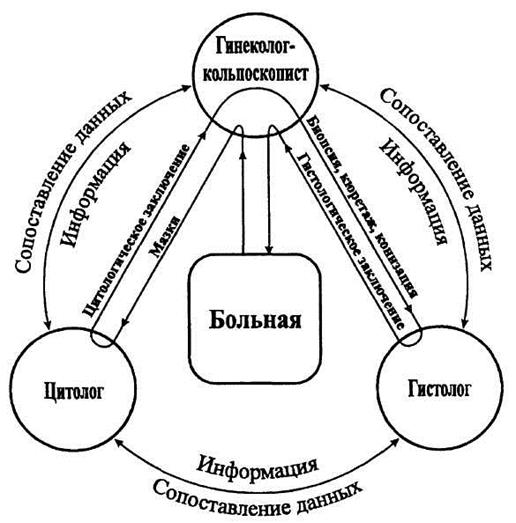
Рис.41. Взаимодействие специалистов в процессе диагностики рака шейки матки (Я.В. Бохман, 1989).
Профилактика РШМ является важной проблемой здравоохранения. Она основана прежде всего на выявлении и своевременном эффективном лечении фоновых и предраковых процессов шейки матки. С этой целью создаются специальные программы, предусматривающие организацию проведения профилактических осмотров всех женщин, систему оповещения женщин в процессе их обследования, обеспеченность обследования с помощью специальных методов, повышение онкологической квалификации гинекологов, усовершенствования цитологов и гистологов, повышение санитарной культуры с онкологической настороженностью населения.
Основная роль в диагностике и профилактике РШМ принадлежит женским консультациям. Проведение профилактических осмотров может быть эффективным в этом плане лишь при использовании цитологического скрининга и проведения по показаниям углубленного обследования.
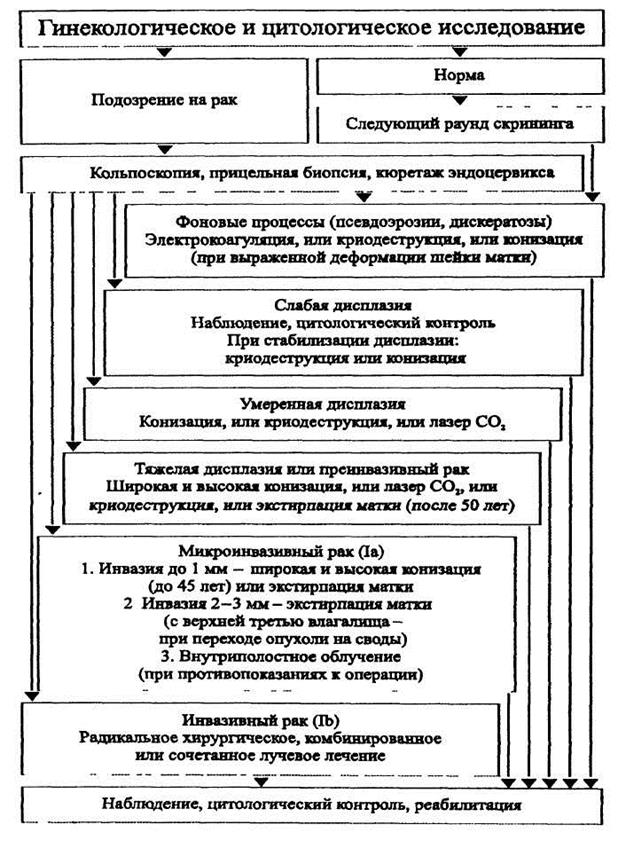
Рис 42. Алгоритм обследования и лечения патологии шейки матки и рака ранних стадий
В группу риска РШМ следует относить всех женщин в возрасте от 20 лет и старше, за исключением не живших половой жизнью и перенесших тотальную гистерэктомию. Эффективность санитарно-просветительной работы по профилактике РШМ можно оценить пониманием необходимости обследования у гинеколога не реже 1—2 раз в течение года.
Принципы лечения рака шейки матки.План лечения (рис. 42) зависит от сущности выявленного патологического процесса, его распространенности в пределах шейки матки, гистотипической характеристики, возраста женщины и состояния менструальной и детородной функций. Лечение РШМ определяется прежде всего распространенностью процесса (преинвазивный, микроинвазивный, I—IV ст.) и гистотипическими особенностями опухоли.
Преинвазивный рак должен быть тщательно дифференцирован с микроинвазивным. Есть разные мнения о тактике лечения Са in situ: от органосохраняющих операций до тотальной гистерэктомии с придатками. По-видимому, можно считать оправданной конусовидную электроэксцизию шейки матки у женщин детородного возраста с тщательным гистологическим исследованием серийных срезов и последующим оптимальным диспансерным наблюдением. Тотальная гистерэктомия с придатками может быть показанной при Са in situ у женщин в перименопаузальный период. И в этот период при наличии Са in situ можно ограничиться конусовидной электроэксцизией шейки матки или внутриполостным облучением у женщин с тяжелой экстрагенитальной патологией. В каждом конкретном случае решение о выборе метода лечения принимается с учетом индивидуальных особенностей.
Лечение микроинвазивного РШМ может быть проведено по таким же принципам, как и Са in situ. Однако при этом должна быть полная уверенность клинициста (и патоморфолога) в том, что в данном конкретном случае имеется именно микроинвазивный рак. Это значит, что клинико-эндоскопическая и морфологическая информации должны подтверждать поверхностную (до 3 мм) инвазию процесса и отсутствие раковых эмболов в кровеносной и лимфатической системах, что практически трудновыполнимо. Поэтому в практике более широкое распространение имеет тенденция радикальных оперативных вмешательств, нередко с дополнительным дистанционным облучением. Выживаемость больных женщин с микроинвазивным РШМ 5 лет и более при различных методах лечения составляет 95—100%. При микроинвазивном РШМ вполне допустима тактика щадящего лучевого и органосохраняющего оперативного лечения.
Лечение инвазивного РШМ осуществляется хирургическими, лучевыми и комбинированными методами. Основой выбора метода лечения является классификация РШМ по стадиям распространенности процесса и системе TNM ст Ia — TlaN0M0, ст Iб — Т1бN0М0, ст IIa — Т2аN0М0, ст IIб — Т2бN0М0, ст IIIa-Т3аN0M0, ст III — T3N0M0 — T3N2M0, ст IV — Т4 и/или М1 при любых вариантах Т и N. Характер опухоли (Т) определяется клиническими методами, с помощью кольпоскопии и УЗИ. Труднее оценить степень поражения лимфатических узлов (N) и наличие метастазов (М). Это достигается с помощью УЗИ, лимфографии, компьютерной томографии и магнитно-ядерного резонанса, а также по оценке функции смежных органов.
В настоящее время используются только хирургическое, только лучевое и комбинированное — хирургическое с облучением лечение РШМ. Облучение может проводиться до операции, после нее, а в отдельных случаях — до и после операции (табл. 11). В ранних стадиях РШМ показаны хирургические и сочетанные с лучевыми методы лечения. При запущенных стадиях РШМ проводится только лучевая терапия. В случаях затруднения определения стадии РШМ (II или III и т.д.) терапия проводится по принципу меньшей стадии (II).
Хирургическое лечение включает конизацию шейки матки (ножевая конизация или электроконизация), простую экстирпацию, операцию Вертгейма (экстирпация с удалением регионарных лимфатических узлов) — расширенную экстирпацию матки, удаление подвздошных лимфатических узлов.
Лучевая терапия проводится по принципу дистанционного облучения и/или внутриполостной гамма-терапии.
Таблица 11. Показания к различным методам лечения РШМ (Я.В.Бохман, 1989)
| Стадия TNM | Клинико- морфологические данные | Предоперационное облучение | Операция | Послеоперационное облучение | Сочетанное лучевое лечение |
| IaT1аN0M0 | Микроинвазивный рак (инвазия в строму не более 3 мм) | — | Экстрафасциальная экстирпация матки с верхней 1/3 влагалища | — | При противопоказаниях к операции — внутриполостная γ-терапия |
| Iб Т1бN0М0 IIа Т2aN0М0 | Возраст до 50 лет и (или) локализация в эндоцервиксе, и (или) аденокарцинома и низкодифференцированный рак, и (или) метастазы в регионарные лимфатические узлы по данным лимфографии | При больших экзофитных опухолях (Т1б) внутриполостная γ-терапия, при IIа — внутриполостное облучение | Операция Вертгейма | Дистанционное облучение показано при 1б (глубина инвазии более 1см), и (или) аденокарциноме и низкодифференцированном раке, и (или) метастазах в лимфатических узлах. При IIа — во всех случаях | При общих противопоказаниях к операции — внут-риполостное +дистанционное облучение |
| Iб Т1бN0M0 IIа Т2aN0М0 | Возраст старше 50 лет, плоскоклеточный рак, негативные данные лимфографии | — | — | — | Внутриполостное + дистанционное облучение |
| IIб T2б.N0M0 T2бN0M0 IIIa Т3aN0M0 T3aN1M0 | Опухоль инфильтрирует параметрий, не доходя до стенки таза (T2б), или нижнюю треть влагалища (T3а) | Через 10—14 дней после курса сочетанной лучевой терапии при позитивных данных лимфографии — экстраперитонеальное удаление подвздошных узлов | — | Внутриполостное + дистанционное облучение | |
| IIIб T3бN0M0 T3бN1M0 | Опухоль инфильтрирует параметрий до стенки таза | Внутриполостное + дистанционное облучение | |||
| IV T4N0M0 T4N0M0 IV | Опухоль прорастает в мочевой пузырь и(или) прямую кишку | — | Дистанционное облучение таза по индивидуальному плану | ||
| T1-1N0-2 M1 | Отдаленные метастазы | Дистанционное облучение таза + химиотерапия по индивидуальному плану |
Дистанционное облучение на первом этапе сочетанной лучевой терапии уменьшает воспалительный компонент, вызывает дистрофические изменения в опухоли, уменьшая ее объем, и тем самым создает благоприятные условия для последующей внутриполостной гамма-терапии. На втором этапе дистанционное облучение проводится в промежутках между сеансами внутриполостной гамма-терапии.
Внутриполостная гамма-терапия используется в различных вариантах: традиционном; по принципу ручного последовательного введения аппликаторов и радионуклидов низкой мощности дозы; по принципу автоматизированного введения радионуклидов высокой активности с помощью шланговых гамма-терапевтических аппаратов.
При внутриполостной гамма-терапии расчет поглощенных доз проводится по анатомическим областям, исходя из суммарной активности вводимых в полость матки и влагалища радионуклидных источников (типа 60Со) облучения. При этом большие дозовые нагрузки попадают на не пораженные опухолью органы и ткани (мочевой пузырь, прямую кишку и др.).
Принцип ручного последовательного введения радионуклидных источников представляет более усовершенствованный метод внутриполостной гамма-терапии. Совершенствование достигается этапностью лечебного процесса. На первом (подготовительном) этапе осуществляется рентгенологический контроль за правильностью установки системы облучения, что дает возможность ее корректировки при необходимости. После этого вводятся радионуклидные источники облучения (уже в палате) и осуществляется процесс терапии — это уже второй этап.
Таким методом удается несколько уменьшить лучевую нагрузку на смежные органы и ткани, повысить выживаемость больных.
Аппаратная методика внутриполостной гамма-терапии дает возможность управлять процессом облучения дистанционно, что почти исключает опасность облучения персонала, улучшает переносимость терапии больными и уменьшает лучевую нагрузку на соседние органы. При этом существенно уменьшаются продолжительность сеанса облучения (20—70 мин, при ранее изложенных методиках — 22—45 ч) и суммарная доза поглощения (40—50 Гр, при других методиках — 70—90 Гр). При аппаратном методе внутриполостной гамма-терапии значительно выше выживаемосгь больных — 5 лет и более. Имеются различные аппараты для внутриполостной гамма-терапии при РШМ (АГАТ-В, селектрон). Используются источники излучения низкой и высокой активности.
Наиболее частыми осложнениями лучевой терапии являются иммунодепрессивные состояния, лейкопения, воспалительные процессы влагалища, мочевого пузыря, прямой кишки и других локализаций.
Выживаемость (5 лет и более) больных при РШМ зависит от стадии распространения процесса, гистотипа опухоли и методов терапии. Она колеблется, по данным разных авторов, при РШМ I стадии от 75 до 98%, II стадии — 60—85% и III стадии — 40—60%.
Комбинированное лечение — это сочетание хирургического вмешательства с лучевой терапией.
Предоперационная лучевая терапия проводится путем дистанционного или внутриполостного облучения, а также их сочетанием. Чаще применяется наружное равномерное облучение таза.
Комбинированное лечение проводится больным при РШМ I и II стадий. При РШМ III—IV стадий выполняется только лучевая терапия. Послеоперационная лучевая терапия не проводится при микроинвазивном РШМ (Iа стадия) и в отдельных случаях (инвазия менее 1 см, отсутствие метастазов в лимфатические узлы, уверенность в радикальности оперативного вмешательства) при РШМ Iб стадии.
По особым программам с учетом индивидуальных особенностей проводится лечение рецидивов и метастазов РШМ. При рецидивах РШМ также используются хирургические вмешательства, повторная лучевая и химиотерапия.
Химиотерапия хотя и используется при лечении рецидивов РШМ, широкого распространения не получила в связи с недостаточной эффективностью.
Дата добавления: 2014-12-16; просмотров: 2157;
