Химические свойства
Атом углерода карбонильной группы находится в состоянии sp2-гибридизации (плоский фрагмент). Электроны двойной связи сильно смещены в сторону более электроотрицательного атома кислорода (связь С=О полярная). Перераспределение зарядов в карбонильной группе оказывает влияние на полярность С–Н связей соседнего с карбонильной группой атома углерода (a-положение):
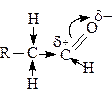
Для альдегидов и кетонов характерны реакции присоединения по двойной связи карбонильной группы и реакции замещения атома водорода у a-атома углерода на галоген. Кроме того, альдегиды способны окисляться по атому водорода при карбонильной группе.
Реакции присоединения по двойной связи С=О группы (нуклеофильное присоединение SN)
В связи с тем, что связь С=О альдегидов и кетонов имеет полярный характер, она легко разрывается под действием полярных молекул типа Н–Х. В общем виде реакцию можно представить в виде:
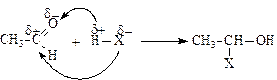
1. Присоединение водорода (восстановление альдегидов и кетонов до первичных и вторичных спиртов):
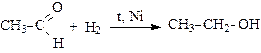
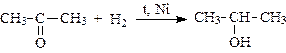
2. Присоединение воды (гидратация) – обратимый процесс (гидраты устойчивы только в водных растворах):
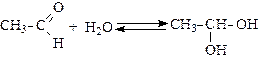
Метаналь в водных растворах гидратирован на 100%, этаналь – на 50%, ацетон практически не гидратирован.
3. Присоединение спиртов:
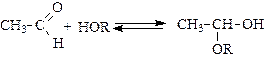 (полуацеталь);
(полуацеталь); 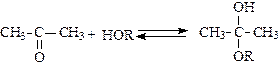 (ацеталь).
(ацеталь).
4. Присоединение гидросульфита натрия (реакция служит для выделения альдегидов и кетонов из смесей с другими органическими веществами):
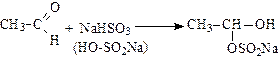
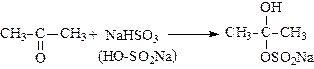 .
.
5. Присоединение аммиака (H–NH2) и аминов (H–NHR):
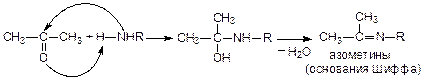
Особым образом происходит присоединение аммиака к уксусному и муравьиному альдегидам:
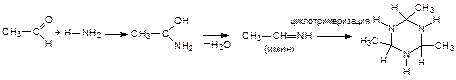
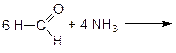
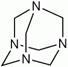
(гексаметилентетрамин – уротропин, дезинфицирующее средство в урологии при воспалении мочевых путей)
5. Присоединение гидразина (H2N–NH2) и фенилгидразина (H2N–NH–С6H5):
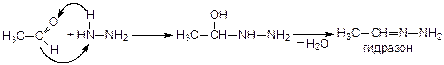
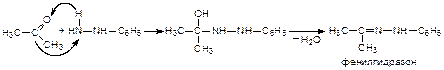
5. Присоединение гидроксиламина (NH2OH):
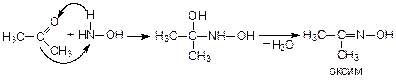
Реакции замещения атома водорода у a-атома углерода
Ослабление связи в СН2-группе углеводородного радикала, соседней с функциональной группой альдегида (a-положение), приводит к тому, что именно эти атомы водорода преимущественно заменяются на галоген:
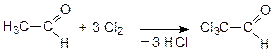
(сильные лакриматоры – вещества, вызывающие слезоотделение).
Иодоформная проба – качественная реакция на соединения с карбонильной группой:
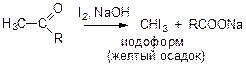
Так как первичные и вторичные спирты окисляются иодом до альдегидов и кетонов, то для них тоже характерна иодоформная проба:
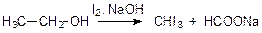
Конденсация альдегидов и кетонов
Реакции идут с участием карбонильной группы и атома водорода в a-положении.
1. Альдольная конденсация:
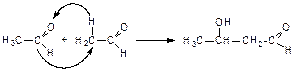
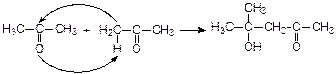
2. Кротоновая конденсация:
При нагревании щелочных растворов альдегидов и кетонов продукты альдольной конденсации отщепляют воду (кротоновая конденсация):
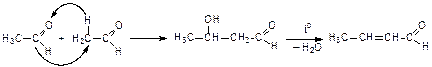
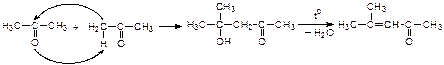
Реакции окисления альдегидов и кетонов
1. Реакция серебряного зеркала (качественная реакция на альдегиды):
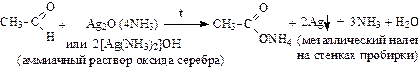
2. Реакция с гидроксидом меди (II) (качественная реакция на альдегиды):
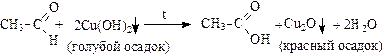
Окисление метаналя (муравьиного альдегида) в этих условиях идет до образования карбоната аммония или оксида углерода (IV):
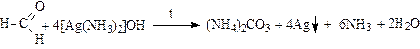
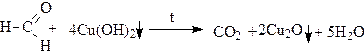
Кетоны в «мягких» условиях (при нагревании с аммиачным раствором оксида серебра или гидроксида меди (II) не окисляются. В «жестких» условиях (нагревание с перманганатом калия или дихроматом калия) окисляются с разрывом углеродной цепи и образованием смеси кислот:
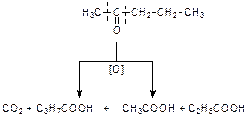
Полимеризация низших альдегидов
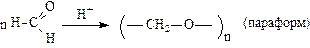
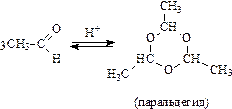
Кетоны в реакции полимеризации не вступают.
Дата добавления: 2016-11-02; просмотров: 1137;
