в історичному аспекті 24 страница
специфічних антитіл мало б призвести до зниження реплікації вірусу. Проте
в умовах, наприклад, порушеного фагоцитозу не відбувається належної анти-
генної презентації, що зрештою призводить до формування недостатньо спе-
цифічних антитіл до даного штаму вірусу. При цьому серологічні дослідження
можуть вказувати на достатню специфічність сформованих антитіл, однак слід
враховувати, що такі дослідження орієнтовані лише на певні типові антигени
і не враховують особливості антигенного спектру конкретного штаму віру-
су. Дисоціацією також є відсутність клінічного регресу симптомів запалення
при переході у лімфоцитарну фазу імунної відповіді на бактеріальні патогени.
Причина такої дисоціації може полягати у зниженні функціональної активнос
ті лімфоцитів, дефектах продукції антитіл, синтезі недостатньо специфічних
антитіл внаслідок зниження фагоцитозу. Ще одним прикладом дисоціації є на-
явність документально підтвердженої вірусної інфекції на тлі ознак переважно
гуморального напрямку розгортання імунної відповіді за даними імунограми.
Можна навести ще чимало прикладів дисоціації між клінічними, імунологіч-
ними даними і результатами загального аналізу крові. Важливо наголосити,
що синдром дисоціації є ознакою ІДЗ і краще виявляється при динамічному
проведенні досліджень і комплексній оцінці їх результатів.
§5. Клініко-імунологічна характеристика стадій гострого
запального процесу
Оцінку імунологічних даних слід проводити у світлі стадії запального про-
цесу. Розглянемо динаміку змін при гострій запальній відповіді на бактеріаль-
ні патогени при нормальному вихідному стані імунної системи і сприятливому
перебігу хвороби (наприклад, при частковій пневмонії). Будь-який запальний
процес характеризується наступними стадіями (рис. 25):
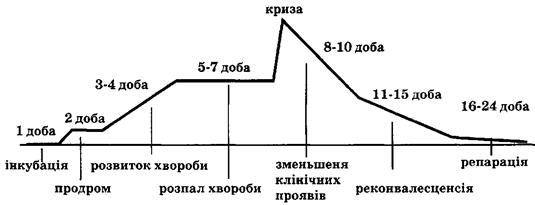
Рис. 25. Стадії гострої запальної відповіді (на прикладі бактеріальної пневмонії)
1. Інкубаційний період (інапарантний);
2. Продром;
3. Розпал хвороби:
• розвиток;
• розгорнута картина;
• криза;
• завершення клінічних проявів.
4. Реконвалесценція:
• рання;
• пізня;
• одужання (репарація).
Слід пам'ятати, що розвиток гострого запального процесу значною мірою
залежить принаймні від трьох умов.
І. Від вихідного (кількісного і якісного) стану імунної системи, який у свою
чергу залежить від того:
а) чи знаходилася імунна система у нормальному функціональному стані;
б) чи мали місце у хворого ті чи інші дефекти імунітету (компенсовані або
декомпенсовані);
в) чи знаходиться імунна система під дією раніше перенесеної хвороби або
певного поточного захворювання.
II. Від кількості і якості патогену, його інвазивності, агресивності, ток-
сичності.
III. Від локалізації патологічного процесу.
Кожному клінічному етапу запального процесу відповідають певні зміни в
лейкограмі й імунограмі. Послідовність цих змін схематично показана на табл.
27. Наявність або відсутність вказаних зрушень в лейкограмі та імунограмі ха-
рактеризують динаміку тієї чи іншої стадії захворювання. Ці дані можуть бути
основою для прогнозування перебігу хвороби і корекції лікувальних заходів за
1-2 доби до появи клінічних ознак можливих ускладнень.
Таблиця 27.
Динаміка показників лейкограми та імунограми
при гострому запальному процесі бактеріального генезу
за умови його сприятливого перебігу
| Стадія | Лейкограма | Імунограма |
| Інкубація | TlgM, tlgE | |
| Продром | Еозинопенія (менше 2 %), відносний нейтрофільоз | 4-т-л, tigM |
| Розвиток захворювання | Лейкоцитоз, абсолютний нейтрофільоз | 4Т- л, f Т- х, ^Т-ц |
| Розпал | Паличкоядерне зміщення формули нейтрофілів, відсутність еозинофілів | ТТ-л, ТТ-х, ІГ-ц, llgM |

В інкубаційному періоді, як правило, відсутні будь-які клінічні прояви,
але можна виявити підвищений рівень IgM і IgE.
На стадії продрому характерна наявність мінімальних клінічних проявів,
які часто не фіксуються клініцистами. На цій стадії в організмі є достатня кіль-
кість антигену, який підлягає знищенню, що і призводить до активації імунної
системи. У цей час фіксуються певні зміни в лейкограмі та імунограмі. По-
перше, найбільш ранньою ознакою продрому є зниження відсоткового вмісту
еозинофілів і базофілів у циркуляції у зв'язку з переміщенням їх до осередку
запалення та дією глюкокортикоїдів. По-друге, відзначається зменшення від-
носної кількості Т-лімфоцитів і наростання вмісту так званих нульових клітин
(недостатньо диференційованих лімфоцитів). В кінці продрому за 1-2 доби
до розвитку симптомів захворювання відмічається відносний нейтрофільоз.
Індекс навантаження зменшується.
Стадія розвитку клінічної картини захворювання. Клінічно протягом
цієї стадії відзначається поступове наростання температури тіла, ознак інтокси-
кації, збільшення осередкових ознак пневмонії-прогресуюче притуплення пер-
куторного тону і послаблення везикулярного дихання, поява crepitacio indux.
Динаміка лейкограми та імунограми допомагає прогнозувати перебіг
процесу. Цей період захворювання характеризується наростаючим лейкоци-
тозом, що досить чітко корелює з поширеністю і силою запального процесу.
Збільшується абсолютний і відносний вміст нейтрофілів, підвищується фа-
гоцитарна активність цих клітин. В результаті збільшення кількості палич-
коядерних і юних форм з'являється зсув ядерної формули нейтрофілів вліво.
Кількісно ступінь зсуву формули корелює із тяжкістю процесу. Відмічається
подальше зниження відсоткового рівня еозинофілів (аж до повного зникнен-
ня) і Т-лімфоцитів, наростання вмісту нульових клітин. Спостерігається під-
вищення відносного вмісту Т-хелперів і зниження рівня цитотоксичних Т-лім-
фоцитів (імунорегуляторний індекс підвищується). Індекс навантаження сягає
мінімальних значень.
На стадії розгорнутої клінічної картини пневмонії спостерігається мак-
симальна температурна реакція, найбільш виражені ознаки інтоксикації і ди-
хальної недостатності. Вогнищеві зміни також досягають свого апогею - ре-
єструється тупий перкуторний тон, зникає везикулярне дихання і вислухову-
ється бронхіальне, зникає крепітація. Відповідно до зазначених клінічних змін
визначаються такі лабораторні зрушення:
• лейкоцитоз досягає максимальних значень;
• підвищується ШОЕ і швидко досягає високих цифр, характеризуючи інтен-
сивність запальної відповіді;
• розвивається відносний моноцитоз;
• відбувається зниження відносного вмісту нейтрофілів за рахунок підвищен-
ня відсоткового вмісту лімфоцитів;
• відмічається подальше зміщення ядерної формули нейтрофілів вліво (по-
при зниження їх відсоткового вмісту), іноді - до появи метамієлоцитів, що
характеризує високу інтенсивність запального процесу;
• продовжує наростати фагоцитарна активність нейтрофілів.
Важливим критерієм збереження інтоксикації в період розгорнутої клініч-
ної картини є збереження анеозинофілії. Зниження адгезійної активності ней-
трофілів корелює з патологічною зернистістю нейтрофілів, що свідчить про
тяжкість інтоксикації. Несприятливою ознакою є поява лейкопенії, яка поєд-
нується з різким зниженням рівня Т-лімфоцитів. Іншою несприятливою озна-
кою може бути зниження фагоцитарної активності нейтрофілів.
Криза. Криза є переломним моментом у гострій запальній відповіді. В
клініці ознакою перелому є відповідна динаміка температурної реакції - спо-
стерігається зниження температури тіла, яке може відбуватися критично або
літично. Найважливішою лабораторною ознакою перелому є нормалізація від-
носного вмісту еозинофілів, що на початку минулого століття назвали "зорею
одужання". Для практикуючого лікаря ця ознака дуже важлива, оскільки про-
являється вона за 1-2 доби до клінічних ознак перелому, після чого розпо-
чинається зниження кількості лейкоцитів. Отже, поява еозинофіли у другій
половині запальної відповіді зазвичай є не свідченням приєднання алергійної
патології, а сприятливою прогностичною ознакою.
Зменшення клінічних проявів. Протягом цього періоду спостерігається
подальше зниження температури тіла, зменшення ознак інтоксикації, позитивна
динаміка вогнищевих змін - підвищення звучності перкуторного тону, усунен-
ня бронхіального дихання і поява везикулярного, реєстрація crepitacio redux.
Лабораторно відмічається зростання відносної кількості В-лімфоцитів,
іноді навіть дуже значне. Крім того, має місце збільшення кількості цитотоксичних Т-клітин щодо рівня Т-хелперів (зменшення імунорегуляторного
індексу), що є ключовою лабораторною ознакою позитивної динаміки хво-
роби. Знижується вміст нульових клітин. Відновлення кількості лімфоцитів
зазвичай співпадає з фактом одужання. Паралельно нормалізується кількість
лейкоцитів, зникає зміщення ядерної формули нейтрофілів. При цьому спо-
чатку зникають юні форми нейтрофілів. Якщо ж спостерігається інша тенден-
ція - зменшується вміст паличкоядерних форм при збереженні юних, існує не-
безпека приєднання лейкемоїдної реакції. На цій стадії зберігається високий
відсотковий вміст лімфоцитів, підвищені цифри ШОЕ. Індекс навантаження
поступово збільшується.
Реконвалесценція. Протягом періоду реконвалесценції відбувається оста-
точна нормалізація температури тіла, усунення ознак інтоксикації, ліквідація
осередкових змін у легенях. Тривало можуть зберігатися астенічні прояви.
Лабораторними ознаками реконвалесценції є нормалізація відсоткового
вмісту усіх субпопуляцій лейкоцитів і усунення лейкоцитозу. Важливим є ви-
рішення питання щодо завершеності запального процесу. Надійною ознакою
незавершеності процесу є збереження низького рівня Т-лімфоцитів при ви-
сокому вмісті нульових клітин. Крім того, ознакою хронізації інфекції може
бути тривале збереження високого рівня В-лімфоцитів і моноцитів. У період
реконвалесценції зберігаються високі цифри ШОЕ, продовжує зростати індекс
навантаження.
Типи імунограми. Характерною особливістю зазначеної динаміки імуно-
логічних показників є зміна нейтрофільної фази раннього періоду на лімфоци-
тарну при завершенні імунної відповіді. Це так званий нейтрофільно-лімфо-
цитарний тип імунограми, який зустрічається при бактеріальних інфекціях.
Нейтрофільний тип імунограми, при якому лімфоцитарна фаза максималь-
но скорочена, характерний для тих бактеріальних інфекцій, у патогенезі яких
провідну роль відіграє не сам збудник, а синтезований ним токсин (дифтерія,
ботулізм, холера). Для інфекцій, спричинених внутрішньоклітинними парази-
тами (віруси, мікоплазми, хламідії тощо), притаманний лімфоцитарний тип
імунограми, при якому суттєво обмежена у часі нейтрофільна фаза запалення.
Провідними змінами за такої імунограми є лімфоцитоз і моноцитоз, оскільки у
цьому разі саме природні кілери, цитотоксичні Т-лімфоцити і армовані макро-
фаги є основними ефекторними клітинами.
Стадійних змін зазнають і показники цитокінового балансу. В періоді про-
дрому, початкових клінічних проявів, розпалу синтезуються переважно так
звані прозапальні доімунні цитокіни: ІЛ-1р, ФНП-а, ІЛ-6, ІЛ-8 та деякі інші.
В подальшому переважають цитокіни специфічної (адаптивної) відповіді. При
цьому відбувається перебудова цитокінового каскаду відповідно до спрямова-
ності імунної відповіді - за Th 1 типом (з переважним синтезом ІФН-у й ІЛ-2)
при вірусних і грибкових інфекціях або за Th 2 типом (з переважним синтезом
ІЛ-4, ІЛ-5, ІЛ-6, ІЛ-10) при бактеріальних інфекціях. У період реконвалесцен-
ції зростає рівень цитокінів, які забезпечують згортання імунної відповіді (ІЛ-
10, ТФР-Р).
Всі зазначені лабораторні зміни спостерігаються при адекватній імунній
відповіді. В умовах ІДЗ має місце нечіткість вирізнення окремих клінічних
стадій запалення у зв'язку з млявістю імунної відповіді, а також невідповід-
ність лабораторних змін клінічній стадії запалення і відсутність характерних
змін окремих показників один щодо одного (так званий синдром дисоціації).
Виявлення синдрому дисоціації є одним із критеріїв постановки діагнозу ІДЗ.
Розділ 4. Клінічна імунопатологія
ГЛАВА І. ДИСФУНКЦІЇ ІМУННОЇ
СИСТЕМИ: ІМУНОДЕФІЦИТНІ ХВОРОБИ
Й ІМУННА НЕДОСТАТНІСТЬ
§1. Визначення, класифікація і клінічні прояви
дисфункцій імунної системи
Імунний статус - це стан імунної системи даної людини в конкретний
момент часу, виражений у клінічних симптомах і спеціальних лабораторних
показниках, які характеризують функцію різних ланок імунної системи.
Дисфункція ІМУННОЇ системи - клінічно маніфестне імунне порушення,
верифіковане за результатами імунологічних лабораторних досліджень у дина-
міці, а також за анамнестичними критеріями і даними генеалогічного дерева.
Дисфункції імунної системи лежать в основі аутоімунної, алергійної, лім-
фопроліферативної, неопластичної патології. Але найчастіше вони проявля-
ються у вигляді інфекційного синдрому. З іншого боку, дисфункції імунної
системи самі можуть бути наслідком інфекцій органів і клітин імунної систе-
ми (наприклад, при СНІДі).
Усі дисфункції можна розділити на дві великі групи: імунодефіцитні за-
хворювання (ІДЗ) і імунну недостатність (IH).
Імунодефіиитними називаються захворювання, які розвиваються внаслі-
док дефектів або дефіциту тих чи інших факторів імунітету.
Спадковими вважаються ІДЗ за умови наявності в родоводі імунодефі-
цитних захворювань у кількох поколіннях, а також декількох клінічних крите-
ріїв ІДЗ у пацієнта і відповідних лабораторних імунологічних даних.
Природженими вважаються ІДЗ при встановленому факті дії протягом
антенатального періоду факторів, які порушують внутрішньоутробний роз-
виток, а також декількох клінічних критеріїв ІДЗ і відповідних лабораторних
імунологічних даних.
Набутими вважаються ІДЗ при встановленому факті дії протягом по-
стнатального періода факторів, які порушують становлення і функціонування
імунної системи, декількох клінічних критеріїв ІДЗ і відповідних лаборатор-
них імунологічних даних, які стійко зберігаються і після усунення провоку-
вальних факторів.
ІМУННОЮ недостатністю вважаються клінічно маніфестні порушення
імунної системи, обумовлені віковими особливостями (фізіологічна) або осно-
вним захворюванням (вторинна), які зникають протягом терміну до 6 місяців
після усунення причинних захворювань або факторів. У зв'язку з цим хворі з
ІН не потребують призначення специфічних імунотропних засобів.
Найчастіше доводиться проводити диференціальну діагностику між набу-
тим імунодефіцитним захворюванням і вторинною імунною недостатністю.
Варто розуміти, що набуте ІДЗ є окремою нозологічною одиницею (хворобою),
що має самостійний перебіг. Це означає, що набуте ІДЗ клінічно маніфестує
навіть за умови усунення причинного захворювання або фактора, оскільки в
основі такої дисфункції лежить стабільний імунний дефект. Хворі з набутими
ІДЗ потребують обов'язкового призначення імунотропної терапії.
Вторинна імунна недостатність (ВІН) є не самостійним захворюванням,
а патологічним станом. ВІН розвивається при багатьох бактеріальних і вірус-
них інфекціях, захворюваннях печінки і нирок, медикаментозній і променевій
терапії, більшості хронічних соматичних захворювань, у результаті стресових
ситуацій, порушень харчування, при протозойних і гельмінтозних захворю-
ваннях. ВІН - супутник будь-якого хронічного процесу, результат тривалого
застосування імунодепресантів, кортикостероїдів, деяких антибіотиків (тетра-
цикліну, левоміцетину), сульфаніламідних препаратів, голодування, утрати
білка, розладів харчування, порушення усмоктування в кишківнику, тривалої
білкової або вітамінної недостатності.
Як видно зі схеми 8, діагноз вторинної імунної недостатності може транс-
формуватися в діагноз набутого ІДЗ у випадку стабільного збереження клі-
нічно маніфестних імунних розладів протягом більше 6 місяців від моменту
усунення основного захворювання або причинного фактору.
Діагноз імунодефіцитного захворювання повинен ґрунтуватися на клініко-
анамнестичних даних (основний критерій), підкріплених даними генеалогіч-
ного дерева й імунограми. Сьогодні добре вивчені основні клінічні, анамнес-
тичні і генеалогічні критерії дисфункцій імунної системи.
Скринінгові клініко-анамнестичні критерії для
виявлення дисфункцій імунної системи:
І. Клінічні симптоми:
1) виражена стигматизація (більше 5-ти стигм);
2) відставання дитини в зрості і масі;
3) симптоми хронічного або рецидивного отиту (не менше 4-х разів на рік) і
синуїту (не менше 4-х разів на рік), менінгіту, пародонтиту, паротиту з ре-
цидивним перебігом; рецидивного бронхіту і пневмонії (не менше 2-х разів
на рік);
4) хронічний або рецидивний ентерит, тривало не заживаючі виразки слизових
оболонок, стійкий синдром мальабсорбції, а також лямбліоз і гельмінтози з
рецидивним перебігом;
5) рецидивні гнійні ураження: фурункули, карбункули, парапроктити, абсце-
си, стафіло-, стрептодермії, піурія неясного генезу, остеомієліт, сепсис;
6) рецидивні герпес-вірусні інфекції й інфекції, викликані умовно-патогенною
мікрофлорою;
7) хронічна або рецидивна лихоманка неясного генезу;
8) персистуюча пліснявка і грибкові ураження шкіри, слизових, внутрішніх
органів;
9) лімфаденопатія з ранньою декомпенсацією (тонзилектомія, апендектомія);
гепатолієнальний синдром неясного генезу;
10) гіпер- і гіпоплазія тимусу; гіпо- або аплазія лімфоїдної тканини, особливо
під час запальних процесів;
11) потреба у тривалому використанні антибіотиків для лікування інфекції (до
2-х місяців і більше), а також необхідність їх внутрішньовенного введення.
II. Сімейний анамнез (генеалогічне дерево):
Нез'ясовані випадки смерті грудних дітей і дітей першого року життя, а та-
кож летальні випадки, пов'язані з інфекційними захворюваннями, муковісци-
дозом; хронічні і рецидивні інфекційні захворювання у родичів (три і більше
по вертикалі або горизонталі); гемопатії у родичів; вади розвитку, стигми ди-
зембріогенезу у родичів; ендокринопатії; алергійні захворювання; аутоімунні
захворювання (СЧВ, тироїдит Хашимото й ін.); злоякісні новоутворення у ро-
дичів; туберкульоз; герпетичні інфекції; кревна спорідненість батьків.
III. Антенатальний анамнез:
Вірусні і бактеріальні захворювання матері протягом першого триместру
вагітності; застосування медикаментів, зокрема гормонів, антибіотиків, суль-
фаніламідів, протизапальних засобів; вплив несприятливих екологічних фак-
торів; шкідливі фактори виробництва і побуту; ранні гестози; загроза пере-
ривання вагітності в ранній термін (тривале застосування прогестинів); пору-
шення харчування вагітної; загострення хронічних захворювань матері під час
вагітності; значні стресові навантаження; патологічний перебіг пологів.
IV. Анамнез життя і хвороби:
Виникнення захворювань у ранньому віці; рання поява рецидивних інфек-
цій: бронхолегеневих захворювань (бронхіти, пневмонії), гнійних отитів, си-
нуїтів, діареї, екземи, фурункульозу, абсцесів, герпетичних висипань, остеомі
єліту, піурії неясного генезу; тяжкість і маніфестність захворювань; тривалий
субфебрилітет; генералізовані процеси і реакції; неефективність традиційної
терапії; розвиток аутоімунних і неопластичних захворювань; побічні реакції
на вакцинацію, алергійні реакції на медикаменти; алергійні захворювання;
тривале застосування глюкокортикоїдів, цитостатиків, сульфаніламідів, анти-
гістамінних препаратів, особливо в ранньому дитячому віці.
V. Лабораторні дані:
Лімфоцитопенія менше 1,0х109/л або лімфоцитоз; нейтропенія; тяжка ге-
молітична або апластична анемія; тромбоцитопенія; гіпоглобулінемія, особли-
во у-фракції; еозинопенія; сповільнена ШОЕ при бактеріальних інфекціях;
Пояснення до клініко-анамнестичних критеріїв:
І. При наявності клінічних симптомів І групи, одного або більше критеріїв
II групи (сімейний анамнез) і одного або більше критеріїв з IV групи (анамнез
хвороби) діагностують спадкове ІДЗ.
II. При наявності клінічних симптомів І групи і відсутності критеріїв II
групи (сімейний анамнез), але наявності одного або більше критеріїв III (анте-
натальний анамнез), IV (анамнез хвороби) діагностують природжене ІДЗ.
III. При наявності клінічних симптомів І групи і відсутності даних П (сі-
мейний анамнез) і III (антенатальний анамнез) груп, але наявності одного або
більше критеріїв IV (анамнез хвороби) діагностують набуте ІДЗ.
На підставі наведених даних створена клінічна класифікація дисфункцій

імунної системи за Казмірчук В. Є. (схема 8).
Скринінгові лабораторні імунологічні тести:
• вміст імуноглобулінів основних класів G, А, М у сироватці крові;
• вміст Т-лімфоцитів у крові;
• вміст В-лімфоцитів;
• оцінка фагоцитозу.
Існує класифікація первинних ІДЗ, запропонована експертами ВООЗ у
1997 році. Вона ґрунтується на характері імунологічного дефекту, що виникає в
процесі диференціювання імунокомпетентних клітин. Однак ІДЗ у вигляді кла-
сичних синдромів, зазначених у класифікації, зустрічаються вкрай рідко. Частіше
лікарю доводиться зустрічатися з фенокопіями спадкових ІДЗ - природженими
або набутими імунодефіцитними захворюваннями, які відповідають за клініко-
лабораторними даними тій або іншій формі спадкового ІДЗ, але не спадкуються.
Епідеміологія дисфункцій імунної системи. Частота класичних ІДЗ
установлена тільки в цивілізованих країнах. Вона різна і залежить від стану
охорони здоров'я в країні. Поширеність малих аномалій імунітету у світі не
встановлена, але ясно, що вона на кілька порядків вище класичних первинних
ІДЗ. У зв'язку з цим ми даємо виклад ІДЗ згідно МКХ-10, орієнтуючи читача
на сучасний погляд на проблему.
Останнім часом, у зв'язку з виявленням молекулярних дефектів, що лежать
в основі багатьох імунодефіцитів, і істотною варіабельністю клінічної картини
і тяжкості перебігу спадкових імунодефіцитних захворювань, усвідомленням
можливості їх пізньої маніфестації, у тому числі в дорослих, стає ясно, що
спадкові ІДЗ - це не настільки рідкісний стан, як це вважалося раніше.
Якщо орієнтуватися на дані Європейського регістру первинних імуноде-
фіцитів (звіт ESID за липень 1997), то співвідношення числа зареєстрованих
хворих до населення в середньому по Європі складає 1:96000. В окремих захід-
ноєвропейських країнах цей коефіцієнт дорівнює 1:38000 (Великобританія),
1:25000 (Нідерланди), 1:12500 (Швейцарія) і навіть 1:10000 (Швеція). Немає
підстав вважати етнічні відмінності в Європі фактором, що істотно впливає
на реальну частоту захворювань. Розходження в частоті на порядок можна
пов'язати з якістю виявлення й активністю реєстрації хворих. Таким чином,
варто орієнтуватися на найвищі з зареєстрованих показників (які також можна
вважати заниженими).
При уточненні характеру і ступеня імунної недостатності, використання
навіть найсучасніших методів оцінки імунного статусу не дозволяє адекватно
інтерпретувати стан імунної реактивності організму без врахування її фізіоло-
гічних коливань.
У літературі довгий час не існувало вказівок на те, що вважати зниженням
показників окремих ланок імунітету. Слід зазначити, що розкид індивідуаль-
них коливань окремих показників у дітей значно ширший, ніж у дорослих.
Проведені дослідження у здорових дітей раннього віку показали, що фізі-
ологічні коливання кількості Т- і В-лімфоцитів у різні сезони року можливі до
40 %, що складає відхилення від середньостатистичних сезонних показників
у межах двох сигм. Кількість імуноглобулінів G, А, М в сироватці крові, Т і
В-лімфоцитів змінюється протягом року - максимальний вміст відзначається
в осінньо-зимовий період, мінімальний - улітку. Цілком очевидно, що для пра-
вильної оцінки імунної реактивності необхідно оцінювати показники імуніте-
ту з урахуванням сезону року. Однак дотепер не впроваджена єдина система
оцінки дефектів імунітету.
Для уніфікації оцінки імунної дисфункції варто виділяти ступінь її вираз-
ності. За імунну недостатність першого ступеня, що супроводжується відпо-
відними клінічними проявами, варто приймати зниження окремих показників
імунної системи на 50 % від нижньої межі вікової норми, що не завжди су-
проводжується декомпенсацією імунних механізмів захисту. Другий ступінь
імунної недостатності супроводжується частими рецидивами захворювань,
що створюють замкнуте коло, з якого хворому важко вийти без відповідної
імунокоригуючої терапії, і характеризується зниженням окремих показників
більше ніж на 50 % від нижньої межі середньостатистичної сезонної норми.
Клінічні прояви ІДЗ. Л. Йєгер (1990) усі клінічні форми ІДЗ розділив на
З основні групи:
1) синдром септицемії, септикопіємії з гнійними ураженнями шкіри, менінгі-
том, артритами й остеомієлітом;
2) синдром рецидивних отитів, синуїтів, бронхітів, пневмоній, інфекцій ди-
хальних шляхів; інфекцій сечовивідних шляхів;
3) шлунково-кишковий синдром із хронічним ентеритом, колітом, проявами
порушеного всмоктування, зі спруподібним синдромом.
Сьогодні стало зрозуміло, що зазначені синдроми - далеко не єдині мож-
ливі клінічні прояви ІДЗ. Останнім часом з'ясували, що в цілому ІДЗ зустрі-
чаються набагато частіше, ніж добре вивчені первинні (спадкові) синдроми.
Виникає питання: чому ІДЗ так рідко діагностуються? Оскільки постановка
такого діагнозу цілком можлива за клініко-анамнестичними даними, недоступ-
ність імунологічних лабораторних досліджень не може служити поясненням
низького ступеня виявлення імунодефіцитних захворювань. Справа в тому, що
для постановки правильного діагнозу в клініциста повинна бути певна імуно-
логічна настороженість, оскільки ІДЗ не мають специфічних симптомів і про-
являються у вигляді "масок" інших захворювань (хронічного бронхіту, хроніч-
ного пієлонефриту, рецидивного отиту). У зв'язку з цим Л. Н. Хахаліним було
запропоновано виділяти клінічні "маски" ІДЗ (табл. 28).
Таблиця 28.
Клінічні "маски"ІДЗ
| Прояви ІДЗ (рецидивні або хронічні інфекційні ураження) | Середні показники у відсотках |
| ЛОР-органів | 65.5 |
| бронхолегеневої системи | 40.1 |
| шкіри | 28.4 |
| кон'юнктиви ока | 27.5 |
| сечостатевого тракту | 21.6 |
| слизової оболонки порожнини роту | 13.8 |
| шлунково-кишкового тракту | 11.2 |
| лімфатичних вузлів | 3.8 |
| кісток і суглобів | 1.7 |
| Сепсис | 8.6 |
Дата добавления: 2016-08-07; просмотров: 600;
