Внутренняя энергия газа
Внутренней энергией газа называется сумма потенциальной и кинетической энергии всех его молекул:
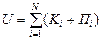 .
.
Для большинства газов при условиях, близких к нормальным, потенциальной энергией взаимодействия молекул можно пренебречь. Пусть <e> – средняя кинетическая энергия молекулы газа. Тогда
U = N<e>,
где N – число молекул.
Если газ одноатомный, то
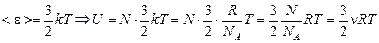 .
.
Таким образом,
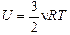 . (19.1)
. (19.1)
Поскольку согласно уравнению Менделеева–Клайперона pV = =nRT, то справедливо также
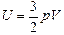 . (19.2)
. (19.2)
Если газ двухатомный, то необходимо учитывать кинетическую энергию вращательного движения молекул, поэтому
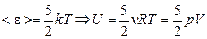 . (19.3)
. (19.3)
Задача 19.1. Найти изменение внутренней энергии 1 г Не и 1 г О2 при нагревании их на 1 К.
| т = 1 г Не: m1 = 4 г/моль О2: m2 = 32 г/моль DТ = 1 К | Решение. Заметим, что гелий (Не) – одноатомный газ, а кислород (О2) – двухатомный. Тогда
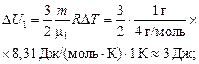
|
| DU1 = ? DU2 = ? | |
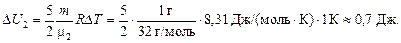
Ответ: DU1 » 3 Дж; DU2 » 0,7 Дж.
Получилось, что 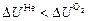 . Это так, потому что в 1 г молекул Не больше, чем 1 г молекул О2.
. Это так, потому что в 1 г молекул Не больше, чем 1 г молекул О2.
СТОП! Решите самостоятельно: А1, А2, А4–А6.
Задача 19.2. В комнате объема V = 100 м3 при атмосферном давлении р = 100 кПа находится воздух. Считая все молекулы воздуха двухатомными, найти внутреннюю энергию воздуха.
| V = 100 м3 р = 100 кПа | Решение. Согласно формуле (19.3)
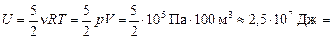 = 25 МДж.
= 25 МДж.
|
| U = ? | |
Ответ: U = 25 МДж.
СТОП! Решите самостоятельно: В3–В6.
Задача 19.3. Воздух в комнате объема V = 100 м3 находится при температуре Т = 300 К и давлении р = 1,0×105 Па. На сколько повысится внутренняя энергия воздуха при повышении температуры на DТ = 1 К? (Все молекулы считать двухатомными.)
| V = 100 м3 Т = 300 К р = 1,0×105 Па DТ = 1 К | Решение. Согласно формуле (19.3)
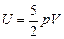 .
Так как р = const и V = const, то и U = const. Значит, DU = 0.
Ответ: DU = 0. .
Так как р = const и V = const, то и U = const. Значит, DU = 0.
Ответ: DU = 0.
|
| DU = ? | |
Дело в том, что повысилась средняя кинетическая энергия молекул, но при этом часть молекул покинула комнату из-за расширения воздуха при нагревании.
Задача 19.4. В первом сосуде находятся N1 = 1,00×1020 молекул водорода при Т1 = 300 К, во втором сосуде N2 = 2,00×1020 молекул кислорода при Т 2 = 400 К. Сосуды соединили. Найти температуру и внутреннюю энергию смеси.
| N1 = 1,00×1020 N2 = 2,00×1020 Т1 = 300 К Т 2 = 400 К | Решение. С одной стороны:
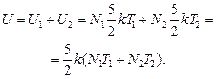 С другой стороны:
С другой стороны:
|
| Т = ? U = ? | |
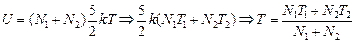 .
.
Подставим численные значения:
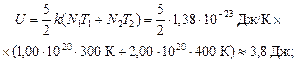
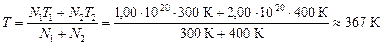 .
.
Ответ: U » 3,8 Дж; Т » 367 К.
СТОП! Решите самостоятельно: С3, D2.
Задача 19.5. В горизонтальном цилиндре под поршнем находится одноатомный газ при атмосферном давлении р0. Объем газа V0. Поршень, площадь которого S, прикреплен ко дну цилиндра пружиной жесткости k, которая в начальный момент не растянута (рис. 19.1). Какое количество теплоты надо медленно подвести к газу, чтобы поршень сместился вправо на расстояние h?
| V0 р0 k h S | Решение. Воспользуемся первым началом термодинамики: Q = A + DU. (1) Найдем А. Сила, с которой газ давит на поршень, должна равняться сумме сил давления атмосферы и упругости пружины: | 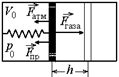 Рис. 19.1
Рис. 19.1
|
| Q = ? | ||
Fгаза = Fатм + Fпр.
Тогда работа газа по модулю будет равна сумме абсолютных значений работ атмосферного воздуха и пружины:
|Aгаза| = |Aпр| + |Аатм.воз|,
где 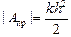 , |Аатм.воз| = р0Sh. Отсюда
, |Аатм.воз| = р0Sh. Отсюда
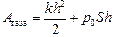 . (2)
. (2)
Найдем DU = U1 – U0. Воспользуемся формулой для внутренней энергии одноатомного газа: 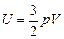 , тогда
, тогда
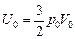 ,
, 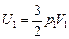 ,
,
где 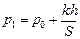 , V1 = V0 + Sh. Отсюда
, V1 = V0 + Sh. Отсюда
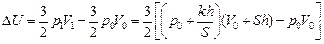 . (3)
. (3)
Подставляя (2) и (3) в (1), получим ответ:
Q = A + DU = 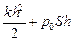 +
+ 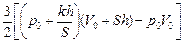 .
.
СТОП! Решите самостоятельно: С4, С7, D4.
Дата добавления: 2016-04-11; просмотров: 1297;
