Уравнение Менделеева–Клайперона
Из уравнения Клайперона (4.1) следует, что для n молей любого газа выполняется соотношение
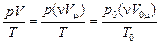 =
= 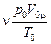 , (1)
, (1)
где Vm – молярный объем газа при температуре Т и давлении р, а V0m – молярный объем газа при температуре Т0 = 273 К и давлении р0 = 1,013×105 Па. Согласно закону Авогадро V0m = 22,4×10–3 м3/моль.
Выражение 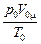 – постоянная величина, не зависящая от параметров (температуры, давления, массы, объема) данного газа. Обозначим его буквой R и получим численное значение в СИ:
– постоянная величина, не зависящая от параметров (температуры, давления, массы, объема) данного газа. Обозначим его буквой R и получим численное значение в СИ:
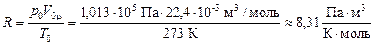 .
.
Учитывая, что Па = Н/м2 и Н×м = Дж, получим:
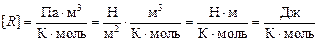 .
.
Итак: R = 8,31 Дж/(К×моль).
Подставляя значение R в (1), получим
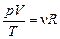 . (5.5)
. (5.5)
Учитывая, что согласно (5.2) 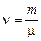 , можем записать
, можем записать
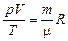 или
или 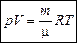 . (5.6)
. (5.6)
Формула (5.6) – это и есть закон Менделеева–Клайперона. Она устанавливает связь между параметрами р, V, т, m и Т одного и того же состояния газа.
Задача 5.1. В сосуде объемом V = 1,0 л содержится т = 22 г СО2 при температуре Т = 300 К. Найти давление в сосуде.
| V = 1,0 л = 1,0×10–3 м3 т = 22 г = 0,022 кг Т = 300 К | Решение. Согласно формуле (5.6)
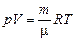 .
Отсюда .
Отсюда 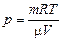 . .
|
| р = ? | |
Проверим размерность:


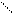



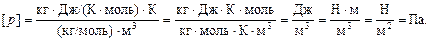
Для СО2 m = 0,044 кг/моль. Тогда
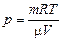 =
= 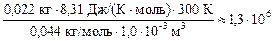 Па.
Па.
Ответ: 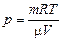 » 1,3×106 Па.
» 1,3×106 Па.
СТОП! Решите самостоятельно: А1–А3, В1, В3.
Задача 5.2. В комнате объемом V = 50 м3 находится воздух при давлении р = 1,0×105 Па и температуре Т = 300 К. На сколько изменится масса воздуха в комнате, если при неизменном давлении температура понизится на DТ = 1 К? Молярную массу воздуха считать равной m = 0,029 кг/моль.
| V = 50 м3 р = 1,0×105 Па Т = 300 К DТ = 1 К m = 0,029 кг/моль | Решение. Запишем уравнение Менделеева–Клайперона для каждого состояния воздуха:
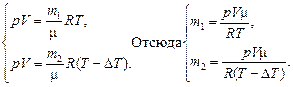
|
| Dт = ? | |
Тогда
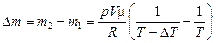 .
.
Подставим численные значения:
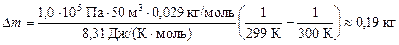 .
.
Ответ: 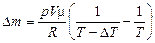 » 0,19 кг.
» 0,19 кг.
СТОП! Решите самостоятельно: В10 – В12.
Задача 5.3. Найти плотность воздуха при нормальных условиях (Т = 273 К, р = 1,0×105 Па). Молярную массу воздуха считать равной m = 0,029 кг/моль.
| р = 1,0×105 Па Т = 273 К m = 0,029 кг/моль | Решение. Согласно формуле (5.6) 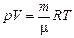 , тогда , тогда 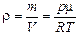 . Подставим численные значения: . Подставим численные значения:
|
| r = ? |
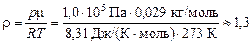 кг/м3.
кг/м3.
Ответ: 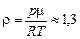 кг/м3.
кг/м3.
СТОП! Решите самостоятельно: А11, А13, В16.
Дата добавления: 2016-04-11; просмотров: 1687;
