Металлоорганические комплексы, правило Сиджвика.
Металлорганические комплексы, наряду с химическими связями комплексообразователя с классическими донорными атомами N, P, S, O…, характеризуются наличием связи с атомом углерода.
Английский химик Н.-В. Сиджвик сформулировал эмпирическое правило, согласно которому «устойчивые металлоорганические комплексы характеризуются наличием 18 электронной валентной оболочки». Например, в комплексе железа с карбонильными лигандами атом Fe (3d64s2) имеет 8-ми электронную валентную оболочку и поскольку каждая молекула СО является донором электронной пары, то образование устойчивой 18-ти электронной структуры карбонил железа происходит при наличии 5-ти СО лигандов – [Fe(CO)5]. Аналогично, карбонил никеля – в этом случае Ni (3d84s2) имеет 10-ти электронную валентную оболочку и для образования устойчивой 18-ти электронной структуры карбонил никеля должен содержать 4 лиганда – [Ni(CO)4]. Для соединения Co (3d74s2) с окисью углерода 18-ти электронная структура образуется либо для [Co(CO)4]- аниона, либо для биядерного [(CO)4Co-Co(CO)4] комплекса с металл-металл связью. Правило Сиджвика применимо не только к комплексам с СО лигандами, но и смешанно-лигандным комплексам – в соответствии с 18-ти электронной структурой комплекс Fe, содержащий две 2-х электронных молекул СО, 2-х электронный этиленовый С2Н4 и 5-ти электронный циклопентадиенильный С5Н5 лиганды, соответствует катиону [Fe(CO)2C2H4(p-C5H5)]+.
Органические лиганды комплексов, подразделяют в зависимости от числа электронов, участвующих в образовании химической связи с металлом:
1. Одноэлектронные алкильные и арильные c образованием s связи М-С: [Co(CN)CH3]2-, [Ptbpy2(Ph)2].
2. Двухэлектронные олефиновые p-комплексы: [PtCl3(C2H4)]-.
3. Трехэлектронные алильные комплексы с s связью М-С и p-связью М-лиганд: [Ni(C3H5)2].
4. Четырехэлектронные ацетиленовые комплексы с двумя p-связями: [Pt(PPh3)2(h-C2Ph2)].
5. Пятиэлектронные металлоцены - [Fe(C5H5)2]:
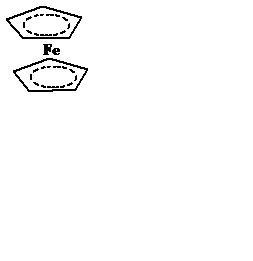
6. Шестиэлектронные ареновые – [Cr(C6H6)2]:
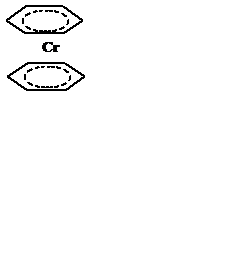
7. Семиэлектронные p-циклогептатриенильные – [V(C7H7)2]+:
Дата добавления: 2016-01-03; просмотров: 3598;
