Теплота и термодинамические функции
В соответствии с уравнением для баланса энергии (1 - 1) при постоянном объеме (механическая работа не совершается) в простой системе теплота равна изменению внутренней энергии
dQv = dU = СvdT (1 - 11)
или
 . (1 - 12)
. (1 - 12)
Для расчета теплоты при постоянном давлении вводится новая термодинамическая функция энтальпияH:
H º U + PV. (1 - 13)
(Заметим, что первоначально буква Н читалась как «эта» (греч.), а затем она стала читаться как буква латинского алфавита).
Энтальпия обладает такими же основными свойствами термодинамической функции, какими обладает и внутренняя энергия, а именно:
* ее изменение не зависит от процесса, а определяется начальным и конечным состоянием системы;
* функция Н подобно внутренней энергии обладает свойством аддитивности.
Приращение энтальпии выражается соотношением
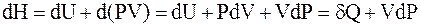 . (1 - 14)
. (1 - 14)
Сумма dU + PdV соответствует теплоте, которая в простой системе равна сумме изменения внутренней энергии и механической работы. Следовательно, при постоянном давлении
dH = dQp ; (1 - 15)
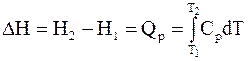 . (1 - 16)
. (1 - 16)
Дата добавления: 2015-07-24; просмотров: 725;
