Метод Кенигса - Кнорра.
Вскоре после открытия реакции Кенигса - Кнорра появились первые сообщения о синтезе дисахаридов с помощью этого метода. За прошедшие с тех пор 60 с лишним лет было опубликовано несколько сотен работ, посвященных синтезу этим методом олигосахаридов, главным образом дисахаридов, значительно реже - трисахаридов и лишь нескольких тетрасахаридов.
Все известные модификации метода Кенигса - Кнорра были использованы для синтеза олигосахаридов, причем некоторые из них были применены главным образом именно в этой области. Закономерности влияния структуры гликозилируемого производного на выходы олигосахаридов неясны, поскольку систематические исследования не проводились, а многочисленные синтезы выполнены в весьма различных условиях, что практически
исключает возможность сопоставления экспериментальных данных. Тем не менее некоторые обобщения могут быть сделаны.
Наиболее легко реакция Кенигса — Кнорра протекает в тех случаях, когда гликозилированию подвергается первичная гидроксильная группа сахара. Поэтому в настоящее время уже осуществлены синтезы большинства известных дисахаридов, содержащих 1,2-транс-гликозидные связи моносахаридно-го остатка с первичным гидроксилом, а также синтезы некоторых более сложных олигосахаридов со связями такого типа. В большинстве этих синтезов был использован классическийвариант реакции Кенигса - Кнорра. В среднем олигосахариды указанного типа получаются с выходами 40-60%, в отдельных случаях — до 80%. Таким путем были, например, синтезированы производные генциобиозы II [24], ((3,В-глюкопиранозил-(1→4)-(β,D-глюкопиранозил-(1→6)-D-галактозы III [25], 6,6'-ди-О-(β,D-глюкопиранозил)-ламинарибиозы (Положение заместителей в восстанавливающих дисахаридах, имеющих тривиальные названия, обозначаются цифрами без индексов в восстанавливающем звене и цифрами со штрихом в концевом моносахаридном остатке) IV [26] и многие другие соединения.

Как и в других случаях применения классического варианта реакции
Кенигса - Кнорра, конденсация нередко протекает с осложнениями, а выхо
ды получаемых соединений подвержены значительным колебаниям. Так, два
различных производных 4-О-(α-D-глюкопиранозил)-6-О-(β-D-глюкопиранозил) – D - глюкопиранозы, синтезируемые гликозилированием
2,3,2',3'-тетра-О-ацетил-4',6'-О-бензилиден-β-бензилмальтозида [27] и 1,2,3,2',3',4',6'-гепта-О-ацетил-β-мальтозы [28] 2,3,4,6-тетра-О-ацетил-α-D-глюкопиранозилбромидом в сходных условиях, были получены с выходами 79 и 8% соответственно.
Модификацию Бредерека использовали почти исключительно для синтеза дисахаридов с гликозидными связями, включающими первичный гидроксил. Во всех изученных примерах реакция протекала с высокими выходами и стереоспецифично. Применение этой модификации особенно удобно в тех случаях, когда синтез соответствующего частично защищенного производного сахара осуществляется через тритиловые эфиры, поскольку при этом исключается стадия детритилирования.
Гликозилирование вторичных гидроксилов сахара обычно сопряжено с значительно большими трудностями. В этом случае в условиях классического варианта реакции Кенигса - Кнорра выходы обычно низки и редко превышают 20%. Примером может служить следующий синтез [29]:
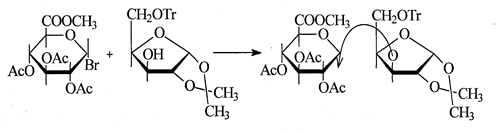
С наибольшими трудностями таким путем получают производные три-сахаридов и других более сложных олигосахаридов. Так, при конденсации ацетобромгенциобиозы с тетраацетатом глюкозы, содержащим экваториальный гидроксил, в наиболее совершенном варианте классической модификации реакции Кенигса - Кнорра выход производного трисахарида составил всего 2,2% [30]:
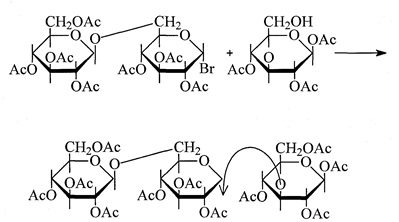
В отдельных случаях различия в реакционной способности вторичных гидроксилов сахара настолько велики, что удается осуществить даже избирательное гликозилирование. Таким способом, например, осуществлен синтез производного софорозы [22]:
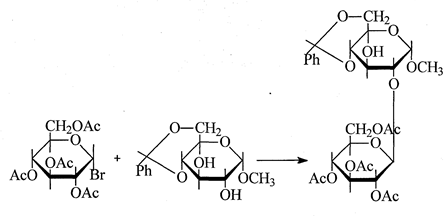
Иногда причины осложнений, возникающих при гликозилировании вторичных гидроксилов сахара, связаны с миграцией защищающих групп. Так, например, при гликозилировании 1,2;5,6-ди-О-изопропилиден-α-D-глюкофуранозы 2,3,4,6-тетра-О-ацетил-α-D-глюкопиранозилбромидом в условиях классического варианта реакции Кенигса - Кнорра была получена сложная смесь веществ [31], из которой ламинарибиоза была выделена с выходом 9,5%, а конденсация тех же соединений по варианту Земплена привела к смеси аномерных дисахаридов с 1→3- и 1→6-связями [32].
Гораздо более успешным для гликозилирования вторичных гидрок-. силов Сахаров оказалось применение модификации Гельфериха, что позволило получить некоторые дисахариды с выходами до 50% и более. Таким путем был осуществлен синтез производного гиалобиоуроновой кислоты [33]:
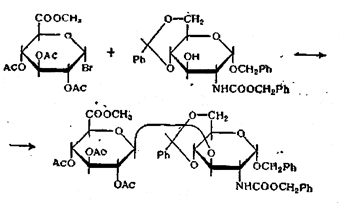
Аналогичным образом был осуществлен синтез производного 3-O-α-D-галактопиранозил)-N-ацетил-D-глюкозамина [34]:
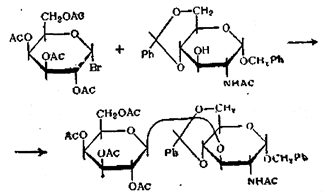
Однако отсутствие стереоспецифичности реакции в варианте Гельфериха сильно ограничивает возможности его применения.
Долгое время значительные трудности вызывал синтез невосстанавливающих дисахаридов, поскольку все попытки получения этих соединений по классическому варианту реакции Кенигса - Кнорра неизменно приводили к весьма низким выходам. Причина осложнений кроется, очевидно, в окислении восстанавливающего производного гликозилируемого сахара окисью или карбонатом серебра, применяемыми в этом варианте для связывания галоидоводорода. Использование для этой цели варианта Гельфериха позволило резко повысить выходы невосстанавливающих дисахаридов (до 30 - 45%). Так, октаацетат β,β-трегалозы был получен таким путем с выходом 31,5%:
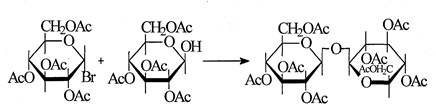
Однако и в этих случаях отсутствие стереоспецифичности реакции дает неожиданные результаты, не позволяющие применять эту модификацию для стереонаправленного синтеза. Так, синтез Б-галактопиранозил-В-глюкопиранозида по методике, аналогичной синтезу β,β-трегалозы, приводит уже не к 1,2-транс-, а к 1,2-цис-изомеру [35].
Дата добавления: 2015-04-05; просмотров: 2365;
