Бадмаев Б.Ц. 8 страница
6. Тромбоцитарный актомиозиноподобный белок ретрактозим обеспечивает консолидацию тромбоцитарно-фибринового сгустка и гемостаз.
7. Избыток образования фибрина ограничивается механизмом фиб- ринолиза, который протекает внутри самого сгустка, так как именно там создаются благоприятные условия для контакта плазминогена с его активатором при отсутствии его ингибиторов.
При этом, конечно, следует иметь в виду постоянное действие антикоагулянтов. И антитромбин, и протеины С и S, так же как и ингибитор пути тканевого фактора, работают постоянно и регулируют образование необходимого для организма количества фибрина (см. рис. 20.1).
Нарушения, возникающие при недостаточном образовании фибрина или при неполноценности функционирования тромбоцитарного звена гемостаза, так же как и при избыточной активности плазмина или неполноценности функционирования компонентов сосудистой стенки, приводят к нарушению процесса гемостаза в целом. Это и является основными механизмами развития феномена кровоточивости. Напротив, избыточное формирование фибрина вследствие неполноценности антикоагулянтов или слабости фибринолитического звена наряду с дефектами сосудистой стенки становится причиной избыточного внутрисосудистого свертывания крови, которое может приводить к нарушению проходимости сосудов или полной их окклюзии тромботическими массами — развитию феномена тромбоза с соответствующими последствиями. Иногда наблюдаются сочетания тромботических и геморрагических проявлений.
Таким образом, при нарушении функционирования системы гемокоагуляции различаются следующие синдромы: геморрагический, тром- ботический и тромбогеморрагический, синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром).
20.2. Геморрагические синдромы
Геморрагический синдром — патологическое состояние, характеризующееся избыточной кровоточивостью.
Патогенетическая классификация геморрагий.
1. Дефект тромбоцитарного звена:
• количественный — тромбоцитопении;
• качественный — тромбоцитопатии;
• смешанный.
2. Дефект прокоагулянтного звена — дефект фибринообразования:
• количественный дефект факторов свертывания крови (недостаток факторов I, II, V, VII, VIII, IX, X, XI);
• дефект структуры молекулы факторов свертывания крови;
• наличие ингибиторов факторов свертывания.
3. Избыточная активность фибринолиза:
• экзогенного происхождения;
• эндогенного происхождения.
4. Дефект сосудистой стенки.
5. Комбинированный дефект компонентов гемостаза.
Геморрагические состояния, обусловленные дефектом тромбоцитарного звена. В норме количество тромбоцитов должно быть в пределах 2,0—4,0x1012/л.
Считают, что для обеспечения полноценного гемостаза достаточно количества тромбоцитов в пределах 30 ООО в 1 мм3. Некоторые авторы полагают, что даже меньшее количество полноценных тромбоцитов (15 ООО и даже 10 ООО в 1 мм3) способно обеспечить полноценный гемостаз. Геморрагическая тромбоцитопения была одной из первых идентифицированных геморрагических заболеваний человека. Ее описал Верльгоф еще в XVIII в. задолго дс того, как были обнаружены сами тромбоциты. В настоящее время различают несколько типов тромбоцитопе- ний (табл. 20.4).
Таблица 20.4
Классификация тромбоцитопений
|
| Тромбоцитопения | |||
| вследствие нарушения образования | вследствие повышенного разрушения | вследствие перераспределения | вследствие коминации причин |
| отслоение плаценты, эмболия околоплодными водами, внутриутробная гибель плода, токсикоз беременных и пр | |||
| Неэффективный тромбоцитопоэз | Тромбоцитопении при отдельных заболеваниях: болезнь Виллебранда | Гипотермия | Лимфопроли- феративные заболевания |
| а) Наследуемые: аутосомальная доминантная, аномалия Мая— Хегглина, синдром Вискотта— Олдриджа и др. б) Дефицит витамина В12, фолиевой кислоты и др. в) Прочие; паро- ксизмальная ночная гемоглобин- урия, синдром ди Гульельмо и пр. | Смешанные механизмы | Прочие |
Тромбоцитопатии — тромбоцитарные дисфункции. Нарушение в тромбоцитарном звене могут приводить к кровоточивости не только при количественном недостатке тромбоцитов, но и при их неполноценности. Неполноценность тромбоцитарного звена характеризуется неспособностью тромбоцитов осуществлять феномены адгезии, агрегации, высвобождения внутреннего содержимого, содержащегося в гранулах, влиять на взаимодействие факторов коагуляции на фосфолипидной поверхности, и неполноценностью феномена ретракции. Эти нарушения тромбоцитарного звена получили название тромбоцитопатии. Первая тромбоци- топатия была описана Эдвардом Гланцманом еще в 1920 г., и ее называли болезнью Гланцмана. Известно довольно большое количество тромбоцитопатии. Существует несколько подходов к их классифицированию. Например, предлагается характеризовать нарушения отдельных тромбо- цитарных функций.
Тромбоцитарные дисфункции включают следующие формы расстройства:
Нарушения адгезии:
• дефект гликопротеида 1Ь — болезнь Бернара-Сулье (в сочетании с умеренной тромбоцитопенией и гигантскими тромбоцитами);
• псевдоболезнь фон Виллебранда (отсутствие реакции на не- мультимерные белки Виллебранда) и др.;
Нарушения агрегации:
• болезнь Гланцмана — нарушение агрегации с АДФ и коллагеном вследствие дефекта комплекса гликопротеинов lib—Ша;
• дефект агрегации в ответ на коллаген (нарушение гликопротеида la);
• дефект аггрегации в ответ на тромбин, дефект агрегации вследствие нарушений коллагена (тип IV, III —синдромы Эй- лерса—Данлоса, Марфана, несовершенного остеогенеза).
Нарушения прокоагулянтной активности тромбоцитов:
• первичный прокоагулянтный дефект тромбоцитарной мембраны в связывании фактора V при нормальной агрегации, секреции и нормальном времени кровотечения;
Нарушения реакции высвобождения:
• дефект плотных телец (нарушение высвобождения адеииннук- леотидов или серотонина, или кислых гидролаз, или арахидоновой кислоты под действием АДФ, коллагена и адреналина);
• синдром серыхтромбоцитов — (отсутствие а-гранул, содержащих фибриноген, фактор Виллебранда, тромбоспондин и др.)
Нарушения ретракции:
• тромбастения Гланцмана;
Сочетанные нарушения функций:
• синдром Херманского—Пудлака — дефект высвобождения из плотных телец и из а-гранул в сочетании с окулокутанным альбинизмом и наличием пигментных .макрофагов в костном мозге;
• синдром Вискотта—Олдриджа — тромбоцитопения, тромбоци- топатия (дефект высвобождения из плотных тел, дефект агрегации на адреналин) в сочетании с экземой и иммунодефицитом;
• аномалия Мэя—Хегглина — гигантские тромбоциты, тромбоцитопения, аномальные гранулоциты с крупными включениями;
• синдром Чедиака—Хигаши — тромбоцитопатия (дефект плотных телец) в сочетании с тромбоцитопенией и дефектом пигментации (волосы, кожа, сетчатка);
• TAR-синдром — тромбоцитопения при отсутствии радиальной кости и тромбоцитопатией (дефект высвобождения из плотных телец).
Кроме перечисленных наследуемых заболеваний, кровоточивость нередко вызывается механизмами, связанными с приобретенными дефектами функций тромбоцитов, которые чаще всего наблюдаются при приеме лекарств (ацетилсалициловая кислота и др.), уремии, операциях с применением аппарата «сердце—легкие» и др.
Следует отметить, что изолированные дефекты тромбоцитарного звена независимо от патогенетического механизма клинически проявляются сходно. Для них характерны «синяки», петехии, экхимозы, кровотечения при повреждениях кожи и слизистых оболочек, маточные, носовые и кишечные кровотечения.
Геморрагии при нарушениях образования фибрина. Дефект прокоагулянтного звена. Дефект каждого из факторов прокоагулянтного ззена может возникать вследствие недостаточной их продукции, но также при образовании антител к факторам свертывания, а иногда вследствие формирования дефектной молекулярной структуры.
Описаны геморрагические состояния при недостаточности следующих факторов свертывания крови: 1, II, V, VII, VIII, IX, X, XI, XIII. Механизм геморрагических состояний при дефекте фактора XII, прекалликреина, ки- ниногена высокой молекулярной массы, Са2+ и тканевого фактора точно не известен. В тех же случаях, когда кровоточивость предполагается именно их недостаточностью, она настолько незначительна, что не требует коррекции. Наиболее часто приходится встречаться с геморрагическими явлениями вследствие дефицита фактора VIII, который бывает у одного из 4000—20 ООО человек. В 5—10 раз реже отмечается другая патология, обусловленная дефектом фактора IX, — гемофилия. Гемофилия А развивается при дефекте фактора VIII, гемофилия В — при дефекте фактора IX. Проявления гемофилии характеризуются кровоточивостью в суставы, образованием гематом в мышцах, кровоизлияними в полость черепа. Возможны случаи кровотечений при укусах языка, повреждении его уздечки.
При гемофилиях крайне редко возникают петехиальные кровотечения, кожная пурпура, кровотечения из слизистых оболочек, нередки гематурии. Геморрагические диатезы вследствие дефицита факторов II, V, VII, X и XI встречаются значительно реже. Проявления этих расстройств сходны с таковыми у больных с дефицитами факторов VIII и IX, хотя их интенсивность выражена значительно слабее. В связи с этим высказывается предложение называть любое из дефектов фибринообразования гемофилией, что не лишено смысла.
Геморрагический синдром при избыточной фибринолитичес- кой активности. Часто причиной этих расстройств является усиление фибринолиза, вызванное экзогенными факторами, нередко при проведении тромболитической терапии. Описаны случаи гиперфибринолити- ческих кровотечений, обусловленных недостаточным контролем за активным плазмином со стороны а2-антиплазмина. Последний может быть как сниженным, так и неполноценным. Гиперфибринолиз часто отмечается в комбинации с избыточным свертыванием крови. Проявления гиперфиб- ринолиза идентичны таковым при дефектах формирования фибрина.
Геморрагические состояния вследствие дефекта сосудистой стенки. Причиной геморрагического синдрома может быть неполноценность сосудистой стенки, определяющая ее неспособность осуществлять эффективный гемостаз без нарушений ее целости. Этот механизм обусловливает развитие патологии, относящейся к геморрагическим телеан- гиэктазиям; она проявляется формированием неполноценных сосудов, стенка которых в отдельных местах состоит лишь из одних эндотелиальных клеток, лишенных мышечного слоя и даже эластической мембраны. Эти участки значительно чаще подвержены разрывам, чем нормальные сосуды, и сопровождаются кровотечениями.
Аномалия коллагена рассматривается в качестве основного механизма, определяющего неполноценность сосудистой стенки и гемостаза при генерализованной фибродисплазии эластических волокон, при дегенеративных повреждениях соединительной ткани, сочетающейся с гипоплазией эластических волокон и аномалией сосудов. Хорошо известны сосудистые геморрагии при дефиците витамина С. Приобретенные дефекты сосудистой стенки проявляются геморрагиями при аутоиммунных заболеваниях— анафилактоидной пурпуре (болезнь Шенлейна—Геноха), васку- литах, а также при изменении сосудистой стенки вследствие отложения в ней аномальных белков (миеломная болезнь, макроглобулинемия и пр.).
Геморрагические синдромы, вызываемые сочетанием нескольких дефектов гемокоагуляции. Наиболее часто такие геморрагии наблюдаются при тромбогеморрагическом синдроме, называемом также синдромом диссеминированного внутрисосудистого свертывания крови (ДВС-синдром) или же коагулопатией потребления. При этом у пациентов отмечается резкое снижение в плазме как факторов свертывания крови, так и уровня тромбоцитов. Одновременно у многих из них имеет место выраженный гиперфибринолиз. К этой же группе необходимо относить наиболее часто встречающуюся геморрагию — болезнь Виллебранда. В основе ее лежит дефицит специфического протеина, называемого белком Виллебранда, который действует двояко: с одной стороны, он обеспечивает контакт тромбоцитов с субэндотелиальными структурами за счет взаимодействия с тромбоцитарным гликопротеидом lb и субэндотелием, а с другой стороны, белок Виллебранда обеспечивает стабильность антигемофилического фактора VIII. Кровоточивость при этом заболевании имеет сходство с кровоточивостью при дефекте образования фибрина, а также с кровоточивостью, характерной для дефектов тром- боцитарного звена.
20-3. Патология, обусловленная гиперкоагуляцией: тромботический синдром
Тромботический синдром, или синдромы, — патологические состояния, характеризующиеся внутрисосудистым или внутрисердечным формированием кровяных сгустков — тромбов, образующихся за счет фибрина, тромбоцитов и оседающих в их структурах тех или иных количеств эритроцитов и лейкоцитов, связанных со стенкой сосудов и в той или иной степени обтурирующих их просвет. Какова причина тромбозов? Еще в середине прошлого века Рудольф Вирхов определил свою знаменитую «тромботическую триаду», согласно которой причинами тромбозов могут быть следующие факторы: нарушение целости сосудистой стенки, замедление кровотока и повышенная способность крови к свертыванию. К настоящему времени известно большое число факторов, с помощью которых стенка сосуда способна влиять на внутрисосудистые тромбооб- разования: на степень спазмирования — через эндотелиальный фактор релаксации — оксид азота, эндотелин-1, ангиотензинпревращающий фактор, за счет влияния на тромбоциты — через синтезируемый эндотелием фактор Виллебранда, фактор, активирующий тромбоциты, проста- циклин, влияющий на функцию тромбоцитов белок теплового шока, Р- селектин и др. На поверхности эндотелия происходит активация факторов V, VIII, X, возникающая вследствие секреции эндотелиальными клетками ингибитора тканевого фактора и продукции протеина S, синтеза тканевого активатора плазминогена и урокиназы, а также ингибиторов активаторов плазминогена РАМ, PAI-2.
Степень обтурации просвета сосуда определяет тяжесть расстройств. Полная обтурация артериального сосуда вызывает ишемию той части органа, кровоснабжение которой она определяет. При быстрой обтурации обычно развивается инфаркт, т.е. омертвение той или иной части органа, которая была полностью лишена доступа крови. При медленной обтурации сосуда возможно развитие коллатерального кровообращения, которое в какой-то степени может ограничить размеры и степень ишемии тканей органа. При развитии тромбов в венах последствия менее драматичны, так как венозная система обычно имеет множество параллельных путей венозного кровотока. Однако тяжесть также определяется размерами окклюзированного венозного сосуда. Чем больше эти размеры, тем труднее развиться коллатеральному кровотоку, адекватному объему крови, оттекающей от региона, принадлежащего ктромбируемой вене.
Венозный тромб определяет не только замедление кровотока, но и степень сдавления окружающих тканей застойной кровью, в т.ч. и артерий, находящихся в зоне поражения. Для венозных тромбов в большей степени, чем для артериальных, характерна способность его частиц отрываться от основной массы тромба, превращаться в эмболы и разноситься током крови в сторону сердца и далее — от него. Но и артериальные, и внутрисердечные тромбы способны вызвать эмболию, которая может определять характер расстройств зависимый от места и объема сосуда.
Известно, что основной причиной артериальных тромбов является атеросклероз сосудов. Нарушение целостности атеросклеротических бляшек является наиболее драматическим процессом их эволюции, который недавно получил название атеротромбоза. При их разрыве высвобождающийся тканевый фактор включает каскад фибринообразования, который наряду с активизацией тромбоцитарного компонента приводит к образованию тромба на месте повреждения. Имеется предположение, что в основе формирования атеросклеротических бляшек большая роль также принадлежит внутрисосудистому свертыванию крови.
Установлено, что при сердечной недостаточности и замедлении кровотока при уменьшении активности мышц, особенно икроножных, частота венозных тромбозов резко увеличивается. И наоборот — ускорение венозного кровотока при стимуляции мышц, в т.ч. искусственной, повышении тонуса венозных сосудов и при уменьшении степени сердечной недостаточности частота венозных тромбозов уменьшается.
Большая роль в формировании тромбов, больше венозных, но также и артериальных, отводится врожденной предрасположенности к их формированию — наличиютакназываемойтромбофилии. Начало учению о тромбофилиях было положено лишь в 1965 году, когда норвежскому ученому О. Эгебергу удалось доказать, что в одной из норвежских семей частые тромбозы связаны с выраженным снижением в их организме антитромбина III, естественного противотромботического фактора человека. Дальнейшие исследования привели к тому, что на сегодня имеется целый перечень состояний, при которых образование тромбов сопровождается дефектом тех или иных противотромботических приспособлений организма.
Тромбофилические состояния включают следующие нарушения:
• дефект антитромбина III:
— количественный;
— качественный, смешанный;
• дефект протеина С;
• дефект протеина S;
• резистентность к активированному протеину С-дефект фактора V (Лейдена);
• дефект молекулы протромбина — протромбин 20210;
• дефект фибриногена;
• дефект кофактора гепарина II;
• дефект плазминогена;
• дефект активатора плазминогена;
• дефект фактора Хагемана;
• наследуемая гиперактивность тромбоцитов;
• гипергомоцистеинемия;
• люпус-антикоагулянт.
Все перечисленные состояния характеризуются повышенной возможностью организма к развитию внутрисосудистых тромбов, однако их наличие не является гарантией обязательного тромбообразования. По- видимому, для этого нужны какие-то добавочные компоненты — повреждение сосудистой стенки или замедление кровотока. Вероятно, что при образовании тромба всегда имеет место сочетание нескольких предрасполагающих факторов.
20.4. Синдром диссеминированного
внутрисосудистого свертывания крови (ДВС-синдром)
ДВС-синдром — патологическое состояние, которое определяется избыточным внутрисосудистым свертыванием крови и геморрагической коагулопатией потребления и проявляется нарушением функции отдельных органов.
Процессы внутрисосудистого свертывания крови являются естественным атрибутом жизнедеятельности организма. В крови каждого здорового человека, как и больных людей, постоянно имеются те или иные количества маркеров внутрисосудистого свертывания крови, таких, как фибринопептид А, отщепляющийся от молекулы фибриногена в начальной фазе формирования фибрина, растворимые комплексы фибрин-мо- номеров, D-димеры — продукты расщепления стабилизированного фибрина, 4-й фактор тромбоцитов и (3-тромбоглобулин — свидетели реакции высвобождения тромбоцитов, подтверждающие их активность. Детализации этих факторов способствовало наблюдение в 1950 г. случая гибели пациента вследствие выраженного геморрагического синдрома, который сопровождался массивным внутрисосудистым свертыванием крови. Предложены о следующей градации интенсивности внутрисосудистого свертывания крови:
I степень интенсивности — нормальная гемокоагуляция, характеризую
щаяся наличием маркеров внутрисосудистого свертывания крови в нормальных пределах;
II степень интенсивности — уровень маркеров внутрисосудистого свер
тывания повышен, но существенно не влияет на клиническую картину заболевания;
III степень интенсивности — характеризуется тем, что внутрисосудистая
гемокоагуляция вызывает нарушение функции органов, гипотензию вплоть до шока или тромбогеморрагический феномен, или же различные их сочетания.
Повышение интенсивности внутрисосудистого свертывания крови наблюдается при любом остром и хроническом заболевании, а также при определенных физиологических состояниях, в том числе при выполнении активных физических упражнений.
Выраженная активация процесса внутрисосудистого свертывания крови за счет появления в крови активных индукторов гемокоагуляции или же действия самого тканевого фактора может активировать как прокоа- гулянтное, так и тромбоцитарное звено гемостаза или же одновременно оба эти звена и приводить к образованию микротромбов, что особенно заметно в микроциркуляторном русле. В результате этого при локализации микротромбов в отдельных органах функции последних нарушаются. Одновременно происходит потребление в тромботическом сгустке факторов свертывания крови и тромбоцитов, что при сочетании с активацией фибринолитической системы крови приводит к развитию выраженной кровоточивости. Эта фаза диссеминированного внутрисосудистого свертывания крови получила название коагулопатии потребления, а также тромбогеморрагического синдрома.
В настоящее время признано, что термин ДВС целесообразно сохранить для III степени интенсивности внутрисосудистого свертывания крови и не применять при наличии двух первых стадий. Тромбогеморра- гический синдром, или коагулопатия потребления, или ДВС, наиболее часто встречается при неоплазмах (особенно при лейкемиях, гепатомах), инфекциях, коллагенозах, а также в акушерской патологии — при преждевременной отслойке плаценты, внутриутробной гибели плода и эмболии околоплодными водами. Нередко его можно наблюдать при травмах, синдроме длительного раздавливания и при ожогах. Иногда он может осложнять операционные вмешательства.
Таким образом, и тромбозы, и геморрагии и их различные сочетания, в том числе тромбогеморрагический синдром, развиваются вследствие нарушений функции системы гемокоагуляции организма.
20.5. Методы оценки нарушений системы гемокоагуляции
Основными лабораторными методами, позволяющими выявить причину кровоточивости, являются время кровотечения, подсчет количества тромбоцитов, протромбиновое время, активированное частичное тром- бопластиновое время.
Время кровотечения. Определяется путем фиксации с помощью секундомера времени от момента появления капельки крови при проколе мочки уха до полного отсутствия кровоточивости из места дефекта кожи. Наиболее распространенным является метод, предложенный Дюком. Нормальными признаются показатели от 2 до 4 мин. При удлинении времени кровотечения следует думать о патологии тромбоцитарного звена гемостаза.
Подсчет количества тромбоцитов. Может выполняться любым из применяемых информативных методов — в камере Горяева и с помощью инструментов, например тромбокаутера При удлиненном времени кровотечений этот показатель позволяет отдифференцировать тромбоцито- пении от тромбоцитопатий.
Протромбиновое время — это время от добавления к исследуемой плазме реактива тромбопластина до появления феномена образования фибрина, превращающего плазму из золя в гель и лишающего ее свойства текучести. Удлинение этого времени по сравнению с показателями, полученными при исследовании смеси плазм здоровых людей, позволяет предполагать дефицит VII, X, V, II, I факторов гемокоагуляции в качестве причины нарушения гемостаза.
Определение активированного частичного тромбопластинового времени (АЧТВ) заключается в выявлении времени образования фибри- нового сгустка в исследуемой плазме после добавления к ней стандарт - ного раствора каолина, активирующего XII фактор гемокоагуляции, и стандартного раствора кефалина, определяющего оптимальное количество фосфолипидов, необходимых для осуществления процесса свертывания крови. Удлинение этого времени по сравнению с нормой позволяет предполагать нарушения на уровне факторов I, II, V, X, IX, VIII, XI, XII. Комбинации перечисленных тестов в сочетании с использованием бариевой плазмы, лишенной белков протромбинового комплекса — II, VII, IX, X факторов, а также дефицитных плазм, каждая из которых имеет определенный дефицит конкретного фактора свертывания, позволяют точно выявить причину кровоточивости у обследуемого больного.
Для выяснения степени интенсивности внутрисосудистого свертывания крови, которая может предполагать тромбообразование, используются иммунные тесты выявления в сыворотке обследуемого продуктов деградации фибрина (ПДФ), продуктов расщепления образовавшегося фибрина — Д-димеров, показателей начинающегося фибринообразова- ния — растворимого комплекса фибрин-мономера, а также показателей активности участия тромбоцитов в тромбообразовании — (3-тромбогло- булин и 4-й фактор тромбоцитов.
Для выявления стадии коагулопатиипотребления при ДВС-синдро- ме основным диагностическим лабораторным критерием является анализ динамики снижения уровня фибриногена и тромбоцитов и ее корреляция с клиническими проявлениями.
Глава 21. Патология лимфатической системы
Сведения о содержащих бесцветную жидкость анатомических образованиях имеются в трудах Гиппократа и Аристотеля. Эти и другие свидетельства, говорящие о существовании белой крови, были забыты почти на две тысячи лет Современная история лимфологии начинается с открытия, сделанного около 400 лет назад Г Азелли, Т. Бартолином, О.Рудбе ком
В 60—70-е годы нашего столетия произошел коренной пересмотр отношения к роли лимфатической системы при патологии. Были доказаны и сформулированы следующие положения.
• Вовлечение лимфатической системы в патологический процесс является универсальным механизмом реагирования организма вне зависимости от этиологии и патогенеза заболевания.
• Нарушения структуры и функций лимфатической системы вносят патогенетический вклад на клеточном, тканевом, органном и орга- низменном уровнях в развитие и исход заболеваний.
• Устранение указанных нарушений требует специальных воздействий на структуру и функции лимфатической системы, повышает эффективность лечебных и профилактических мероприятий.
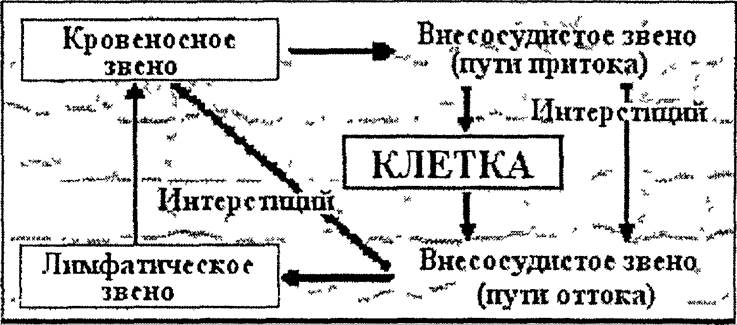 Рис 21 1 Место лимфатической системы среди звеньев
гуморального транспорта
Рис 21 1 Место лимфатической системы среди звеньев
гуморального транспорта
|
Роль лимфатической системы в патологии определяется ее положением в цепи гуморального транспорта (рис 21.1) и многообразием осуществляющих ею функций:
• обеспечение клеточного метаболизма,
• дренажная,
• барьерная,
• детоксикационная,
• иммунная,
• гемо- и лимфокоагуляционная,
• резорбционная,
• концентрационная,
• лимфопоэтическая.
21.1. Нарушение лимфообразования
*
Лимфообразование — один из ключевых этапов в цепи функционально взаимозависимых процессов гуморального транспорта организма. Лимфообразование обеспечивает дренаж межклеточного пространства—удаление выделяемых клетками продуктов жизнедеятельности, проникших микроорганизмов, накопившихся там экзо- и эндотоксинов. Термин «лимфатический дренаж» нередко используется как синоним термина «лимфообразование».
Различают общее и местное (регионарное, локальное) нарушения лимфообразования. И то, и другое проявляется в виде уменьшения или увеличения транспорта тканевой жидкости в лимфатические капилляры.
Общее уменьшение лимфообразования обычно не связано с нарушением собственно этой функции. Оно характерно для лиц пожилого и старческого возраста и возникает вследствие возрастного уменьшения числа функционирующих лимфатических сосудов и/или атеросклероза, В патологии общее уменьшение лимфообразования проявляется при обезвоживании организма, кровопотере, шоке, кахексии.
Общее увеличение лимфообразования возникает как временная реакция на введение крови, кровезаменяющих растворов или стимулирующих лимфатический дренаж препаратов.
Дата добавления: 2015-02-05; просмотров: 1037;
