Бадмаев Б.Ц. 1 страница
i
|
| Ожирение |
| Избыток Na* |
Сгресс
__ I__
Генетически обусловленные изменения
Увеличение NV - Н* ( Na* - ЬГ) прошвотока
| \ клетки |
| Увеличение тоиуса аргерий и вен,задержка Na+ в клетках Увеличение Усиление сократимости |
| ОЦК |
| миокарда |
| V |
| Увеличение СВ |
Увеличение р i
Ремоделирование peiHCTHBHbix артерий ;
Усиление тоиуса артерий, гипертрофия сосудистой С1енки
I
Ишемия почек Увеличение ОПГС
| Увеличение внутриклеючного Са+~ |

(ренин,ангио!еизнн) / * /
Гипертоническая болезнь!
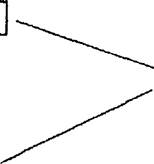
Схема 17 1 Патогенез гипертонической болезни КА — катехоламины, НУГ — натрийуретический гормон СВ — сердечный выброс, ОПСС — общее периферическое сосудистое сопротивление, ОЦК — объем циркулирующей крови
Артериальную гипертензию обычно сопровождают увеличение сердечного выброса и повышение периферической сосудистой резистентности.
Увеличение сердечного выброса объясняют влиянием нескольких механизмов:
• увеличением частоты сердечных сокращений,
• увеличением сократительной способности миокарда;
• нарушением регуляции почками объема внеклеточной жидкости в связи с расстройством транспорта натрия или усилением минера- локортикоидной активности
Увеличение первичной сосудистой резистентности связывают с дефектом симпатической регуляции (нарушение реакции а- или Р-ад- ренергических рецепторов), расстройством гуморальных влияний (высвобождение простагландинов, кининов, ангиотензина), а также нарушением тонуса артериол, связанное с действием локальных факторов.
Артериальная гипертензия может быть проявлением самостоятельного заболевания и тогда применяется термин «гипертоническая болезнь», введенный русским кардиологом Г.Ф. Лангом в 20-х годах нынешнего столетия.
Зарубежные авторы для обозначения этой патологии используют термины «эссенциальная гипертензия»или «первичная артериальная гипертензия», подчеркивая неясность вопроса об этиологии и патогенезе заболевания и целесообразность отделения гипертонической болезни от артериальной гипертензии, развивающейся при некоторых заболеваниях — вторичной АГ,
17.4.1. Патогенез гипертонической болезни
Причины и механизмы развития данного заболевания до конца не
ясны.
Определенное значение придают факторам, предрасполагающим к его развитию.
Не вызывает сомнения наличие наследственной отягощенности при ГБ. Расчетная величина генетического вклада в развитие данной болезни составляет 30—60 %. Однако его роль реализуется в результате взаимодействия с другими факторами, включая факторы окружающей среды. Наиболее признанными гипотезами возникновения ГБ являются две:
• наличие врожденного уменьшенного количества нефронов;
• нарушение транспорта ионов через клеточную мембрану. Первая гипотеза основывается на наблюдениях, установивших взаимоотношение между малой массой тела ребенка при рождении (например, недостаточное питание) и последующим повышением АД. В таких случаях можно предположить наличие уменьшенного количества нефронов, что способствует задержке натрия и прогрессирующему поражению почек с последующим повышением АД. Роль натрия в развитии ГБ доказывается следующими данными:
• у животных, генетически предрасположенных кАГ, солевая нагрузка приводит к ее возникновению;
• повышение АД прямо коррелирует с увеличенным потреблением поваренной соли в соответствующих группах населения;
• потребление соли в количестве менее 50 ммоль/сут сочетается с отсутствием или очень малой распространенностью АГ в популяции. Существует также гипотеза, основывающаяся на факте, что при повышении АД наиболее распространенным нарушением является изменение транспорта ионов через клеточную мембрану. В частности, при изучении различных функций клеточных мембран было установлено увеличение натриевого и калиевого тока из-за возможного снижения активности Ыа+-К+-АТФазы. Снижение активности Са2+-АТФазы сопровождается увеличением содержания связанного кальция. Нарушается также про- тивотранспорт натрий—водород, натрий—литий, что увеличивает рН внутри клетки. Это в свою очередь способствует развитию гипертрофии сосудистой стенки. При этом происходит задержка натрия внутри клетки, что повышает сократительные свойства гладкомышечных клеток.
На ранней стадии заболевания повышение АД чаще всего обусловлено увеличением сердечного выброса.
Увеличение сердечного выброса непосредственно связано со следующими нарушениями:
• увеличением объема циркулирующей крови;
• усилением венозного тонуса;
• увеличением притока крови к сердцу;
• усилением сократимости миокарда.
Под влиянием вазопрессорных факторов и при наличии генетических предпосылок, а также возникающих нарушений в системе ауторегу- ляции уровня АД постепенно формируются изменения в фосфолипидах клеточных мембран. В результате увеличивается содержание внутриклеточного кальция, усиливается констрикция гладкомышечных клеток, а также возрастает рН в клетках, что стимулирует развитие гипертрофических процессов в сосудистой стенке. Конечным итогом возникших нарушений является увеличение сосудистого сопротивления и повышение уровня АД.
В целом, в формировании и поддержании повышенного АД в результате неспецифического механизма —■ трофически обусловленной обратной связи принимают участие многочисленные пусковые факторы. Отсюда становится понятной трудность выявления этиологического фактора, вызывающего гипертоническую болезнь.
17.4.2. Вторичная артериальная гипертензия
1. Артериальная гипертензия, связанная с приемом оральных контрацептивных средств или приемом эстрогенов в постменопаузе, развивается вследствие увеличения объема циркулирующей крови, обусловленного активацией ренин-альдостероновой системы. Определенную роль может также играть развивающаяся при гормональной контрацепции резистентность к инсулину.
2. Артериальная гипертензия при паренхиматозных заболеваниях почек является следствием нарушения экскреции солей и воды, уменьшения почечного кровотока и усиления активности системы ренин—ан- гиотензин—альдостерон.
3. Ре нова окулярная гипертония — артериальная гипертензия, развивающаяся при поражении сосудов почек. У людей пожилого возраста чаще вызывается атеросклерозом, тромбозом почечной артерии, а у молодых (особенно женщин) — связана с фибромышечной дисплазией основного ствола или ветвей почечной артерии. В результате ишемии почки и снижения пульсового давления усиливается секреция ренина, альдостеро на, происходит задержка жидкости и возрастает сердечный выброс.
4. Причиной артериальной гипертензии эндокринного генеза могут быть:
• первичный гиперальдостеронизм;
• избыточная продукция кортизола;
• избыточная продукция катехоламинов;
• избыточное образование дезоксикортикостерона. Первичный гиперальдостеронизм чаще связан с наличием доброкачественной аденомы надпочечников или их двусторонней гиперплазии. Установлена семейная форма альдостеронизма, обусловленного мутацией генов, кодирующих синтез энзима, в частности 18-гидроокси- лированного кортизола в фасцикулярной зоне надпочечника, или вызывающих дефицит образования 11-(3-гидроксистероиддегидрогенезы в канальцах почек. В этих случаях избыток минералокортикоида способствует возникновению гипертензии и гипокалиемии.
Феохромоцитома — опухольхромаффинной ткани, которая может локализоваться в надпочечниках или симпатических ганглиях (параганг- лиома). Ее клетки продуцируют активные катехоламины, преимущественно адреналин. Выделена семейная форма феохромоцитомы, для которой характерно поражение нескольких эндокринных желез, в том числе щитовидной, а также слизистой оболочки (ганглионеврома). В этих случаях имеется мутантный ген в одном и том же локусе 10-й хромосомы.
Опухоль, продуцирующая адреналин, чаще локализуется в надпочечниках и вызывает преимущественно систолическую гипертензию. Опухоли другой локализации чаще продуцируют норадреналин и инициируют систоло-диастолическую гипертонию.
5. При коарктации аорты повышенное АД регистрируется только на руках, что связано с наличием механического препятствия. Наряду с этим при коарктации аорты наблюдается усиление активности симпатико-ад- реналовой и ренин-ангиотензиновой систем.
6- Артериальная гипертензия после операции на сердце имеет преходящий характер и обусловлена многими факторами: болью, стрессом, гипоксией, гиперкапнией, избыточной трансфузией жидкости, отменой (3-адреноблокаторов. Резкое повышение АД регистрируют после:
а) аорто-коронарного шунтирования;
б) имплантации аортальных клапанов;
в) устранения дефекта межпредсердной перегородки;
г) трансплантации сердца.
7. Различают две формы артериальной гипертензии беременных: впервые возникшая и хронически существующая. Первая возникает чаще при первой беременности, при последующей беременности от другого отца или в поздние сроки беременности. Эта форма АГ сопровождается внезапным развитием отеков, протеинурией и повышением содержания мочевой кислоты в плазме крови. Полагают, что в механизме повышения АД в этих случаях принимают участие иммунологические механизмы.
АГ при некоторых сердечно-сосудистых заболеваниях имеет компенсаторный характер и наблюдается при недостаточности аортальных клапанов, атриовентрикулярной блокаде III степени, артериовенозной фистуле.
Повышение АД может быть вызвано приемом оральных контрацептивов, глюкокортикоидов, циклоспорина, алкоголя.
Длительное повышение АД приводит к поражению органов-мише- ней — сердца, мозга, почек, артерий глазного дна.
17.5. Патогенез артериальной гипотензии
Артериальная гипотензия — это падение уровня артериального давления ниже 90 мм рт.ст., которое сопровождается появлением ряда патологических симптомов (слабость, потливость, головокружение, обморок). Снижение АД может быть вызвано влиянием многих факторов. Чаще наблюдаются преходящая ортостатическая гипотензия, реже возможно развитие длительной гипотензии или шока.
Ортостатическая гипотензия — резкое снижение АД (систолического АД более чем на 20 мм рт.ст. и диастолического — более чем на 10 мм рт.ст.), обусловленное нарушением его регуляции. В норме при быстром вставании создаются условия для депонирования крови в венах ног и нижней части туловища, уменьшения притока крови к сердцу и сердечного выброса, что приводит к умеренному снижению АД. В ответ на это барорецепторы дуги аорты и каротидных синусов активируют вегетативные рефлексы и, в частности, вызывают умеренное учащение ритма. При этом увеличивается выброс катехоламинов, повышаются тонус гладкой мускулатуры сосудов, сократимость миокарда, что нормализует сердечный выброс и способствует снижению АД до нормального уровня.
При некоторых заболеваниях, а также под влиянием определенных химических веществ или лекарственных средств могут происходить нарушения в афферентном, центральном или периферическом отделах рефлекторной дуги. В результате при различных патологических состояниях — снижении сократимости миокарда, уменьшении сосудистой реактивности, возникновении гиповолемии или гормональных расстройствах гомеостатические механизмы, необходимые для поддержания АД на нормальном уровне, оказываются несостоятельными.
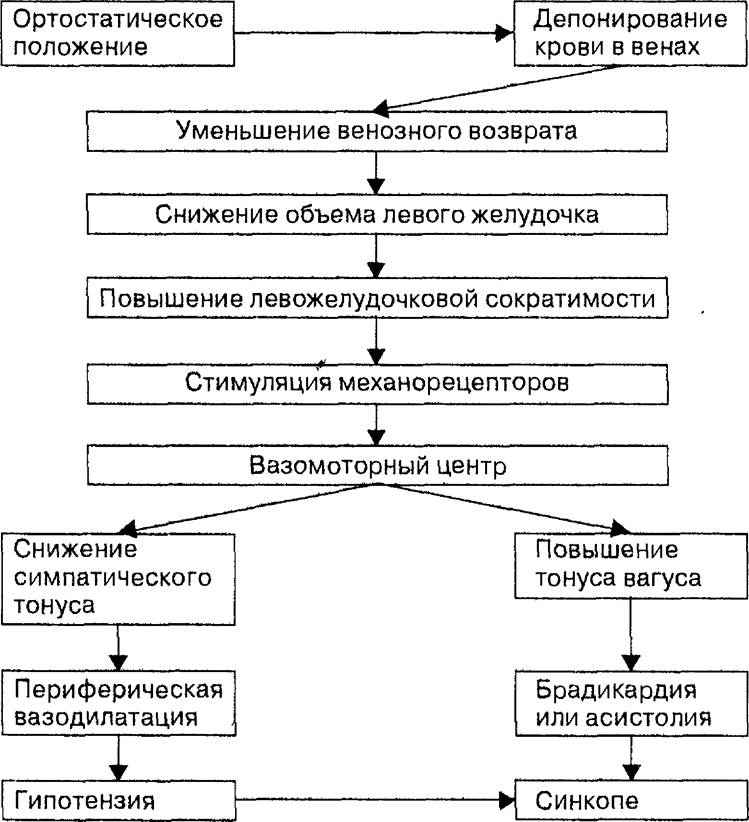
Одной из наиболее частых причин артериальной гипотензии является поражение вегетативной нервной системы, при котором снижается адренергическая реакции на вставание (схема 17.2). Это регистрируют при сахарном диабете, амилоидозе, порфирии, пернициозной анемии, алкоголизме, спинной сухотке, сирингомиелии, тяжелой форме варикозного расширение вен, после перенесенной инфекции. Ортостатическая гипотензия может быть также обусловлена снижением чувствительности барорецепторов. В этих случаях многие другие факторы, вклю-
|
Схема 17.2. Механизмы возникновения ортостатической гипотензии.
чая лекарственные препараты, вызывают более значительное снижение АД при быстрой перемене положения. Дисфункция вегетативной нервной системы может передаваться по наследству (синдром Райна—Дея).
К лекарственным препаратам, нарушающим вегетативные рефлекторные механизмы контроля АД, относятся гипотензивные препараты (симпатолитики, ганглиоблокаторы, блокаторыр-адренорецепторов, ва- зодилататоры). При феохромоцитоме, а также при первичном гипераль- достеронизме в положении лежа регистрируется артериальная гипертен- зия, но в положении стоя возможно развитие гипотензии.
Многие препараты, используемые для лечения психических расстройств, также способны вызвать обратимое нарушение вегетативных механизмов регуляции уровня АД и обусловливать его снижение в положении стоя. Такое действие могут оказывать ингибиторы моноаминокси- дазы, трициклическиеантидепрессанты (амитриптилин, имипрамин), тет- рациклические антидепрессанты и фенотиазиновые антипсихотические препараты (хлорпромазин, меллирил и др).
Ортостатическую гипотензию вызывают некоторые цитостатики (винкристин), барбитураты, алкоголь, L-Дофа, хинидин,
При органических поражениях вегетативной нервной системы неясного генеза (синдром Шая—Дрейджера), для которых характерно поражение симпатической и парасимпатической нервной системы, базальных ганглиев и проводящих путей спинного мозга, происходит угнетение вазоконстрикторной реакции артериол и вен. В результате нарушения регуляции тонуса сосудов АД в положении лежа может быть высоким, а в вертикальном —■ низким. В таких случаях регистрируют и другие проявления вегетативной дисфункции — угнетение потоотделения, атонию кишечника и мочевого пузыря, желудка, импотенцию, уменьшение слюно- и слезоотделения, расширение зрачка и ухудшение зрения.
Шок —остро развившийся синдром, как правило, сопровождающийся падением артериального давления. Может быть обусловлен различными причинами:
• снижением объема циркулирующей крови (гиповолемический шок);
• резким падением сердечного выброса (кардиогенный шок);
• резким снижением сосудистого тонуса (вазомоторный, или сосудистый, шок);
• прекращением венозного притока крови к сердцу из-за тромбоэмболии легочной артерии, напряженного пневмоторакса (обструктив- ный шок).
Возможно также влияние нескольких факторов. При шоке резко снижено кровоснабжение тканей. При этом доставка кислорода ниже минимального уровня, необходимого для поддержания аэробного обмена. В связи с этим обеспечение энергией происходит за счет анаэробного распада с гиперпродукцией кислых метаболитов. Сохранение такого состояния в течение длительного времени вызывает необратимое повреждение клеток.
Гиповолемический шок. Его развитие связано с уменьшением объема (на 20 % и более) циркулирующей крови (ОЦК), уменьшением ударного объема, а также с недостаточным наполнением желудочков. Уменьшение объема циркулирующей крови в течение некоторого времени может компенсироваться учащением ритма сердца и ускорением кровотока. Частой причиной этой формы шока является острая кровопотеря в связи с травмой, язвенной болезнью, варикозным расширением вен пищевода, расслаивающей аневризмой аорты или внематочной беременностью.
Потеря большого количества других жидкостей также вызывает гиповолемический шок, что наблюдается, например, при химических или термических ожогах большой поверхности кожи, перитоните, кишечной непроходимости и скоплении большого количества жидкости в кишечнике, обильной рвоте и поносе. Чрезмерная потеря жидкости развивается при несахарном диабете, недостаточности надпочечников, сольтеряющем нефрите, приеме мощных диуретиков, а также в период полиурической фазы после острого некроза канальцев. Резкое увеличение проницаемости капилляров при аноксии или анафилактической реакции сопровождается расширением артериол и выходом большого количества внутри- сосудистой жидкости в экстравазальное пространство.
Гиповолемический шок в основе своей имеет сниженное наполнение желудочков. Возможно также наличие низкого (менее 5 мм рт.ст.) центрального венозного давления (ЦВД). Однако показатель ЦВД —не точный критерий, так как предшествующая патология (легочная гипертензия, клапанный порок сердца, инфаркт миокарда правого желудочка) также может способствовать снижению ЦВД.
Наиболее точно степень наполнения левого желудочка отражает величина давления в легочной артерии (диастоличес-
кое или давление заклинивания в легочных капиллярах).
Последний показатель при гиповолемии составляет менее 12 мм рт.ст. Обнаруживают также компенсаторное увеличение общего периферического сосудистого сопротивления.
Кардиогенный шок возникает как осложнение при обширном инфаркте миокарда. Встречается также при тяжелом миокардите, остро возникшей аортальной или митральной недостаточности, тромбозе протезированного клапана, разрыве межжелудочковой перегородки, тампонаде сердца.
Для кардиогенного шока характерно высокое давление заклинивания в легочных капиллярах, шейные вены набухают, сердечный выброс резко снижен, возможен отек легких. Однако при инфаркте миокарда правого желудочка шок имеет характер гиповолемического, т.е. давление в легочной артерии снижено.
Вазомоторный шок характеризуется низким центральным венозным давлением и низким давлением в легочной артерии, повышенным сердечным выбросом, низким ОПСС.
Вазомоторный шок развивается при тяжелой черепно-мозговой травме, кровоизлиянии в мозг, острой надпочечниковой недостаточности, анафилаксии, сепсисе, тяжелых интоксикациях. Вазомоторный шок может осложняться нарушением функции миокарда вследствие недостаточной перфузии коронарных артерий, а также кардиодепрессорного действия токсичных веществ.
Обструктивный шок характеризуется снижением ударного объема вследствие нарушения наполнения или опорожнения желудочков от причин, не связанных с поражением сердца. Центральное венозное и давление в легочной артерии может быть высоким или низким, общее периферическое сосудистое сопротивление — высоким.
17.6. Механизмы развития сердечной недостаточности
Сердечная недостаточность — состояние, при котором пропульсив- ная (насосная) функция сердца не обеспечивает метаболические потребности тканей или обеспечивает лишь определенную степень ее компенсации в результате увеличения давления наполнения в желудочках.
Среди взрослого населения причинами сердечной недостаточности в 70—80 % случаев являются ишемическая болезнь сердца, артериальная гипертензия или их сочетание. Развитие сердечной недостаточ- мости возможно также при пороках сердца (10—15 %), болезнях миокарда, кардиомиопатии, патологических процессах в миокарде при других заболеваниях
Сердечная недостаточность может быть обусловлена преимущественно нарушением систолической или диастолической функции желудочков. Возможно одновременное нарушение обеих функций.
Для систолической формы сердечной недостаточности характерны следующие признаки — увеличение размеров сердца, снижение фракции выброса, застой крови в малом и/или большом круге кровообращения.
Для диастолической формы сердечной недостаточности характерны нормальные или умеренно увеличенные размеры сердца, нормальная или увеличенная фракция выброса; редко она может быть умеренно сниженной.
17.б»1 . Систолическая форма сердечной недостаточности
Систолическая форма сердечной недостаточности развивается из- за перегрузки сердца давлением, объемом или вследствие поражения миокарда. Перегрузка давлением может быть вызвана патологическими изменениями клапанного аппарата сердца: стенозом устья аорты, стенозом легочной артерии, а также стенозом митрального и трикуспидально- \ о атриовентрикулярных отверстий, и наряду с этим артериальной гипер- тензией, легочной гипертензией (первичной или вторичной). Перегрузка объемом наблюдается вследствие регургитации крови при недостаточности аортального, митрального или трикуспидального клапанов. Сердечная недостаточность, вызванная поражением миокарда, наблюдается после перенесенного инфаркта миокарда, при миокардитах, идиопати- ческой кардиомиопатии или поражении миокарда при других заболеваниях.
При перегрузке давлением регистрируется увеличение внут- I римиокардиального напряжения, что обусловливает разви- I тие гипертрофии миокарда без дилатации полости же л у- I дочков. I
Нарастание остаточного объема крови в желудочках сопровождается повышением давления в них, снижением фракции выброса и нарастанием перегрузки. При этом уменьшается степень укорочения передне- заднего размера желудочков во время систолы и ухудшаются показатели центральной гемодинамики. Появление признаков сердечной недостаточности сопровождается умеренным расширением полости желудочков, сочетающимся с дальнейшим увеличением массы миокарда и толщины стенок желудочков.
| При перегрузке объемом достаточно быстро возникает ди- I I латация камер сердца, что имеет компенсаторный характер. |
Однако для обеспечения адекватного выброса крови необходимо более значительное напряжение стенок камер, что требует развития гипертрофии миокарда. Увеличение напряжения, возрастание остаточного
объема сопровождаются повышением диастолического давления, что в свою очередь вызывает перегрузку давлением.
При заболеваниях миокарда на ранних стадиях развития систолической формы сердечной недостаточности возникает дилатация полостей желудочков без явлений гипертрофии миокарда, увеличивается их диастолический объем и уменьшается фракция выброса, т.е. нарушается сократительная функция миокарда. В дальнейшем нарастание тяжести сердечной недостаточности сопровождается увеличением объемов камер сердца и массы миокарда, без прироста толщины стенок сердца. Фракция выброса прогрессивно снижается. .
При перегрузке объемом на ранней стадии компенсация обеспечивается включением механизма Франка—Старлинга.
По мере истощения резервов миокарда компенсаторная дилатация желудочка переходит в патологическую» что проявляется нарастанием остаточного объема крови и конечного диастолического давления, а также возникновением симптомов сердечной недостаточности.
Значительную роль в развитии и прогрессировании сердечной недостаточности играют активация ренин-ангиотензин-альдостероновой и симпатической систем.
При систолической сердечной недостаточности повышается чувствительность барорецепторов, что ведет к усилению симпатической стимуляции сердца, почек и периферических сосудов. Гиперактивация ней- роэндокринной системы проявляется увеличением содержания в плазме
|

| Артериальные хеморецегтторы |
| Артериальные барорецепторы |

|
| Отрицательное влияние на сердце |
| Кардиопульмональиые барорецепторы о |
| ^ | Реабсорбция На* ж JJ» }f Сопротивление V^N*/ почечных артерий t ОПСС |
| Мышечные метаболические рецепторы |
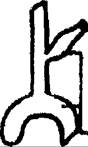
Рис. 17.3, Нейрогуморальные нарушения при сердечной недостаточности. + — активация; — — угнетение; Т — увеличение; ! — уменьшение; ЧСС — число сердечных сокращений; АЦХ — ацетилхолин; НА — норадреналин; А — адреналин; ОПСС — общее периферическое сосудистое сопротивление.
крови норадреналина, который вызывает вазоконстрикцию, тахикардию и задержку натрия и воды (рис. 17.3).
В ответ на симпатическую стимуляцию усиливается синтез ренина в почках и образование ангиотензина II, альдостерона, простагландинов, антидиуретического гормона и эндотелина. Это в свою очередь увеличивает задержку натрия и воды и объем циркулирующей крови (ОЦК). Возрастание ОЦК и притока крови к сердцу способствует повышению диас- толического заполнения желудочков, дилатации сердца, прогрессивному снижению сердечного выброса.
17.6.2. Диастолическая форма сердечной недостаточности
Диастолическая форма сердечной недостаточности возникает в связи с нарушением релаксации и увеличением ригидности стенок желудочков. Уменьшение скорости расслабления желудочков как проявление ухудшения релаксации приводит к уменьшению их наполнений в раннюю фазу диастолы, а увеличение ригидности — к нарастанию конечно-диас- толического давления, что увеличивает нагрузку на предсердия во время их систолы и повышает давление в них, а также вызывает дилатацию предсердий, застой кро^ви в легких и в большом круге кровообращения.
Данная форма сердечной недостаточности развивается при гипертрофии миокарда, поражении миокарда при сахарном диабете, ожирении, перикардите, некоторых редких формах патологии сердца — амилоидо- зе, саркоидозе. Установлено, что диастолическая сердечная недостаточность сопровождается нарушением метаболизма миокарда и энергетического обеспечения сокращения миоцитов, нарушением транспорта ионов и прежде всего кальция. Большую роль в процессе расслабления отводят ионам кальция — их внутриклеточному содержанию, скорости высвобождения, транспорту, повторного захвата, натрий-кальциевому обмену. Сократимость миокарда снижается вследствие уменьшения внутриклеточного содержания АТФазы, изменений изоформ миозина и регу- ляторных протеинов. Возрастание ригидности миокарда определенным образом связано с увеличением содержания коллагена.
17.7. Механизмы развития аритмий
Аритмии сердца — это нарушение образования импульсов возбуждения и/или их распространения по проводящей системе и миокарду.
Возникновение аритмий чаще всего ассоциируется с наличием органического заболевания сердца различной этиологии — ишемией, воспалением, дегенеративными изменениями, токсическим поражением. Однако их регистрируют также у лиц с практически здоровым сердцем, у которых с помощью современных методов исследования, включая прижизненную биопсию миокарда, не выявляют какой-либо патологии. При обследовании населения различных возрастных групп отмечено, что аритмии учащаются параллельно увеличению возраста. В связи с этим в общей популяции определяется наличие взаимосвязи между распространенностью ИБС и частотой обнаружения нарушений ритма сердца.
Общепринятой классификацией аритмий является клинико-элект- рокардиографическая, в соответствии с которой учитывают: ® место образования импульсов (наджелудочковые или желудочковые);
* последовательность их возникновения (преждевременные, выскальзывающие экстрасистолы, регулярные и нерегулярные ритмы или тахикардия);
» характера проведения (нормальное, блокада); » специфические понятия (искусственный водитель ритма, скрытое проведение, интервал сцепления, блокада входа, преждевременное возбуждение, риэнтри и др).
Механизмы возникновения сердечных аритмий изучены в основном в условиях эксперимента (in vitro, in vivo). Существующие в настоящее время в клинике возможности не позволяют с уверенностью раскрыть механизмы возникновения аритмий, так же как и уточнить характер нарушений транспорта ионов через клеточную мембрану и тяжесть внутриклеточных изменений.
Возникновение аритмии при поражении миокарда или специализированных волокон связано с тем, что максимальный диастолический потенциал мембрцны клеток становится менее отрицательным в связи с нарушениями транспорта ионов, которые оказывают влияние на деполяризацию клеток.
Деполяризация клетки может быть следствием увеличения концентрации внеклеточного калия или снижения внутриклеточного калия, увеличения проницаемости мембран клеток для ионов натрия или уменьшения их проницаемости для ионов калия. Кроме того, например, при ишемии миокарда вследствие высвобождения норадреналина и развития внутриклеточного ацидоза увеличивается содержание ионов кальция внутри клеток, что также влияет на величину мембранного потенциала.
I В основе нарушений проводимости лежит уменьшение количества натриевых каналов, принимающих участие в деполяризации, и уменьшение величины быстрого натриевого тока в течение фазы «О» потенциала действия клетки.
В результате уменьшается Vmax (скорость подъема кривой потенциала) и его амплитуда, что сопровождается замедлением проведения импульса возбуждения или развитием полной его блокады.
17.7.1. Нарушение образования импульсов
Дата добавления: 2015-02-05; просмотров: 985;
