НАРУШЕНИЯ АППЕТИТА 4 страница
При гипохолии ослабляется перистальтичес-
 кая активность кишечника, что ведет к усилению метеоризма, гниения, брожения, так как выпадает бактерицидное действие желчи.
кая активность кишечника, что ведет к усилению метеоризма, гниения, брожения, так как выпадает бактерицидное действие желчи.
16.5.2. Нарушение внешней секреции поджелудочной железы
Объем секрета поджелудочной железы составляет 1500 мл в сутки. Он выделяется в тонкую кишку и содержит ферменты, гидролизирующие белки, жиры и углеводы. Регуляция секреции осуществляется гормонами - холецистокинином (стимулирует секрецию ферментов) и секретином (стимулирует секрецию бикарбонатов). Регуляция панкреатической секреции осуществляется через блуждающий нерв.
Основными причинами нарушений внешней секреции поджелудочной железы являются: 1)недостаточная продукция секретина при ахлор-гидрии; 2) неврогенное торможение функции поджелудочной железы (при ваготомии, отравлении атропином); 3) развитие аллергических реакций; 4) воздействие различными химическими веществами (отравление фосфором, свинцом, ртутью, кобальтом); 5) травмы брюшной полости; 6) токсикоинфекции (брюшной тиф, паратифы); 7) хронические инфекции (туберкулез, малярия); 8) алиментарные факторы (избыточный прием пищи,животных жиров и др.); 9)разрушение поджелудочной железы опухолевым процессом; 10) закупорка и сдавление протока опухолью; 11) дуодениты - воспалительные процессы в ДПК любой этиологии (инфекционные, паразитарные и др.), ведущие к уменьшению образования секретина, с последующей гипосек-рецией поджелудочной железы; 12) воздействие алкоголем, что усиливает выброс соляной кислоты, ведущей к стимуляции выработки секретина с избыточным выделением панкреатического секрета; 13) острые и хронические панкреатиты.
Этиология и патогенез острого панкреатита.Рассматриваются 3 механизма развития острого панкреатита. Наиболее принята теория самопереваривания ткани железы,согласно которой протеолитические ферменты - трипсино-ген, химотрипсиноген, проэластаза и фосфоли-паза А активируются внутри протока поджелудочной железы. Полагают, что некоторые факторы (эндо- иэкзотоксины, в частности алкоголь, вирусные инфекции, ишемия и травма) активируют проферменты, т. е. в условиях па-
тологии трипсиноген может активироваться в железе под влиянием кофермента цитокиназы, выделяющейся из поврежденных клеток паренхимы. Важную роль в развитии панкреатита играет и ингибитор трипсин, который в норме в достаточном количестве содержится в поджелудочной железе и препятствует превращению трипсиногена в трипсин. При большой активности трипсина ингибиторы антиферментной системы истощаются и возникает их дефицит. Это используется как тест в диагностике острого панкреатита - чем выше содержание трипсиногена в сыворотке крови, тем меньше ингибитора трипсина. При дефиците этого фактора отмечается активный переход трипсиногена в трипсин. Усиленная активность протеолитических ферментов, особенно трипсина, приводит к перевариванию ткани поджелудочной железы и к активации других ферментов - эластазы и фосфо-липазы. Происходит переваривание активными ферментами клеточных мембран, наблюдаются протеолиз, отек, интерстициальное воспаление, повреждение сосудов, коагуляционный, жировой некроз (стеатонекроз)и некроз паренхимы железы. Повреждение и разрушение клеток ведут к высвобождению активированных ферментов. Переваривающее действие ферментов сказывается и на периферии - феномен «уклонения ферментов в кровь», что вызывает развитие некротических процессов в других органах. При попадании липазы в кровь возможны некрозы отдаленных органов с тяжелой последующей интоксикацией. Процесс может осложниться перитонитом и абсцессами брюшной полости. Трипсин активирует панкреатический калликреин, вызывающий образование каллидина и бради-кинина, которые усиливают повреждение ткани железы. Идет дальнейшая активация кинино-вой системы. Активация и высвобождение бра-дикинина и гистамина вызывают различные ге-модинамические расстройства. Расширяются сосуды, повышается проницаемость их стенок и развивается отек железы. Выход жидкости и белка в ткани ведет к снижению онкотического давления и к развитию панкреатического коллапса,иногда со смертельным исходом. Этот коллапс можно воспроизвести в эксперименте при внутривенном введении животному панкреатического сока. Если сок предварительно прокипятить, то коллапс не разовьется.
Вторая теория - это теория «общего канала».Благодаря анатомической особенности у


 большинства людей (у 80%) имеется общий желчный и панкреатический проток, что облегчает рефлюкс желчи в проток поджелудочной железы. Однако в норме давление в панкреатическом протоке в 2 раза выше, чем в общем желчном протоке (200 мм вод. ст.). Это предохраняет от заброса желчи и кишечного содержимого в протоки поджелудочной железы. Заброс желчи может отмечаться при гипертонусе сфинктера Одди или при гипермоторной дискинезии желчных путей. Частое развитие панкреатита при желчекаменной болезни объясняется происходящим повышением давления в желчевыводящей системе. Это обеспечивает заброс инфицированной желчи под большим давлением в панкреатический проток, что вызывает химическое повреждение ткани железы, повышает ее ферментативную активность. Фосфолипаза желчи активирует трипсиноген. При желчекаменной болезни приступы острого панкреатита могут быть связаны с преходящей обтурацией фатерова соска желчными камнями. Заброс кишечного содержимого возможен при зиянии фатерова соска или при гипертонической дискинезии ДПК, возникающей при воспалении, воздействии алиментарных и других факторов. При этом попадающая в железу энтеропептидаза активирует трипсиноген. Образовавшийся трипсин оказывает аутокаталитическое действие - активирует трипсиноген и другие протеолитические ферменты. Так, если в эксперименте ввести в проток поджелудочной железы небольшое количество трипсина, то происходит выраженный некроз ее ткани, поскольку образуются активные протеолитические ферменты.
большинства людей (у 80%) имеется общий желчный и панкреатический проток, что облегчает рефлюкс желчи в проток поджелудочной железы. Однако в норме давление в панкреатическом протоке в 2 раза выше, чем в общем желчном протоке (200 мм вод. ст.). Это предохраняет от заброса желчи и кишечного содержимого в протоки поджелудочной железы. Заброс желчи может отмечаться при гипертонусе сфинктера Одди или при гипермоторной дискинезии желчных путей. Частое развитие панкреатита при желчекаменной болезни объясняется происходящим повышением давления в желчевыводящей системе. Это обеспечивает заброс инфицированной желчи под большим давлением в панкреатический проток, что вызывает химическое повреждение ткани железы, повышает ее ферментативную активность. Фосфолипаза желчи активирует трипсиноген. При желчекаменной болезни приступы острого панкреатита могут быть связаны с преходящей обтурацией фатерова соска желчными камнями. Заброс кишечного содержимого возможен при зиянии фатерова соска или при гипертонической дискинезии ДПК, возникающей при воспалении, воздействии алиментарных и других факторов. При этом попадающая в железу энтеропептидаза активирует трипсиноген. Образовавшийся трипсин оказывает аутокаталитическое действие - активирует трипсиноген и другие протеолитические ферменты. Так, если в эксперименте ввести в проток поджелудочной железы небольшое количество трипсина, то происходит выраженный некроз ее ткани, поскольку образуются активные протеолитические ферменты.
Третья теория объясняет развитие панкреатита обструкцией панкреатического протокаи гиперсекрецией.Обструкция (спазм сфинктера Одди, отек ДПК и др.) вызывает задержку выделения панкреатического секрета с последующей активацией ферментов внутри железы.
Основными этиологическими факторами(в 70%случаев) острого панкреатита являются желчекаменная болезнь и прием алкоголя.Возникновение острых алкогольных панкреатитов объясняется не только токсическим воздействием алкоголя. Алкоголь стимулирует выброс соляной кислоты, которая, воздействуя на слизистую двенадцатиперстной кишки, усиливает секрецию секретина. Последний является мощным стимулятором панкреатической секреции, избыточное выделение которой ведет к повыше-
нию давления в протоках железы и развитию острого панкреатита. Кроме того, крепкие алкогольные напитки способствуют отеку слизистой ДПК, что вызывает спазм фатерова соска с последующим повышением давления в панкреатических протоках. Известно и непосредственное воздействие алкоголя на сосуды поджелудочной железы, вызывающее их спазм. Это ведет к ишемии органа с гибелью ацинозных клеток и к активации ферментов в ткани железы. Прием алкоголя в дозе более 100 г/сут в течение нескольких лет может привести к преципитации панкреатических ферментов в мелких протоках и формированию белковых пробок. Более редкими причинами развития острого панкреатита являются травмы живота, гиперлипидемия (особенно I и IV типа), прием некоторых лекарственных препаратов (азотиаприн, сульфазалазин, фуросемид, кортикостероиды, эстрогены), инфекции (эпидемический паротит, болезнь Боткина, сальмонеллез), оперативные вмешательства, диагностическая ретроградная холангиопанкреа-тография, анатомические аномалии панкреатического протока (стриктуры, опухоли), гипер-кальциемия, уремия, сосудистые поражения, наследственная предрасположенность.
При панкреатите развиваются 3 стадии: острый приступ (отек, возможно, панкреонекроз), стадиянеполного излечения с персистирующим хроническим воспалением или деструкцией панкреатического протока и затем стадия хронического воспаления с экзокринной недостаточностью поджелудочной железы. То есть с развитием фиброзных изменений в ткани железы, связанных с перенесенным острым панкреатитом, наступает внешнесекреторная (экзокринная) недостаточность поджелудочной железы, характерная для хронического панкреатита. В железе уменьшается, а затем полностью прекращается (при склерозировании, сморщивании органа) образование пищеварительных ферментов (панкреатическая ахилия).Нарушаются полостное пищеварение (в полости тонкой кишки) и всасывание. В первую очередь резко страдает переваривание и всасывание жиров. Жиры до 60-80% не усваиваются и в повышенном количестве выводятся с калом (стеаторея - выделение с калом более 5 г в сутки или более 5-6% от введенного изотопа - триолеат-глицерина J131). Отмечается полифекалия, при копрологическом исследовании в кале много нейтрального жира (так как нарушается расщепление жиров до
Глава 16 / ПАТОФИЗИОЛОГИЯ ПИЩЕВАРЕНИЯ
жирных кислот). Стеаторея вызывает потерю организмом кальция, который экскретируется вместе с жирами в виде нерастворимых мыл (в кале, кроме нейтрального жира, будут мыла). Наряду с ионами кальция, теряются и ионы магния, цинка, которые также образуют мыла с невсосавшимися жирами. Развиваются синдромы гипокальциемии, гипомагниемии. В меньшей степени и позднее нарушается переваривание белка (не усваивается до 30-40%). Об этом свидетельствует появление большого количества мышечных волокон в кале (креаторея),особенно после приема мясной пищи. Переваривание углеводов также нарушается. Отмечается снижение объема секреции поджелудочной железы, гидрокарбонатов в панкреатическом соке (после стимуляции секретином 1 мг/кг массы) и ферментов - амилазы, трипсина, липазы (после стимуляции панкреозимином 1,5 мг/кг массы). Расстройство пищеварения усугубляется диспепсическим симптомокомплексом. Возникает синдром диареи, развивается синдром малдигестии, идет прогрессирующая потеря массы (в случае отсутствия заместительной терапии).
16.5.3. Нарушение секреторной
функции тонкой кишки
Расстройства секреторной функции кишечника могут зависеть от уменьшения количества отделяемого сока, снижения содержания и активности его ферментов и нарушений пристеночного пищеварения. Они часто обусловлены ин-тестинальными энзимопатиями- недостаточной продукцией ферментов в тонкой кишке. Энзи-мопатии могут быть врожденнымии приобретенными.Чаще встречается дисахаридная недостаточность(врожденный дефицит ферментов - дисахаридаз) и особенно недостаточность лак-тазы,сопровождаемая признаками непереносимости лактозы. Поскольку лактоза служит важнейшим углеводом молока, ее недостаточность вызывает непереносимость молочных продуктов. Особенно тяжело она протекает у детей первого года. При этом нерасщепленная лактоза переходит в толстую кишку, где под влиянием микрофлоры распадается до молочной и уксусной кислот. Последние являются осмотически активными веществами и, вызывая приток в кишку большого количества воды, способствуют болям в животе спастического характера, метеоризму и
диарее. Развивается недостаточность пищеварения, ведущая к истощению, снижению роста и задержке развития ребенка. При дефиците са-харазы и изомальтазы больные плохо переносят сахарозу и крахмал. У детей описан дефицит сахаразы, при котором отмечались хронические поносы. Исключение сахарозы из пищевого режима приводило к прекращению поносов. После нагрузки сахарозой не наступал подъем уровня глюкозы в крови (плоские гликемические кривые), в то время как прием смеси глюкозы и фруктозы, моносахаридов, из которых состоит сахароза, вызывал повышение уровня сахара. Установлена генетическая природа этой патологии (по аутосомно-рецессивному типу). Значительно реже встречается недостаточность трега-лазы, которая расщепляет дисахарид трегалозу, содержащийся в грибах, водорослях и у насекомых (у некоторых народов Востока доля его в пище значительна). При дефиците трегалазы плохо переносятся грибы, особенно молодые. К редким формам пептидазной недостаточности относится врожденный дефицит энтерокиназы (энтеропептидазы). Энтерокиназа является ключевым ферментом протеолитических процессов в кишечнике. Она активирует панкреатический трипсиноген, переводя его в активный протео-литический энзим - трипсин. В этом случае у детей наблюдаются тяжелые нарушения белкового обмена, гипопротеинемия, отеки, диарея, синдром мальабсорбции. Больных лечат экстрактами поджелудочной железы.
К врожденным энтеропатиям относится и глю-теновая болезнь.При развитии этой болезни нарушается расщепление глютена (белковый компонент клейковины, склеивающий составные части некоторых злаков: пшеницы, ржи, ячменя, овса). Существуют две основные теории патогенеза глютеновой болезни. Согласно первой интестинальные эпителиальные клетки, участвующие в процессе переваривания глютена, лишены соответствующей пептидазы или протеазы. В связи с этим не происходит расщепления и последующего всасывания глютена. Заболевание рассматривают как метаболический дефект, из-за которого непереваренный глютен и продукты его неполного расщепления оказывают токсическое действие на слизистую тонкой кишки. Согласно второй теории первичную роль играют иммунологические реакции на глютен. Нерас-щепленный глютен, взаимодействуя с иммуно-цитами слизистой, приводит к их сенсибилиза-
Часть III. ПАТОФИЗИОЛОГИЯ ОРГАНОВ И СИСТЕМ
ции, в частности к сенсибилизации лимфоцитов. В результате этого образуются различные продукты иммуногенеза - антитела к глютену, иммунизированные лимфоциты, лимфокины, вызывающие повреждение кишечного эпителия с нарушением его переваривающей и всасывающей функций. Существуют доказательства участия генетических факторов в патогенезе глюте-новой болезни. Основными диагностическими критериями ее являются: мальабсорбция, субто-гальная или тотальная атрофия слизистой тонкой кишки, клинический эффект от безглюте-новой диеты.
Приобретенные энзимопатии могут быть связаны с недостаточной продукцией как одного (моноэнзимопатии), так и нескольких (полиэн-зимопатии) ферментов кишечного сока. Они сопровождаются вздутием кишечника (метеоризм), диареей и ведут к другим проявлениям синдрома малдигестии.
Нарушение преимущественно полостного пищеварения (синдром малдигестии) возникает вследствие многих причин: некомпенсированного снижения секреторной функции желудка, тонкой кишки, поджелудочной железы, желчеотделения. Существенную роль в его возникновении играют нарушения двигательной функции желудочно-кишечного тракта: застой содержимого вследствие спазма, стеноза или сдавления кишки, ускорение пассажа пищевого химуса из-за усиленной перистальтики. Клинически синдром малдигестии проявляется болями в животе, главным образом в околопупочной области, диспепсическими симптомами - ощущением полноты, вздутия живота, тошноты. Часто отмечаются непереносимость молока, особенно сырого, вздутие, урчание в кишечнике, так как молочный сахар не расщепляется до глюкозы и галактозы, а образуются промежуточные продукты гидролиза, вызывающие метеоризм. Наблюдаются вазомоторные и нейровегетативные симптомы (чувство жара, потливость, тахикардия), связанные с повышенной чувствительностью тонкой кишки к поступлению химически и осмотически несоответствующего содержимого. Нарушение пищеварения ведет к нарушению всасывания.
В клинической картине малдигестии могут преобладать признаки нарушения пищеварения в различных отделах желудочно-кишечного тракта. Различают желудочную, кишечную и панк-
реатическую формы. Возникновение желудочной формы связано обычно с атрофическим гастритом, приводящим к секреторной недостаточности. Возможно развитие желудочной формы и при декомпенсированном стенозе привратника, раке желудка. Клинически она характеризуется потерей аппетита, ощущением тяжести, распираний и давления в эпигастральной области после еды, отрыжкой воздухом, пищей с тухлым запахом, метеоризмом, диареей. При исследовании желудочной секреции выявляют ахилию, ахлоргидрию. При кишечной форме, связанной с хроническим воспалительным процессом в тонкой кишке, выявляются урчание, переливание в кишечнике, вздутие живота, метеоризм, неустойчивый стул с преобладанием поносов. При нарушении кишечного полостного пищеварения чаще находят кишечную стеато-рею, когда преобладают жирные кислоты, мыла, амилорею, креаторею, повышенное содержание аммиака. О степени нарушения полостного пищеварения судят по уровню ферментов (энтеро-киназы и щелочной фосфатазы) в кишечном содержимом и кале, а также по характеру глике-мической кривой при нагрузке крахмалом и исследованию всасывания жиров при последовательной нагрузке триолеат-глицерином J131 и олеиновой кислотой, меченной J131. Возникновение панкреатической формы малдигестии связывают с внешнесекреторной недостаточностью поджелудочной железы. В клинике преобладают анорексия, метеоризм, коликообразные боли в животе, обильные «панкреатогенные» поносы. При копрологическом анализе выявляются стеаторея панкреатического типа (за счет нейтрального жира), амилорея, креаторея. При заболеваниях кишечника нередко наблюдается сочетание всех трех форм нарушения полостного пищеварения.
16.5.4. Нарушение пристеночного (мембранного) пищеварения
При полостном пищеварении гидролизируют-ся крупномолекулярные вещества, образуя оли-гомеры. Их гидролиз завершается адсорбированием на микроворсинках и гликокаликсе ферментами в зоне исчерченной каймы энтеро-цитов с образованием уже мономеров (пристеночное пищеварение). Конечные продукты гидролиза олигомеров - мономеры всасываются в
Глава 16 / ПАТОФИЗИОЛОГИЯ ПИЩЕВАРЕНИЯ
кровь и лимфу. Микроворсинки апикальной мембраны эятероцитов представляют собой мельчайшие цитоплазматические выросты, длина которых составляет 1 мкм, ширина - 0,1 мкм. Благодаря такой структуре активная поверхность пищеварения возрастает в 30 раз. Расстояние между ворсинками колеблется от 10 до 20 нм, и поэтому в щеточную кайму проникают только мелкие молекулы. Микробы, размеры которых составляют несколько микрометров, не способны проникать через нее - это своеобразный бактериальный фильтр. Процессы пристеночного пищеварения совершаются на огромной поверхности. Слизистая тонкой кишки имеет складки, ворсинки и микроворсинки, увеличивающие ее внутреннюю поверхность в 300-500 раз. Ферменты, последовательно осуществляющие в гликокалик-се и на цитоплазматической мембране микроворсинок пристеночное пищеварение, имеют двоякое происхождение. Часть их адсорбируется из полости тонкой кишки (куда они поступают в составе панкреатического и кишечного соков), и они связываются с гликокаликсом микроворсинок. Другая часть переносится из энтероцитов (кишечного эпителия), фиксируясь на цитоплаз-матических мембранах микроворсинок. Основными кишечными ферментами, участвующими в пристеночном гидролизе углеводов, являются D-глюкозидазы (мальтаза, трегалаза и др.), р-галактаза (лактаза), глюкоамилаза (у-изоамила-за), инвертаза и др. Гидролиз олиго- и дипепти-дов осуществляется несколькими пептидазами фосфорных эфиров (например, щелочной фос-фатазой), а липидов - липазами. В гликокаликсе ферментами расщепляются продукты полостного гидролиза - олигомеры до стадии димеров. До мономеров расщепление происходит на цитоплазматической мембране микроворсинок, и из этой зоны они попадают в энтероцит.
Причинами нарушения пристеночного пищеварения могут быть:
1) нарушения структуры ворсинок и микроворсинок, уменьшение их числа на единицу поверхности (А. М. Уголев). Это характерный признак хронических заболеваний тонкой кишки, где морфологическим субстрактом являются воспалительные, дистрофические и склеротические изменения слизистой оболочки. Развитие атро-фических изменений слизистой тонкой кишки, преимущественно ворсинок, отмечается при дизентерии, холере;
2) изменение ферментного слоя кишечной
поверхности в результате генетической или при
обретенной недостаточности ферментов, участву
ющих в пристеночном пищеварении. Первичная
недостаточность пристеночного пищеварения,
как правило, развивается у детей в раннем воз
расте при приеме в пищу непереносимого диса-
харида. Приобретенная недостаточность чаще
является следствием заболеваний тонкой киш
ки - хронического энтерита, а также следствием
вирусного гепатита и других инфекций;
3)расстройства кишечной перистальтики, что приводит к нарушению переноса пищевых веществ из полости кишки на поверхность энтероцитов, например хронические энтериты, болезни Уиппла, болезни Крона и другие заболевания тонкой кишки;
4)недостаточность полостного пищеварения, когда мало расщепленные крупные молекулы не проходят в щеточную кайму эпителия ворсинок.
Клиническая картина недостаточности пристеночного пищеварения аналогична диспепсии при синдроме недостаточности всасывания. Отмечаются упорные поносы. Кал жидкий, обильный, пенистый. С целью уточнения диагноза определяют активность ферментов (амилазы, липазы) при последовательной их дезорбции в гомогенатах биопсии слизистой оболочки тонкой кишки, полученных при еюноскопии. Часть биоп-тата исследуют морфологически, что позволяет обнаружить воспалительные, атрофические изменения слизистой. Сопоставление активности определяемых ферментов в десорбируемых фракциях позволяет вывести кривые активности ферментов, которые характеризуют взаимоотношения полостного и мембранного пищеварения. Нарушение пристеночного пищеварения при хронических энтеритах определяется и с помощью других методических приемов.
16.5.5. Нарушение всасывания в кишечнике
Нарушения всасывания проявляются в его замедлении или патологическом усилении. Замедление всасываниялежит в основе синдрома мальабсорбции(от франц. mal - болезнь), обусловленного нарушением всасывания в тонкой кишке одного или нескольких пищевых веществ. Синдром мальабсорбции может быть первичным(врожденным или наследственно обус-
Часть III. ПАТОФИЗИОЛОГИЯ ОРГАНОВ И СИСТЕМ
 ловленным) или вторичным(приобретенным). Врожденное нарушение всасывания встречается в клинической практике редко. Чаще всего это патология детского возраста, обусловленная, например, врожденными нарушениями транспорта (недостаточность ферментов-переносчиков) аминокислот в тонкой кишке. Так, с этим связаны синдром нарушения всасывания нейтральных аминокислот (болезнь Хартнапа - пеллаг-рические изменения кожи, мозжечковая атаксия); синдром нарушения всасывания цистеина и основных аминокислот, синдром снижения всасывания многих аминокислот (синдром Лоу - врожденная катаракта, глаукома, гипертония, остеопороз, умственная отсталость), снижение всасывания лизина (врожденная лизинурия -непереносимость белков, диарея, рвота, отставание в развитии) и др. Возможно врожденное нарушение всасывания глюкозы и галактозы. В слизистой тонкой кишки таких больных отсутствует фермент глкжозо-6-фосфатаза. При врожденном нарушении абсорбции фруктозы в слизистой оболочке имеется дефицит фруктозо-1-фосфатальдолазы, отвечающей за ее транспорт. Происходит изолированное нарушение всасывания данных веществ, возникают диарея и боли в животе. Первичная мальабсорбция витамина В12 или фолиевой кислоты ведет к развитию ме-галобластной анемии.
ловленным) или вторичным(приобретенным). Врожденное нарушение всасывания встречается в клинической практике редко. Чаще всего это патология детского возраста, обусловленная, например, врожденными нарушениями транспорта (недостаточность ферментов-переносчиков) аминокислот в тонкой кишке. Так, с этим связаны синдром нарушения всасывания нейтральных аминокислот (болезнь Хартнапа - пеллаг-рические изменения кожи, мозжечковая атаксия); синдром нарушения всасывания цистеина и основных аминокислот, синдром снижения всасывания многих аминокислот (синдром Лоу - врожденная катаракта, глаукома, гипертония, остеопороз, умственная отсталость), снижение всасывания лизина (врожденная лизинурия -непереносимость белков, диарея, рвота, отставание в развитии) и др. Возможно врожденное нарушение всасывания глюкозы и галактозы. В слизистой тонкой кишки таких больных отсутствует фермент глкжозо-6-фосфатаза. При врожденном нарушении абсорбции фруктозы в слизистой оболочке имеется дефицит фруктозо-1-фосфатальдолазы, отвечающей за ее транспорт. Происходит изолированное нарушение всасывания данных веществ, возникают диарея и боли в животе. Первичная мальабсорбция витамина В12 или фолиевой кислоты ведет к развитию ме-галобластной анемии.
Вторичное нарушение всасывания более распространено. Оно связано с такими заболеваниями кишечника, печени, поджелудочной железы и других органов, как:
1) недостаточное расщепление пищи в желудке (из-за ахлоргидрии, субтотальной резекции желудка, стволовой ваготомии) или двенадцатиперстной кишке;
2) экзокринная панкреатическая недостаточность (хронический панкреатит, рак, кистозный фиброз, резекция поджелудочной железы);
3) заболевания печени (хронические гепатиты, циррозы) и обструкция желчных путей (камни желчного пузыря или рак головки поджелудочной железы), что связано с недостаточностью желчных кислот, поступающих в ДПК;
4) ишемическая энтеропатия с возможным инфарктом кишечника (например, при отравлении свинцом, мезентериальном атеросклерозе);
5) воспаление тонкой кишки различной этиологии (острые и особенно хронические энтериты с развитием изменений в слизистой тонкой киш-
ки вплоть до атрофии, что уменьшает ее всасывательную поверхность), болезнь Крона (с поражением ДПК или подвздошной кишки);
6) дисбактериоз, когда особенно страдает абсорбция жира и витамина В12, так как микробы вызывают деконъюгацию желчных кислот в кишечнике и поглощают витамин В12;
7) лучевая (радиационная) энтеропатия, связанная с облучением кишечника, например при лечении онкологических заболеваний, что вызывает отек слизистой, позднее - атрофию ворсинок и истончение слизистой оболочки. Поражение подвздошной кишки приводит к дефициту витамина В12 и нарушению кишечно-пече-ночного обмена желчных кислот;
8) резекция части тонкой кишки (синдром короткой кишки), связанная с травмой, тонкокишечной непроходимостью, сосудистыми тром-боэмболиями, тяжелой болезнью Крона и др.;
9) кишечная непроходимость в верхних отделах кишки, когда пищевые массы не поступают в дистальные ее отделы;
10)двигательные расстройства кишечника, в частности при ускоренной перистальтике, когда уменьшается время контакта химуса с всасывательной поверхностью тонкой кишки;
11)закупорка лимфатических путей (лимфан-гиоэктазия кишечника, болезнь Уиппла, лим-фома);
12)сердечно-сосудистые болезни (перикардиты, застойная сердечная недостаточность II Б -III стадии, васкулиты);
13)иммунодефицит, эндокринные нарушения (сахарный диабет, гипо- и гиперпаратиреоз, синдром Золлингера - Эллисона).
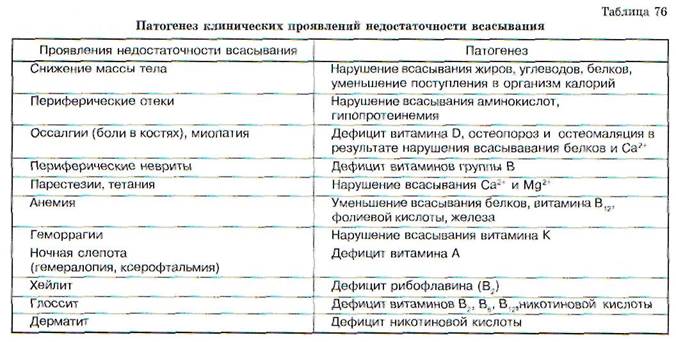
Вследствие нарушения всасывания развивается синдром мальабсорбции, который характеризуется, помимо изменений со стороны желудочно-кишечного тракта, патологическими изменениями со стороны других органов и систем (табл. 76).
Нередко возникает вздутие живота, обычно после еды, связанное с приемом молока, повышенное газообразование. Отмечается диарея в связи с накоплением в полости кишечника осмотически активных веществ, ускорением транзита по кишечнику и гиперэкссудацией. Наблюдается полифекалия с остатками непереваренной пищи. Возникает стеаторея - признак нарушения всасывания жира (потери жира с калом составляют более 5 г/сут, доходя до 10 г/сут и
Глава 16 / ПАТОФИЗИОЛОГИЯ ПИЩЕВАРЕНИЯ
|
более). Потери радиоактивного жира с калом после нагрузки олеиновой кислотой, меченной J131, составляют более 5% от введенной активности и до 30% при выраженном характере нарушения всасывания. При проведении пробы с d-ксилозой наблюдается снижение всасывания углеводов (экскреция d-ксилозы с мочой ниже 1,2 г за 5 ч, т. е. менее 25% от введенной дозы) при приеме ее внутрь - 5 г. Позднее нарушается всасывание белка (отмечаются повышенные потери альбумина J131 с калом, составляющие более 3% от введенной активности).
Важным клиническим симптомом нарушения всасывания является потеря в массе (при I степени мальабсорбции - до 5-10 кг, при II степени - свыше 10 кг, при III степени - свыше 20 кг). Возникают признаки гипоавитаминозов, трофические расстройства. Кожа становится сухой с пониженным тургором, волосы - сухими, тусклыми, отмечается выпадение волос. Наблюдаются изменения ногтевых пластинок, их ломкость, а также болезни десен, гиперемия языка, сглаженность его сосочков, что объясняется дефицитом витаминов В2, В6, В1г, никотиновой кислоты. Отмечается кровоточивость десен, связанная с дефицитом витамина С. Нередко развиваются полиневриты, нарушение зрения, обусловленные дефицитом витамина А. При тяжелом синдроме мальабсорбции страдает всасыва-
ние микроэлементов. Вследствие дефицита кальция возникает остеопороз, вплоть до остеомаляции. Нарушение всасывания железа ведет к развитию железодефицитной анемии. За счет нарушения всасывания белков развивается гипопро-теинемия с последующим отечным синдромом. Могут наблюдаться нарушения деятельности эндокринных желез по типу плюригландуляр-ной недостаточности - развитие эндокринопатии с поражением гипофиза, надпочечников, половых желез.
Патологическое усиление всасыванияможет быть связано с повышенной проницаемостью кишечной стенки (например, при ее артериальной гиперемии или раздражении эпителия кишечника). Усиление всасывания легко развивается у детей раннего возраста, когда проницаемость кишечной стенки довольно высока. При этом быстро всасываются и вызывают интоксикацию продукты неполного расщепления пищевых веществ. В неизмененном виде может всасываться белок коровьего молока или куриного яйца, что вызывает сенсибилизацию организма с развитием аллергических реакций.
Дата добавления: 2015-03-19; просмотров: 897;
