Физические свойства металлов
Электронное строение металлов определяет такие их общие физические свойства, как блеск, ковкость, пластичность, высокие тепло- и электропроводность. Практически все металлы, кроме ртути, при комнатной температуре – твердые вещества. Большинство из них кристаллизуется в одной из трех форм кристаллических решеток:
а) кубическая гранецентрированная (Al, Cu, Ag);
б) кубическая объемноцентрированная (Na, K, Ba);
в) гексагональная (Mg, Zn, Cd).
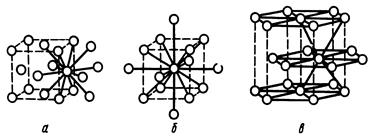
Рис. 2. Кристаллические решетки металлов: а – кубическая гранецентрированная; б – кубическая объемноцентрированная; в - гексагональная
Металлы обладают полиморфизмом – способностью в определенных условиях кристаллизоваться в разных формах.
При температуре затвердевания расплавленного кристалла кристаллизация начинается одновременно во многих точках – центрах кристаллизации. Обычно кристаллы металлов имеют неправильную форму за счет сросшихся мелких кристаллов, то есть образуют кристаллиты. В особых случаях при температуре затвердевания расплавленного металла можно получить монокристалл (кристаллизация идет из одной точки).
Сплавы
В жидком состоянии большинство металлов растворяются друг в друге, образуя однородные расплавы. При охлаждении расплавов происходит кристаллизация, в процессе которой получаются сплавы. Металлы и сплавы широко используются как конструкционные и электротехнические материалы. Сплавы улучшают свойства металлов, придавая им новые свойства (жаропрочность, коррозионную устойчивость, механическую прочность и др.).
Изучение природы сплавов, их особенностей и свойств, а также свойств чистых металлом – область науки, называемой металловодением. В основе металловедения лежит физико-химический анализ – установление зависимости между изучаемым свойством и составом системы. Результаты исследования выражаются графически в виде диаграммы состав – свойство. Изучаемыми свойствами могут быть температура плавления или кристаллизации (термический анализ), электропроводность, плотность и др.
При проведении термического анализа диаграмма состав – свойство строится в координатах температура плавления (затвердевания) – процентный состав компонентов и называется диаграммой плавкости. Диаграммы плавкости строят с помощью кривых охлаждения.
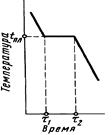
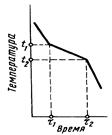
Кривая охлаждения чистого вещества приведена на рис. 3а. Горизонтальный участок соответствует температуре плавления или затвердевания. Как только исчезает жидкая фаза, охлаждение продолжается с обычной скоростью. Кривая охлаждения смеси веществ (рис. 3б) не имеет горизонтального участка и изменяет наклон в двух точках (начало и конец кристаллизации).
|
|
| а | б |
Рис. 3. Кривые охлаждения: а- чистого вещества; б – смеси веществ
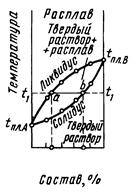
По характеру взаимодействия компонентов различают три основных вида твердых сплавов: 1) твердый раствор одного компонента в другом; 2) механическая смесь, состоящая из кристаллов одного и другого компонентов; 3) химическое соединение одного компонента с другим. Диаграммы плавкости различных видов сплавов приведены на рис. 4.
|
|
|
| а | б | в |
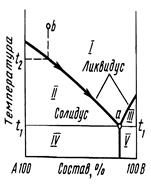
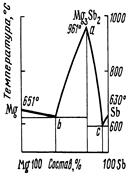
Рис. 4. Диаграммы плавкости сплавов: а) твердый раствор одного компонента в другом; б) механическая смесь, состоящая из кристаллов одного и другого компонентов; в) химическое соединение одного компонента с другим.
Верхние кривые на диаграммах плавкости (ликвидус) показывает температуры, при которой из жидкой фазы начинают выделяться кристаллы. Выше этой кривой лежит область расплава. Нижняя кривая (солидус) показывает температуры конца затвердевания. Под ней на диаграмме лежит область твердой фазы. Между кривыми ликвидуса и солидуса находится область, отвечающая сосуществованию жидкой и твердой фаз.
Диаграмма плавкости, представленная на рис. 4а, соответствует неограниченной растворимости одного металла в другом как в жидкой, так и в твердой фазе. Образованию таких сплавов способствует близость химических свойств металлов, их атомных радиусов и типа кристаллической структуры (например, Cu – Au).
Диаграмма плавкости сплава, являющегося механической смесью компонентов (рис. 4б), имеет пять областей. Область I, отвечает однородной жидкой фазе (расплаву компонентов А + В). Области, отвечающие двухфазным состояниям системы: II – твердая фаза компонента А + жидкая фаза расплава А + В; III – твердая фаза компонента В + жидкая фаза расплава А + В; IV – твердая фаза компонента А, вкрапленная в сплав эвтектического состава; V – твердая фаза компонента В, вкрапленная в сплав эвтектического состава.
Однородный сплав А + В можно рассматривать как ненасыщенный раствор (А в В или В в А). При охлаждении начинается постепенное выделение из раствора одного из компонентов, растворимость которого достигает насыщения. При этом жидкая фаза обогащается другим компонентом в соответствии с кривой ликвидуса (движение по стрелкам) до тех пор, пока состав расплава и температура кристаллизации не достигнут минимума. Расплав такого состава (эвтектический состав) насыщен одновременно по двум компонентам и поэтому затвердевает полностью. Температура плавления эвтектической смеси обычно ниже температуры плавления ее отдельных компонентов. К числу сплавов, образующих эвтектику, относятся сплавы Bi – Cd, Pb – Sb, Sn – Pb. Например, температура плавления чистой сурьмы равна 630°С, а температура плавления свинца равна 327°С, в то время, как эвтектическая смесь, содержащая 13% сурьмы и 87% свинца, плавится при температуре 246°С и используется как легкоплавкий припой. Сплавы типа эвтектических образуют металлы, близкие по природе, но имеющие разные формы кристаллических решеток.
Металлы, имеющие чаще всего несходную химическую природу и заметно отличающиеся по электроотрицательности, образуют сплавы, относящиеся к химическим соединениям (интерметаллидам). Диаграммы состояния сплавов такого типа можно представить как наложение двух диаграмм сплавов эвтектического типа. Максимум на кривой ликвидуса соответствует составу химического соединения. Состав интерметаллида определяется валентными состояниями металлов (K4Pb), взаимными размерами атомов (MgCu2) или числом электронов в зоне проводимости (Cu5Zn8).
Дата добавления: 2016-11-22; просмотров: 774;
