И комплексных ионов
Большинство комплексных соединений являются электролитами. В растворах они необратимо диссоциируют на внутреннюю и внешнюю сферу (первичная диссоциация):
[Cu(NH3)4]SO4 
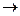 [Cu(NH3)4]2+ + SO42
[Cu(NH3)4]2+ + SO42
Комплексный ион способен к вторичной диссоциации и является слабым электролитом (обратимая и ступенчатая диссоциация): [Cu(NH3)4]2+ 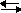 [Cu(NH3)3]2+ + NH3
[Cu(NH3)3]2+ + NH3
[Cu(NH3)3]2+ 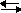 [Cu(NH3)2]2+ + NH3
[Cu(NH3)2]2+ + NH3
[Cu(NH3)2]2+ 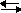 [Cu(NH3)]2+ + NH3
[Cu(NH3)]2+ + NH3
[Cu(NH3)]2+ 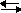 Cu2+ + NH3
Cu2+ + NH3
Суммарный процесс: [Cu(NH3)4]2+ 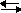 Cu2+ + 4NH3
Cu2+ + 4NH3
Каждый из этих обратимых процессов характеризуется константой равновесия Кнест, которая носит название константы нестойкости комплексного иона (ступенчатая или общая). Чем меньше величина константы нестойкости, тем более устойчиво комплексное соединение. Константы нестойкости – табличные значения.
Константа равновесия реакции образования комплексного иона за счет взаимодействия центрального иона с лигандами носит название константы устойчивости, Куст. Так как реакция образования комплексного соединения противоположна реакции его диссоциации, то Куст = 1/Кнест.
Смещение равновесие реакции диссоциации комплексного иона подчиняется всем описанным ранее правилам смещения химического равновесия: равновесие смещается в сторону более полного связывания молекул и ионов в растворе в молекулы или ионы слабых электролитов (равновесие химической реакции смещается в сторону образования более устойчивого комплексного соединения.
Дата добавления: 2016-11-22; просмотров: 701;
