КРИСТАЛЛИЗАЦИЯ ПРИ ИЗМЕНЕНИИ ТЕМПЕРАТУРЫ РАСТВОРА
Пересыщение в этом методе создается за счет такого изменения температуры насыщенного раствора, которое переводит его в метастабильное, неравновесное состояние (см. диаграмму растворимости на рис. 1-8).
В тех редких случаях, когда растворимость падает с повышением температуры (см., например, MgS04-H20 на рис. 1-9), температурный коэффициент растворимости мал и поэтому описываемый метод для выращивания кристаллов таких веществ практически не применяется. В силу ограниченности объема кристаллизатора невозможно осуществить процесс так, чтобы он шел одновременно при постоянных температуре и пересыщении. Поэтому кристаллизация ведется так, что точка состав — температура движется в области метастабильных растворов вдоль кривой насыщения в сторону уменьшения растворимости, что соответствует снижению температуры, почему описываемый метод обычно называют методом кристаллизации при снижении температуры.
Как следует из гл. 1, изменение температуры и пересыщения неизбежно в большей или меньшей мере сказывается на ходе процесса роста и порождает различие состава и строения между отдельными зонами кристалла. В этом основной недостаток метода.
Для выращивания кристаллов по методу снижения температуры используют кристаллизаторы, изображенные на рис. 5-2. Объем раствора определяют, исходя из необходимого размера (массы) кристалла и хода растворимости вещества (рис. 3-1, а). Так, если растворимость при температуре начала процесса составляет cmax г/100 г растворителя, а при температуре конца процесса — cmin и нужно получить кристалл массой A, г, то минимальное количество раствора в граммах составит
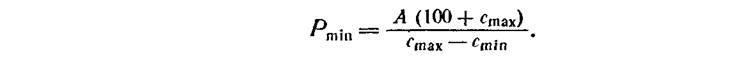
Верхняя граница температур, с которых начинают процесс кристаллизации, обычно 50—70° С. При более высоких температурах постановка опыта существенно затрудняется. Необходим подогрев фильтровальной колбы и фильтра; при откачке воздуха из колбы раствор начинает кипеть и резко растут потери растворителя. Кроме того, чем выше температура, тем большую опасность представляет открывание кристаллизатора (при введении затравки, в частности) ввиду испарения раствора и образования паразитических кристаллов на его поверхности. С повышением температуры уменьшается также ширина метастабильной зоны раствора, что предъявляет повышенные требования к качеству термостатирования и к чистоте при постановке опытов.
При известном опыте выращивания кристаллов эти затруднения, в общем, преодолимы, но нужно хорошо отдавать себе отчет в особенностях постановок при повышенных температурах. Заметим, что в случае очень больших затруднений можно перейти к выращиванию методом тепловой конвекции (§ 3.6) практически без изменений в технике. Обычно нижний предел снижения температуры — комнатная. Однако с целью максимального извлечения вещества из раствора можно снижать температуру в термостате и ниже комнатной. Это достигается введением холодильников в термостат с прогоном через них водопроводной или специально охлаждаемой воды. Таким путем добиваются снижения температуры на 10—15° С ниже комнатной.
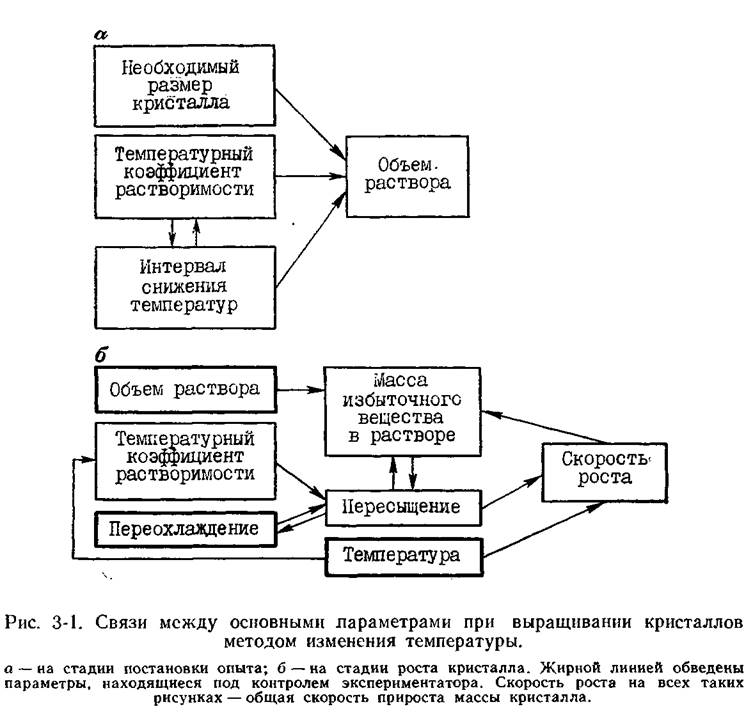
При выборе рабочего участка кривой растворимости нужно учитывать, что крутизна кривой растворимости обычно увеличивается с возрастанием температуры. Иначе говоря, выбор интервала снижения температур и температурного коэффициента растворимости сообразуют между собой, что отмечено стрелками на рис. 3-1, а.
Взаимосвязи между основными параметрами при выращивании кристаллов по этому методу достаточно просты (рис. 3-1,б). Произведение температурного коэффициента растворимости на величину переохлаждения дает пересыщение раствора. Пересыщение раствора в совокупности с объемом раствора создают общую массу избыточного вещества в растворе. Пересыщение в совокупности с температурой определяют скорость роста и соответственно качество кристалла. Качество кристалла, как уже упоминалось в предыдущей главе, влияет в свою очередь на скорость роста. По мере роста кристалла в зависимости от его скорости уменьшается избыточная масса вещества в растворе, т. е. соответственно и пересыщение, и переохлаждение. Основная трудность технического порядка при использовании этого метода — это контроль за изменением пересыщения в процессе роста кристалла, что порождает затруднения в выборе необходимой скорости снижения температуры с целью поддержания пересыщения на необходимом уровне. Обычно идут по пути экспериментального подбора оптимальных скоростей снижения t для разных периодов роста.
Методика постановки опытов следующая. Приготавливается раствор с концентрацией, соответствующей насыщению при выбранной температуре, которая, пусть, например, составляет 50°С, и перегревается градусов на десять. Тщательно вымытый кристаллизатор, который не следует сушить, а тем более вытирать (при этом попадают механические примеси!), прикрытый от попадания пыли из воздуха, должен находиться в термостате при 55—57° С. Раствор быстро — чтобы не остыл — фильтруется и без промедления сливается в кристаллизатор, который сразу закрывается временной крышкой с закрепленным в ней термометром.
Неточность в табличных данных по растворимости, ошибки при взвешивании и отмеривании растворителя и растворяемого вещества, потери растворителя при приготовлении раствора и фильтрации — все это приводит к тому, что к моменту заливки раствора в кристаллизатор температура его насыщения может существенно отличаться от ожидаемой. Если раствор сильно недосыщен, то затравка в нем будет быстро растворяться, а большая тепловая инерция термостата и кристаллизатора не позволит быстро установить нужную температуру и предотвратить потерю затравки. Если в кристаллизаторе раствор пересыщен, то приоткрывание крышки кристаллизатора, не говоря уже о введении в него затравки, ведет к запаразичиванию раствора и к срыву опыта.
Для роста удовлетворительных кристаллов многих веществ требуются переохлаждения, составляющие десятые доли градуса или первые градусы. Повышение пересыщения часто ведет к порче кристалла и к запаразичиванию раствора. Все это вынуждает перед постановкой затравки определять температуру насыщения раствора tн (§ 4.4). Если выбран способ определения температуры насыщения по конвекционным потокам или по наблюдению за ростом — растворением кристалла непосредственно в кристаллизаторе, то в крышке наряду с термометром укрепляют кристаллоносец с пробным кристаллом.
Крышка тщательно моется, а кристалл должен быть сполоснут теплой водой. После окончания определения tH пробный кристалл извлекают и в термостате устанавливают температуру на 5—6° С выше температуры насыщения. Кристаллизатор герметизируется и оставляется на 10—12 ч для растворения попавших из воздуха или отделившихся от пробного кристалла частиц, которые могут стать центрами кристаллизации. По истечении этого срока температуру снижают. К этому времени подготавливается кристаллоносец с затравкой. После мытья в горячей воде кристаллоносца и крышки споласкивается теплой водой затравка. Удобно, особенно для кристаллов, плохо переносящих резкие изменения температуры, выдерживать кристаллоносец и крышку в теплых парах растворителя. Для этого достаточно в свободный кристаллизационный сосуд налить немного горячей воды, закрыть его крышкой с кристаллоносцем и держать его так до момента постановки. Хранение чистого кристаллоносца в открытом виде не допускается.
Когда температура в кристаллизаторе станет на 2—2,5° С выше температуры насыщения, в кристаллизатор можно ввести затравку. Делать эту операцию нужно быстро, лучше вдвоем. Один убирает крышку с термометром, другой переносит крышку с кристаллоносцем на кристаллизатор, после чего оба его герметизируют. Температуру в термостате снижают до температуры роста, например на 1°С ниже tн, и ждут начала регенерации кристалла, которая устанавливается по появлению отблесков от граней или по помутнению поверхности, что при некотором навыке легко замечается. При регенерации в районе будущих вершин и ребер возможно появление очень тонких нависающих слоев кристаллического вещества, которые при преждевременном включении движения могут отрываться и давать начало паразитическим кристаллам. Поэтому следует подождать с включением движения до завершения регенерации, отмечаемой по исчезновению замутнения поверхности. Если по истечении нескольких часов ни на дне кристаллизатора, ни на кристаллоносце не возникло паразитических кристаллов, если затравочный кристалл не превратился в сросток или в скелет, то можно считать, что первая часть постановки опыта успешно завершена. Следующий этап — собственно выращивание кристалла — требует постепенного снижения температуры.
С какой скоростью и как снижать температуру кристаллизации? Здесь возможно несколько вариантов. Первый, наименее благоприятный, когда предварительным обследованием (кристаллизацией в малых объемах раствора, согласно рекомендациям предыдущей главы) установлено только, что кристаллы из имеющегося вещества и выбранного растворителя растут визуально однородными (прозрачными), а сведений о желательном пересыщении нет. В этом случае к вопросу подходят грубо эмпирически — методом проб и ошибок. Например, в начале опыта задано переохлаждение 1°С. Рост идет хорошо. Допустим, через 12 ч снижают температуру на 0,4° С. Все в порядке. Еще через 12 ч — на 0,4° С. Через час-полтора появились включения.
Не следует прерывать процесс, пусть кристалл испорчен. Регулярно записывая время, снижение температуры и реакцию кристалла, мы получим сведения для корректировки своих действий при последующих опытах.
Появившиеся включения раствора свидетельствуют о том, что при существующем размере кристалла и скорости перемешивания раствора (или движения кристалла) пересыщение велико. Для его уменьшения по прошествии следующих 12 ч либо вообще не снижают температуру, либо снижают ее на 0,2—0,3° С. Если наблюдение за поверхностью в отраженном свете показывает, что грани стали гладкими, т. е. включения заросли, необходимое снижение пересыщения найдено.
При последующем снижении можно вновь вернуться к скачку в 0,4° С и проверить реакцию кристалла. Если включения перестали появляться, можно постепенно увеличивать скачки снижения, имея в виду, что увеличивающийся в размере кристалл при сохранении линейной скорости роста будет иметь возрастающий прирост массы. Результаты эксперимента нужно перенести на график время — температура с отметками периодов возникновения включений и следующий опыт проводить с уменьшением тех скоростей снижения, которые привели к появлению дефектов. Для хорошо растворимых веществ с крутой зависимостью растворимости от температуры и в случае простой геометрической формы кристалла, приставив линейку к кристаллизатору, определяют приблизительно размеры и массу кристалла. Затем (конечно, с погрешностью) рассчитывают температуру насыщения при данной температуре роста. И, уже исходя из этого расчета, определяют, насколько следует снизить температуру в кристаллизаторе. Заметим, что в цилиндрических кристаллизаторах остаются неискаженными лишь вертикальные размеры кристалла.
Слежение за размерами кристалла удобно вести, если на крис-таллоносец нанести метки через 5 мм.
Описанная последовательность операций проста, но она относится к получению кристаллов, в общем хорошо растущих (Аl - К-квасцы, сегнетова соль, семиводный сульфат магния), которые легко получить массой до 200—300 г. Что касается других веществ, то обычно довольно легко найти оптимальные условия для получения небольших кристаллов, но трудности резко возрастают при увеличении их размеров. Опыт показывает, что такой путь поиска оптимальных условий выращивания какого-либо даже не слишком капризного вещества может занять месяцы. Поэтому подчеркнем еще раз, что не следует считать потерянным время, потраченное на предварительное обследование роста методом, описанным в § 2.2.
Поиск оптимальных условий роста крупных кристаллов облегчается, если кристаллизатор снабжен измерителем пересыщения — переохлаждения (§ 4.4). В этом случае нахождение нужных пересыщений на разных этапах роста кристалла ведется таким же путем, как описано выше, — по границе между внешне однородным и неоднородным ростом, но здесь мы уже можем действовать гораздо увереннее, определяя числовые значения области пересыщений, в которой растут кристаллы удовлетворительного качества.
В описываемом способе выращивания сложной задачей является борьба с возникновением паразитических кристаллов. Единичные или множественные паразиты могут появиться вскоре — в первые часы после начала роста основного кристалла — или появиться (появляться) по истечении более длительных сроков. В первом случае причины связаны с ошибками в постановке эксперимента, во втором — с нарушением нормального хода кристаллизации. Основные причины появления паразитов при постановке сводятся к следующим.
1. Попадание кристаллической пыли из воздуха при введении затравки в кристаллизатор. Для предотвращения этого работы с соответствующим сухим веществом должны проводиться либо в другом помещении, либо в вытяжном шкафу.
2. Плохое обмывание крышки, кристаллоносца и затравки.
3. Дефектность затравки — трещины и включения в ней, что приводит к отрыву от нее крупинок при выдержке кристалла в не-досыщенном растворе перед началом роста.
4. Недостаточное время или низкая температура выдержки раствора после определения температуры насыщения с помощью пробного кристалла.
5. Слишком большое начальное пересыщение, которое может быть следствием как испарения, ввиду плохой герметизации кристаллизатора при выдержке раствора перед введением затравки, так и ошибки при определении температуры насыщения.
Если эти погрешности постановки сравнительно легко устранимы, то появление плавающих кристаллов или кристаллических пленок на поверхности кристаллизатора говорит за то, что необходимо либо менять температуру начала процесса, либо даже как-то изменять аппаратуру. Если герметизация удовлетворительна, то появление плавающих кристаллов на поверхности является результатом переохлаждения поверхности раствора. Устранению переохлаждения поверхности способствует дополнительная теплоизоляция крышки кристаллизатора либо даже специальный обогрев ее.
Причины появления паразитических кристаллов по истечении суток и более после начала роста обычно следующие.
1. Единичные кристаллы, особенно если они появляются в одних и тех же местах кристаллоносца или кристаллизатора из опыта в опыт, свидетельствуют о наличии трещин и царапин, в которых даже при тщательном мытье посуды сохраняются остатки кристаллической фазы. Это происходит при использовании кристаллизаторов, в которых было допущено высыхание раствора. В такие сосуды перед их использованием надо на несколько суток налить растворитель. Кристаллоносцы, имеющие сложную форму, вообще лучше хранить в растворителе.
2. Нарушение герметизации кристаллизатора, что обычно вызывает массовое запаразичивание.
3. Нарушение нормального движения кристаллоносца, приводящее к его вздрагиванию и выкрашиванию кристалла в контакте с ним.
4. Появление трещин в кристалле, выходящих на его поверхность (о причинах их см. в § 3.10).
5. Превышение допустимой скорости снижения температуры, что приводит к переходу раствора в лабильное состояние. Этому почти всегда предшествует порча кристалла, появление включений, расщепление, рост в виде скелета, дендрита и т. д. Разумеется, может действовать одновременно ряд причин, и устранение какой-либо одной из найденных причин не даст тогда ощутимых результатов. В качестве способа борьбы с паразитами можно использовать такой подогрев, который обеспечивает более высокую температуру придонных частей раствора. Это достигается, в частности, если в использующемся, обычно жидкостном, термостате оставить такое количество воды, чтобы кристаллизатор был погружен в нее всего на 10—15 мм. В этом случае температура в кристаллизаторе будет несколько ниже температуры термостата. Последняя мера в общем не может считаться радикальной, так как уменьшение поверхности контакта кристаллизатора с термостатирующей жидкостью приводит к снижению стабильности температуры в кристаллизаторе, что в свою очередь влияет на однородность кристаллов, а также резко увеличивает переохлаждение поверхности раствора.
Заметим, что описанные причины возникновения паразитических кристаллов являются общими для почти всех методов кристаллизации.
Температуру в процессе выращивания снижают либо вручную — один - два раза в сутки (желательно чаще, но на более малые значения), в соответствии с подобранным режимом снижения, либо с помощью специальных устройств (§ 5.4), позволяющих уменьшать ее плавно и непрерывно. Автоматическое снижение температуры, разумеется, предпочтительнее ручного.
Кристаллизацию можно считать законченной по истечении суток с момента последнего снижения температуры. Затем кристалл извлекается из кристаллизатора (§ 4.7). Оставшийся раствор может быть вновь использован. Для этого в раствор добавляется вещество в количестве, равном массе полученного кристалла. Во время длительных опытов бывают заметные потери растворителя. Поэтому после зарядки кристаллизатора нужно измерить уровень раствора, а после окончания опыта и досыпки вещества долить растворитель до прежнего уровня раствора. После этого вновь определяют температуру насыщения и ведут процесс, как было изложено выше.
Даже в случае использования весьма чистых веществ многократное получение кристаллов из одного и того же раствора ведет к накоплению в нем примесей, которые рано или поздно начнут
заметно влиять на рост и качество кристаллов. Нужно суметь вовремя уловить этот момент и полностью заменить раствор. Это замечание относится и к ряду последующих методов.
Описываемый метод широко применяется для получения кристаллов из растворов, в том числе из раствора в расплавах солей. Этому способствует относительная простота метода и, по-видимому, большая его освоенность по сравнению со многими другими.
С помощью этого метода выращивается ряд важных в промышленном отношении веществ: дигидрофосфат калия, дигидрофосфат аммония, сегнетова соль, бифталат калия, алюмокалиевые квасцы и др.
В природе при снижении температуры растворов образуется, видимо, наибольшая часть всей массы кристаллов. При снижении температуры кристаллизуются горные породы из магмы, представляющей собой, как уже говорилось в § 1.2, поликомпонентные растворы. При снижении температуры образуются кристаллы различных минералов из растворов при самых разных температурах, в том числе и высокотемпературных (гидротермальных) растворов. При уменьшении температуры кристаллизуется лед, при падении температуры осенью и зимой растут кристаллы в соляных озерах. Заметим, что в последнем случае пересыщение создается также и за счет испарения, что рассматривается в следующем параграфе.
3.3. КРИСТАЛЛИЗАЦИЯ ПРИ ИСПАРЕНИИ РАСТВОРИТЕЛЯ
Для создания избытка вещества здесь используются различия в скорости испарения из раствора растворенного вещества и растворителя. Поэтому главным требованием для использования этого метода является то, что давление равновесных (насыщенных) паров растворителя над раствором должно быть существенно больше давления равновесных паров растворенного вещества. Это требование практически всегда выполняется для водных растворов ионных соединений, но не всегда реализуется для растворов органических соединений. Вторым общим требованием является превышение давления насыщенных паров растворителя над данным раствором сверх реально существующего давления паров растворителя в окружающей среде.
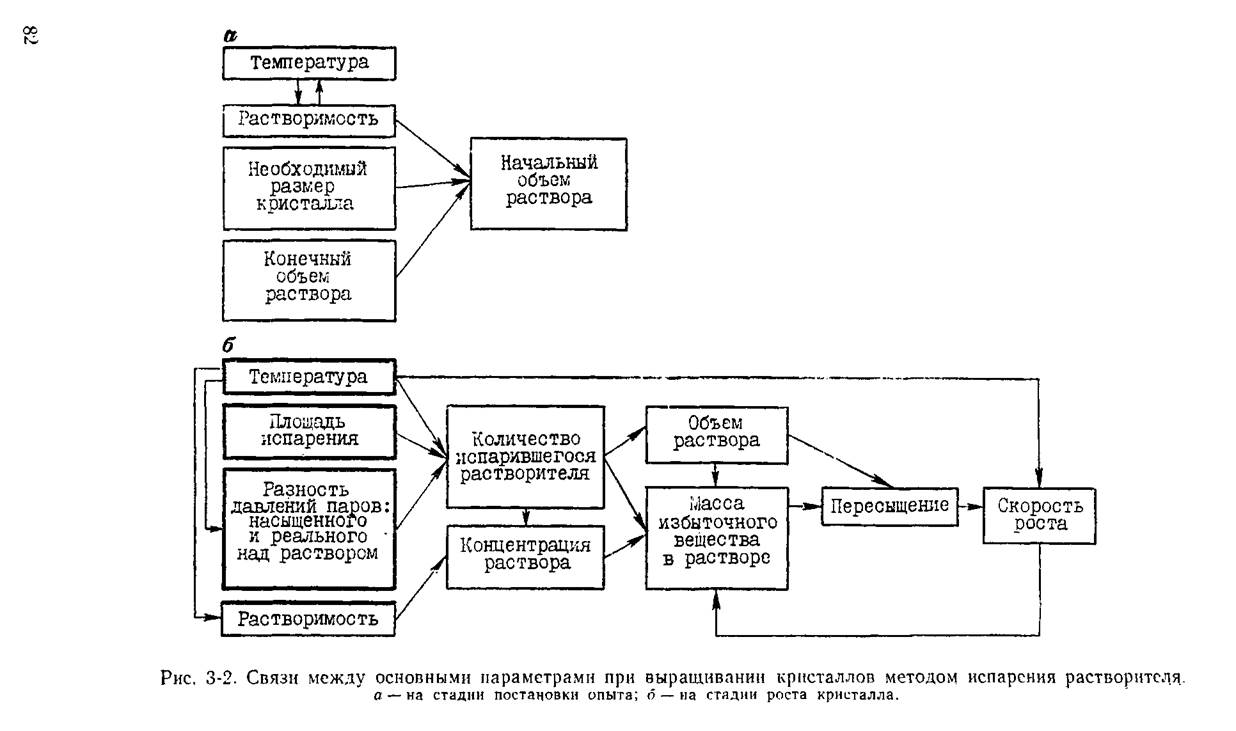
На рис. 3-2, а показано, какие параметры являются определяющими при постановке выращивания кристаллов по этому методу. Выбор температуры и растворимости взаимообусловлен, что отражают противоположно направленные стрелки между обоими указанными параметрами. Взаимосвязь между основными параметрами в процессе выращивания кристалла методом испарения изображена на рис. 3-2, б. Температура, площадь испарения раствора и разность упомянутых выше давлений определяют количество испарившегося растворителя.* Произведение количества испарившегося
* Вообще говоря, равновесное давление паров растворителя зависит от концентрации раствора, но здесь это несущественно, и соответствующая стрелка отсутствует, так как концентрация раствора в течение выращивания почти не изменяется.
|
растворителя на концентрацию раствора (в граммах на 100 г растворителя) дает массу избыточного вещества в растворе. От количества испарившегося растворителя зависит наличный объем раствора. Масса избыточного вещества, будучи отнесенная к объему раствора, определяет пересыщение. Рост кристалла приводит к уменьшению массы избыточного вещества, т. е. и к уменьшению пересыщения.
Общие требования к устройствам для кристаллизации по этому методу следующие.
1. Кристаллизатор должен быть термостатирован. При слабой зависимости растворимости от температуры и в случае не очень высоких требований к качеству кристаллов нередко применяется пассивное термостатирование (§ 5.3), обеспечивающее отсутствие резких колебаний температуры. Оно не ликвидирует плавных, хотя, может быть, и значительных, ее изменений, которые не так опасны для кристалла. Дело в том, что при медленных колебаниях температуры, например в период ее повышения, пересыщение уменьшается. Но одновременно при повышении температуры увеличивается скорость испарения, что препятствует уменьшению пересыщения. При понижении температуры действуют обратные тенденции. Таким образом, происходит частичная саморегулировка пересыщения. Однако всегда, когда есть возможность, следует использовать активное термостатирование (воздушные термостаты, например, или хотя бы сушильные шкафы).
2. Испарение раствора необходимо вести при изоляции раствора от пыли, находящейся в воздухе. Несоблюдение этого приводит к появлению паразитических кристаллов.
Выделим два варианта осуществления описываемого метода.
а) Испарение растворителя в атмосферу. Это один из простей
ших приемов получения кристаллов. Здесь необходимы: сосуд лю
бой формы, предпочтительно из стекла (стандартный кристалли
затор, стеклянная банка, колба), пыленепроницаемый фильтр —
лист фильтровальной бумаги или кусок плотной ткани для пере
крытия отверстия сосуда и кусок шпагата, которым закрепляется
фильтр. Фильтр можно прижать перфорированной крышкой или
плоским кольцом. Щелей между фильтром и торцом отверстия ис
пользуемого сосуда не должно быть. Поэтому крышка должна
быть плоской и не должна коробиться при увлажнении и нагреве.
Если торец сосуда недостаточно плоский, его пришлифовывают.
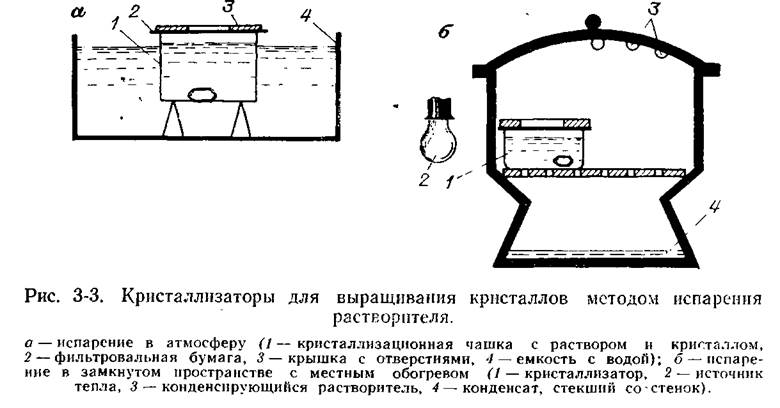
На рис. 3-3, а показан такой кристаллизатор, помещенный в пассивный термостат.
б) Испарение растворителя в закрытом сосуде. Для использования этой методики, помимо желания ускорить испарение, могут
быть и другие причины. Первая — невозможность получения кристалла вышеописанным путем, из-за того что равновесное давление
паров растворителя над раствором меньше, чем реально существующее в атмосфере. Растворы некоторых солей (например, Nal)
поглощают из воздуха воду и разбавляются. Вторая — нежелательность испарения растворителя в атмосферу, из-за того что он
либо ядовит, либо имеет неприятный запах, огнеопасен или дефицитен.
Для поддержания испарения в закрытом сосуде создают внутри него перепад давления паров растворителя. Это может быть сделано путем помещения в указанный сосуд какого-нибудь вещества, поглощающего пары используемого растворителя, как это делается в обычном эксикаторе, в который для поглощения водяных паров помещается концентрированная серная кислота или обезвоженный хлористый кальций. Если же вещество, поглощающее пары, трудно подобрать (например, пары органических растворителей) или если стремятся к повышенной чистоте при кристаллизации, так как поглотители паров сами испаряются и их пары поглощаются раствором, то можно организовать местный боковой подогрев кристаллизатора. На удаленных от него стенках сосуда идет конденсация паров, и конденсат в простейшем варианте этой методики стекает на дно сосуда (рис. 3-3, б).
Методика постановки опыта при выращивании кристаллов по описываемому способу следующая. Вымешиванием или с использованием табличных данных приготавливается раствор, насыщенный при выбранной температуре роста. Раствор перегревается на 8—10° С и заливается в чистый, можно мокрый, кристаллизатор. Если растворимость вещества сильно зависит от температуры, то кристаллоносец вводится в раствор, когда температура будет выше температуры роста на 2—3°С. Раствор можно заливать в кристаллизатор, в котором уже находятся затравки. В этом случае, чтобы предотвратить их полное растворение, затравки следует помещать в углубления, высверленные в пластине из какого-либо инертного материала (фторопласт, оргстекло). Кристаллизатор закрывается заранее подготовленными фильтром, крышкой с отверстиями (или кольцом) и устанавливается в термостат или эксикатор. После установки кристаллизатора его нельзя переставлять, двигать,
наклонять, так как жидкость, смочившая стенки, может дать начало паразитическим кристаллам. Если затравка на стадии постановки сильно уменьшилась в размерах, кристалл может появиться из углубления лишь на вторые — третьи сутки. Поэтому не следует спешить с выводами о неудаче опыта.
Внешняя простота описанного метода не означает отсутствия трудностей при получении крупных однородных кристаллов. По мере испарения растворителя и высадки растворенного вещества возрастает концентрация в растворе всех примесей, коэффициент распределения которых меньше единицы. Так, при уменьшении объема растворителя вдвое почти вдвое увеличивается концентрация плохо входящих в кристалл примесей, и при сохранении коэффициента распределения соответственно почти вдвое увеличивается концентрация этих примесей в кристалле. Поэтому, в принципе, нужно использовать специально очищенные вещество и растворитель. Можно, кроме того, вести получение небольших кристаллов из больших объемов раствора, с тем, чтобы в течение опыта несущественно изменялся объем раствора.
Пересыщение также изменяется в процессе кристаллизации. Изменение пересыщения зависит в первую очередь от скорости испарения. Скорость испарения единицы массы растворителя при прочих равных условиях зависит от поверхности жидкости в кристаллизаторе S. Возникающий избыток растворенного вещества распределяется в объеме раствора W. Скорость нарастания пересыщения в отсутствие затравки пропорциональна S/W. Если взять, как это обычно делается, цилиндрический сосуд радиусом r, то пересыщение, мало изменяющееся при большой высоте жидкости в нем, очень быстро увеличивается, когда жидкости остается немного. Зависимость элементарна:
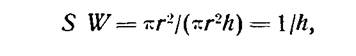
где h — высота столба жидкости. Поэтому опять-таки рационально вести кристаллизацию, пока изменение уровня невелико по сравнению с самим уровнем. (Между прочим, резкие различия в скоростях роста кристаллов и их огранки в пределах одной испаряющейся капли на предметном стекле связаны с неравномерностью нарастания пересыщения в разных участках капли).
Так как поверхность свободно растущего кристалла увеличивается во время роста, кристалл будет выбирать со временем все больше и больше вещества. Поэтому нарастание пересыщения в известной степени компенсируется увеличением поверхности растущих кристаллов. Отсюда следует, что большая площадь кристаллов (несколько затравок) обеспечит меньшие пересыщения, а следовательно, в общем и более высокое качество кристаллов. Понятно, что прирост каждого кристалла уменьшится по сравнению с тем, который был бы при наличии одной затравки.
Таким образом, важнейшие параметры, с помощью которых можно управлять здесь ростом кристалла, — это объем и поверхность раствора (т. е. отношение S/W), температура, давление па ров растворителя в окружающей среде, растворимость.
Однако интенсификация испарения с помощью изменения каких-либо из упомянутых параметров заключает в себе опасность запаразичивания, особенно серьезную в этом методе. Дело в том, что при выращивании по этому методу в статическом режиме концентрация раствора сильно переменна от точки к точке. На поверхности раствора может создаться очень большое пересыщение, которое не успеет распределиться по остальному объему раствора. В результате на поверхности начнется самопроизвольное зародышеобразование.
Если нужно уменьшить испарение, т. е. вести опыт при меньшем пересыщении, то либо увеличивают число листов фильтровальной бумаги, покрывающей кристаллизатор, либо уменьшают площадь отверстия (отверстий) в крышке, придавливающей бумагу.
Одно из обычных затруднений, встречающихся в этом методе, — ползучесть раствора по стенкам кристаллизатора. Поднимаемый капиллярными силами раствор кристаллизуется на стенках и дает начало паразитическим кристаллам. Для борьбы с ползучестью применяется обмазывание стенок кристаллизатора выше уровня раствора инертным веществом — парафином, воском и т. д. Однако нельзя забывать, что при повышенной температуре эти вещества могут, давая пленку на поверхности раствора, существенно затормозить испарение. Ползучесть затормаживается, если кристаллизационный сосуд имеет наклонные внутрь стенки (заметим, что в этом случае переменна площадь испарения). Наблюдается связь между ползучестью и скоростью испарения. В связи с этим можно попытаться снизить скорость испарения. Ползучесть сильно зависит от кислотности раствора, что заметно проявляется, например, при кристаллизации KNO3. Поэтому можно также избавиться от ползучести, несколько меняя кислотность среды, если, конечно, это не отражается на качестве кристалла и не ведет к нежелательным химическим реакциям в растворе. Простой метод борьбы с ползучестью и связанным с ней запаразичиванием предложил И. В. Исаков [1973]. В крышке кристаллизатора делается отверстие с диаметром, существенно меньшим, чем диаметр кристаллизатора. В него плотно вставляется стеклянный цилиндр, нижний край которого должен находиться на высоте нескольких миллиметров над поверхностью раствора. Цилиндр сверху закрывается так же, как кристаллизатор в других случаях в этом методе. В пространстве вокруг цилиндра над раствором давление паров становится близким к давлению насыщения, испарение здесь затрудняется, и паразитические кристаллы не возникают. Единственная погрешность этого технического решения задачи — необходимость поддержания указанного расстояния между цилиндром и раствором, чего без усложнения конструкции не добиться.
Простые варианты метода испарения удобны для получения небольших кристаллов, пригодных для исследования целого ряда их физических свойств. Этим путем выращивают визуально однородные
кристаллы многих соединений с хорошей растворимостью, таких как сернокислые соли магния, никеля, цинка, калия и др., некоторые нитраты, сегнетову соль и многие другие. Таким путем можно получить первые сведения об особенностях роста кристаллов, вырастить первые затравки нового вещества.
В природе при испарении растворителя образуются кристаллы солей в солевых озерах, а также агрегаты кальцита в виде сталактитов и сталагмитов в карстовых пещерах. В последнем случае мы имеем в основном снижение растворимости карбоната кальция за счет ухода из раствора углекислого газа.
В устройствах, предназначенных для промышленного выращивания кристаллов, используется активное термостатирование, а конденсат собирается и периодически с нужной скоростью выводится из кристаллизатора. Эти варианты кристаллизаторов носят название испарительных с регулируемым отбором. Трудности оценки необходимой скорости отбора растворителя для поддержания постоянного пересыщения в отсутствие датчика пересыщения здесь остаются теми же, что и в других вариантах метода.
Прибор, описанный В. Ф. Парвовым [1964], обеспечивает динамический режим роста и возможность плавной регулировки скорости испарения растворителя. Заметим только, что на рисунке в этой статье водосборное кольцо имеет одинаковую высоту внутреннего и внешнего краев. Чтобы избежать перелива конденсата наружу, внутренний край кольца должен быть несколько ниже внешнего. Способ кристаллизации при регулируемом испарении растворителя, примененный для вещества с обратной зависимостью растворимости от температуры (Li2S04*H20), описан В.Н. Непомнящей и др. [1961]. Там же даны способ вращения кристалла при его росте, а также удобная методика выращивания кристаллов в формах. Нужно отметить, что добавление раствора в кристаллизатор, описанное в этой статье, переводит данный способ выращивания в число стационарных методов получения кристаллов.
Дата добавления: 2016-09-20; просмотров: 5121;
