Рівновага при адсорбції, типи ізотерм адсорбції, кінетичні закономірності адсорбції. Методи регенерації адсорбентів
Поглинальна або адсорбційна здатність (величина адсорбції, активність, ємність) адсорбентів виражається концентрацією адсорбата в масовій або об'ємній одиниці адсорбенту. Вона визначається природою поверхні адсорбенту, величиною і характером його пористості, температурою процесу, властивостями адсорбтива, його концентрацією в навколишньому адсорбент середовищі. Процес адсорбції супроводжується виділенням тепла, у зв'язку з чим зниження температури забезпечує його реалізацію. Залежність, що характеризує зв'язок величини адсорбції (тим або іншим поглиначем) цільового компонента (при певних його концентраціях у середовищі, що очищується) в умовах рівноваги між фазами при постійній температурі, називають ізотермою адсорбції. У загальному випадку:
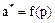 або
або 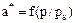 (5.71)
(5.71)
де  - парціальний тиск цільового компонента в газі, що очищується, зрівноважений з величиною його поглинання
- парціальний тиск цільового компонента в газі, що очищується, зрівноважений з величиною його поглинання 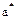 ;
;
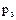 - тиск насиченої пари цільового компонента при даній температурі.
- тиск насиченої пари цільового компонента при даній температурі.
Визначені експериментально ізотерми адсорбції можуть мати досить різні форми (рисунок 5.42).
Наявність сіток (сімейств) ізотерм адсорбції для визначеного температурного інтервалу реалізації прогнозного процесу на ряді відповідних адсорбентів дає змогу здійснити обґрунтований попередній вибір оптимального з них і певною мірою охарактеризувати оптимальні умови проведення процесу.
Для математичного опису ізотерм адсорбції використовують емпіричні залежності і рівняння, виведені при деяких припущеннях на основі відповідних теоретичних моделей адсорбції.
При високих температурах або малих парціальних тисках ізотерми адсорбції апроксимуються законом Генрі:
 (5.72)
(5.72)
де  - коефіцієнт Генрі, константа фазової рівноваги.
- коефіцієнт Генрі, константа фазової рівноваги.

Рисунок 5.42 – Типи ізотерм адсорбції
1 – різко випукла; 2 – випукла; 3 – лінійна; 4 – S-подібна; 5 - увігнута
Під час практичних розрахунків для опису ізотерм адсорбції часто використовують емпіричне рівняння Фрейндліха:
 (5.73)
(5.73)
де  і
і 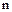 - постійні для даної температури коефіцієнти.
- постійні для даної температури коефіцієнти.
Рівновага в широкому інтервалі тисків у системах, де процес не ускладнений полімолекулярною адсорбцією, адсорбцією в мікропорах і капілярної конденсації, може бути апроксимована рівнянням ізотерми адсорбції Ленгмюра:
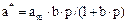 (5.74)
(5.74)
де 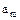 - гранична величина адсорбції (ємність моношару) при
- гранична величина адсорбції (ємність моношару) при  ;
;
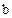 - коефіцієнт, залежний від температури.
- коефіцієнт, залежний від температури.
Згідно з потенційною теорією адсорбції на поглинаючі молекули з боку поверхні адсорбенту діє сила притягання, пропорційна адсорбційному потенціалу  . Останній виражається роботою, здійсненою адсорбційними силами при переміщенні одного моля адсорбенту із рівноваги газової фази тиском
. Останній виражається роботою, здійсненою адсорбційними силами при переміщенні одного моля адсорбенту із рівноваги газової фази тиском  на поверхню пошарово заповнюючою адсорбційною плівкою, що є сконцентрованим адсорбентом, тиск над яким дорівнює тиску насиченої пари адсорбтива
на поверхню пошарово заповнюючою адсорбційною плівкою, що є сконцентрованим адсорбентом, тиск над яким дорівнює тиску насиченої пари адсорбтива 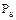 при даній температурі процесу:
при даній температурі процесу:
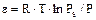 (5.75)
(5.75)
Якщо адсорбція визначається не залежними від температури дисперсійними силами взаємодії поглинаючої речовини з адсорбентом, то при постійному об'ємі  адсорбційної плівки
адсорбційної плівки
 (5.76)
(5.76)
де  - величина адсорбції, ммоль/г;
- величина адсорбції, ммоль/г;
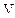 - мілімолярний об'єм нормального рідкого адсорбтива, величина
- мілімолярний об'єм нормального рідкого адсорбтива, величина  не залежить від температури.
не залежить від температури.
Звідси виходить, що так звана характеристична крива представляє величину як функцію  ;
; 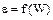 не залежить від температури.
не залежить від температури.
Кінетичні закономірності адсорбції
Адсорбційний процес складається з послідовних стадій дифузії молекул речовини, що поглинається з потоку газу до зовнішньої поверхні зерен адсорбенту (зовнішня дифузія), проникнення зовнішньої поверхні зерен, що досягла молекул усередині пористого зерна поглинача до місць сорбції (внутрішня дифузія) і власне сорбції (конденсації) молекул на внутрішній поверхні зерен. Ймовірно що остання стадія відбувається практично миттєво - протягом 10-8 – 10-9 с.
Одномірна дифузія супроводжується адсорбцією не стаціонарно. Її можна описати другим законом Фика:
 (5.77)
(5.77)
де  і
і 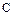 - концентрація цільового компонента відповідно у твердій і газовій фазах;
- концентрація цільового компонента відповідно у твердій і газовій фазах;
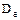 - ефективний коефіцієнт дифузії;
- ефективний коефіцієнт дифузії;
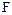 - поверхня, перпендикулярна напрямку потоку;
- поверхня, перпендикулярна напрямку потоку;
 - приватна похідна по градієнту концентрації в напрямку осі х.
- приватна похідна по градієнту концентрації в напрямку осі х.
Складність аналітичного розв'язання диференціальних рівнянь одномірної нестаціонарної дифузії обумовлює наявність відповідних співвідношень лише для гранул адсорбенту правильної геометричної форми і лінійних ізотерм адсорбції. Для сферичних гранул у формі кулі, наприклад при адсорбції з потоку газу-носія, зумовленої зовнішнім масообміном і внутрішньою дифузією, розв'язання має такий вигляд:
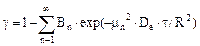 (5.78)
(5.78)
де  - ступінь відпрацювання сорбційної ємності гранул у момент часу
- ступінь відпрацювання сорбційної ємності гранул у момент часу  (час дифузії);
(час дифузії);
 і
і  - відповідно поточні та рівноважна величини адсорбції;
- відповідно поточні та рівноважна величини адсорбції;
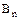 - коефіцієнти, що випливають з рівняння
- коефіцієнти, що випливають з рівняння
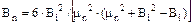 (5.79)
(5.79)
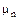 - корені характеристичного рівняння:
- корені характеристичного рівняння:
 (5.80)
(5.80)
де Ві - критерій крайової подоби Біо:  ;
;
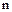 - ряд натуральних чисел;
- ряд натуральних чисел;
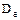 - ефективний еквівалентний коефіцієнт дифузії:
- ефективний еквівалентний коефіцієнт дифузії:  ;
;
 - коефіцієнт зовнішнього масообміну;
- коефіцієнт зовнішнього масообміну;
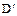 - коефіцієнт дифузії цільового компонента через шар пористого насиченого адсорбенту;
- коефіцієнт дифузії цільового компонента через шар пористого насиченого адсорбенту;
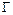 - константа Генрі (коефіцієнт адсорбції);
- константа Генрі (коефіцієнт адсорбції);
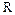 - радіус гранули.
- радіус гранули.
Значення  можна знайти в спеціальній літературі. При великій швидкості зовнішнього масообміну
можна знайти в спеціальній літературі. При великій швидкості зовнішнього масообміну 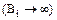 концентрації цільового компонента в потоці газу і на поверхні гранул адсорбенту близькі, тому рівняння можна записати в трохи спрощеній формі:
концентрації цільового компонента в потоці газу і на поверхні гранул адсорбенту близькі, тому рівняння можна записати в трохи спрощеній формі:
 (5.81)
(5.81)
При низькій швидкості зовнішнього масообміну 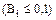 задовільну точність забезпечує рівняння:
задовільну точність забезпечує рівняння:
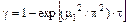 (5.82)
(5.82)
У технічних розрахунках для значення 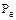 можна використати наступну наближену залежність:
можна використати наступну наближену залежність:
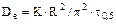 (5.83)
(5.83)
де  - коефіцієнт, значення якого визначається формою гранул адсорбенту (для кульки
- коефіцієнт, значення якого визначається формою гранул адсорбенту (для кульки  = 0,308, для циліндра з відношенням довжини до радіуса 1, 2, 4 і
= 0,308, для циліндра з відношенням довжини до радіуса 1, 2, 4 і 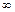 значення
значення  відповідно 0,168, 0,318, 0,45 і 0,6);
відповідно 0,168, 0,318, 0,45 і 0,6);
 - час половинного відпрацювання адсорбційної ємності поглинача.
- час половинного відпрацювання адсорбційної ємності поглинача.
Промислові адсорбенти характеризуються складною пористою структурою і працюють у різних умовах реалізації процесів газоочистки, що визначає можливість і особливості внутрішнього переносу речовини, що поглинається, за різними, часто рівнобіжними і взаємозалежними, механізмами (звичайна і кнудсенівська дифузія, дифузія по поверхні, капілярна течія й інші види переносу). У цьому зв'язку ефективні коефіцієнти дифузії, зумовлені за формулою (5.73, 5.74), хоча і можуть використовуватися для порівняльних оцінок відповідних адсорбентів, однаково є формальними характеристиками, що не розкривають механізму переносу речовини в пористих тілах. Механізм конкретного процесу визначають на основі вивчення залежностей коефіцієнтів дифузії від тиску, температури молекулярних мас речовини, що поглинається, і газу-носія та інших характеристик.
Через відносно малі концентрації шкідливих домішок у відхідних газах промисловості можна думати, що процеси їхнього адсорбційного витягу відбуваються в ізотермічних умовах. При проведенні технологічних розрахунків адсорбційних процесів газоочистки, реалізованих у стаціонарному шарі поглинача, дані з рівноваги для конкретної системи адсорбтивів (адсорбент знаходять у технічній літературі) одержують шляхом розрахунку відповідно до тієї або іншої теорії адсорбції або визначають експериментально. На їхній основі в координатах  (кг/м3; кг/кг) - С(кг/м3; кг/кг) будують рівноважну лінію процесу (ізотерму адсорбції).
(кг/м3; кг/кг) - С(кг/м3; кг/кг) будують рівноважну лінію процесу (ізотерму адсорбції).
Для побудови робочої лінії процесу необхідно розташувати величини динамічної адсорбційної ємності адсорбенту 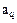 по компоненті, що добувається, для заданих концентрацій адсорбтиву на вході в адсорбер і виході з нього. Ця характеристика пов'язана з концентрацією домішки у газ що подається на очищення
по компоненті, що добувається, для заданих концентрацій адсорбтиву на вході в адсорбер і виході з нього. Ця характеристика пов'язана з концентрацією домішки у газ що подається на очищення 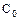 , його фіктивної (віднесеної до перетину порожнього апарата) швидкості
, його фіктивної (віднесеної до перетину порожнього апарата) швидкості  і часом захисної дії шару адсорбенту
і часом захисної дії шару адсорбенту  :
:
 (5.84)
(5.84)
Час захисної дії адсорбенту у виді шару визначеної висоти встановлюють для даної концентрації адсорбтива у газі, який подається на очищення на підставі експериментальних даних (за початковими ділянками вихідних кривих «відповідних процесів»), або розраховують за формулами одержаними на основі наближених рішень при визначених граничних умовах відповідних систем і рівнянь, що описують ту чи іншу модель адсорбції. У практиці використовують, зокрема, такі наближені розв'язання відповідно для ізотерм адсорбції ленгмюрівського і прямокутного типу:
 (5.85)
(5.85)
 (5.86)
(5.86)
де  ,
, 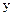 - вміст адсорбтиву в газі рівнозважений з половиною граничної величини адсорбції;
- вміст адсорбтиву в газі рівнозважений з половиною граничної величини адсорбції;
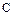 - концентрація цільового компонента в газі, що виходить з адсорбера.
- концентрація цільового компонента в газі, що виходить з адсорбера.
Необхідну довжину (висота) шару поглинача 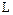 може бути розрахована з допомогою загального рівняння масопередачі:
може бути розрахована з допомогою загального рівняння масопередачі:
 (5.87)
(5.87)
Із рівняння (5.87) висота шару визначається за формулою:
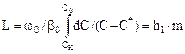 (5.88)
(5.88)
де  - висота шару адсорбенту, еквівалентна одиниці переносу;
- висота шару адсорбенту, еквівалентна одиниці переносу;
 — число одиниць переносу.
— число одиниць переносу.
Зважаючи на те, що залежність 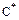 від
від  різна для кожної конкретної системи поглинача речовини-адсорбенту, інтеграл рівняння (5.88), який виражає число одиниць переносу, не може бути знайдений аналітично. Для його обчислення можуть бути використані або метод графічного інтегрування, або метод графічної побудови ступенів зміни концентрації.
різна для кожної конкретної системи поглинача речовини-адсорбенту, інтеграл рівняння (5.88), який виражає число одиниць переносу, не може бути знайдений аналітично. Для його обчислення можуть бути використані або метод графічного інтегрування, або метод графічної побудови ступенів зміни концентрації.
Розрахункові задачі звичайно передбачають наявність числових значень коефіцієнтів масопередачі. Величини останніх і їх залежність від основних параметрів відповідних процесів надходять дослідницьким шляхом.
Площу поперечного перерізу адсорбера 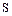 визначають із рівняння витрат:
визначають із рівняння витрат:
 (5.89)
(5.89)
де 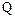 - об'ємна витрата газу, який очищують.
- об'ємна витрата газу, який очищують.
Для циліндричного адсорбера із суцільним стаціонарним шаром адсорбер  , і це дорівнює:
, і це дорівнює:
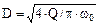 (5.90)
(5.90)
Десорбція поглинених домішок
Необхідність періодичної регенерації насичених цільовими компонентами поглиначів визначає циклічність адсорбційних процесів. Серед операцій (стадій), основна мета яких відновлення сорбційної здатності адсорбентів, ключовою є десорбція у зв'язку з тим, що для її проведення потрібно від 40 до 70 % загальних витрат із адсорбційної газоочистки. Цей процес проводять, використовуючи в основному підвищення температури, витиснення адсорбата кращою сорбуючою речовиною, зниження тиску (у тому числі створення вакууму) або комбінацію цих прийомів. Можливість ефективного здійснення десорбції в ряді випадків визначає доцільність вибору адсорбції серед інших прийомів газоочистки.
Термічну десорбцію реалізують, нагріваючи насичений адсорбент до певної температури, яка забезпечує прийнятну інтенсивність процесу, прямим контактом з потоком водяної пари, гарячого повітря або інертного газу, чи проводячи нагрівання через стінку з подачею в апарат деякої кількості віддувного агента (звичайно інертного газу). Температурний потенціал в області 100-200 °С звичайно забезпечує можливість десорбції цільових компонентів, поглинених активованим вугіллям, силікагелями й алюмогелями. Область температур від 200 до 400 °С здебільшого достатня для десорбції домішок, поглинених цеолітами.
Для випадку десорбції летких розчинників з нерухомого шару активованого вугілля (зокрема, при допущенні ізотермічності процесу через маловажність десорбції під час розігріву вугілля до 100 °С і відносно недовготривалому часі розігріву адсорбенту стосовно загальної тривалості стадії десорбції) математичний опис процесу має такий вигляд:
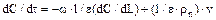 , (5.91)
, (5.91)

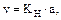
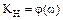 (5.92)
(5.92)
де 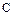 - концентрація цільового компонента десорбуючого агента;
- концентрація цільового компонента десорбуючого агента;
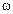 - фіктивна швидкість десорбуючого агента;
- фіктивна швидкість десорбуючого агента;
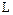 - висота шару адсорбенту;
- висота шару адсорбенту;
 - пористість шару;
- пористість шару;
 - щільність парової фази;
- щільність парової фази;
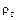 - уявна щільність адсорбенту;
- уявна щільність адсорбенту;
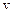 — швидкість десорбції;
— швидкість десорбції;
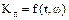 - константа наявної швидкості десорбції.
- константа наявної швидкості десорбції.
Розв'язання системи рівнянь (5.93) щодо часу десорбції 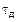 цільових компонентів при відповідних початкових і граничних умовах приводить до виразу:
цільових компонентів при відповідних початкових і граничних умовах приводить до виразу:
 (5.93)
(5.93)
де  і
і  - відповідно початкова і поточна величини адсорбції.
- відповідно початкова і поточна величини адсорбції.
Величина  , яка входить до рівняння, істотно залежить від середньої швидкості десорбуючого агента і може бути знайдена експериментальним шляхом.
, яка входить до рівняння, істотно залежить від середньої швидкості десорбуючого агента і може бути знайдена експериментальним шляхом.
Витискувана десорбція, яку називають також холодною, основується на різниці сорбуючості цільового компонента і речовини, використаної як витискувач (десорбента). Для десорбції поглинаючих адсорбентом органічних речовин можна використати діоксид вуглецю, аміак, воду, деякі органічні та інші речовини, здатні забезпечити ефективне витиснення цільового компонента і відносну простоту наступної десорбції з адсорбенту. Перспективним є застосування цього методу десорбції - під час організації адсорбційних процесів на основі використання цеолітів, які характеризуються підвищеною адсорбційною активністю щодо пари води, що визначає її ефективність як десорбенту поглинених цеолітами речовин.
Десорбція зниженням тиску може бути реалізована в двох варіантах: редукуванням тиску в системі після насичення поглинача у проведеній під надлишковим тиском стадії адсорбції або створенням у ній розрідження при здійсненні стадії адсорбції під нормальним тиском.
Вакуумна десорбція через необхідність значних енерговитрат і забезпечення герметичності відповідних установок вкрай обмежено використовується у практиці санітарної газоочистки. Принцип десорбції, заснований на перепаді тиску між стадіями адсорбції і десорбції, 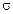 знайшов практичне втілення в установках коротко циклової безнагрівної адсорбції, які широко застосовуються для осушування повітря й інших газів. Осушування газів у ряді випадків є необхідним ступенем перед їхнім очищенням від шкідливих домішок.
знайшов практичне втілення в установках коротко циклової безнагрівної адсорбції, які широко застосовуються для осушування повітря й інших газів. Осушування газів у ряді випадків є необхідним ступенем перед їхнім очищенням від шкідливих домішок.
Методи інженерного розрахунку процесів десорбції, що основані на зниженні тиску в системі виділення з адсорбентів цільових компонентів, викладені в спеціальній літературі.
Дата добавления: 2016-03-27; просмотров: 3120;
