Раздел 6. Расслаивание фаз и потери цветных металлов в пирометаллургических процессах
.
Потери цветных металлов со шлаками
Пирометаллургическое производство цветных металлов характеризуется высоким выходом шлаков по отношению к выплавляемому металлу. Иногда при плавке количество шлаков в десятки раз превышает выход ценных промпродуктов, в которых концентрируются металлы. Поэтому, несмотря на относительно невысокие концентрации ценных компонентов в шлаках потери цветных металлов со шлаками в целом достаточно высоки.
При решении сложной задачи снижения потерь цветных металлов с промышленными шлаками важно знать, в каких формах находятся цветные металлы в жидких промышленных шлаках, и какие факторы наиболее существенно влияют на закономерности распределения цветных металлов между фазами в пирометаллургических процессах.
Традиционно формы нахождения цветных металлов в жидких промышленных шлаках принято подразделять на три вида:
химические,
физические и
механические.
1. Химические потери связаны с протеканием в процессе окислительно-восстановительных и обменных реакций с образованием оксидов цветных металлов. Например:
[Me] + 1/2O2 = (MeO)
[Me] + CO2 = (MeO) + CO
[Me] + H2O = (MeO) + H2
[MeS] + (FeO) = (MeO) + [FeS]
Образующиеся оксиды цветных металлов концентрируются в шлаке в виде раствора. Величина потерь цветных металлов в растворенной форме (aMeO) в этом случае определяется термодинамикой реакции. В промышленных условиях реакции могут не доходить до равновесия и доля химических потерь может быть выше равновесных значений (в первичных шлаковых расплавах растворимость цветных металлов как правило повышена).
2. Физические потери связаны с растворением в шлаке сульфидов или металлов и определяются законами распределения вещества между двумя несмешивающимися фазами.
[MeS] = (MeS)
[Me] = (Me)
Первый и второй вид потерь отличаются друг от друга лишь механизмом перехода металлов через межфазную границу (металл-шлак или штейн-шлак). В обоих случаях цветные металлы в шлаке находятся в виде раствора. Согласно ионной теории строения шлаков металл в обоих случаях должен находиться в шлаке в растворенном состоянии в виде ионов. Возможность существования металла в шлаке в виде атома (6) маловероятна для случая железистых шлаков цветной металлургии.
Химические и физические потери металлов со шлаками можно объеденить в единую группу - электрохимические потери, к которым будем относить металлы, находящиеся в шлаке в растворе в виде ионов.
3. Механические потери имеют место при неполном разделении фаз и возникают вследствие запутывания в шлаке мельчайших капель штейна или металла.
Электрохимические (или растворенные) потери цветных металлов со шлаками
Одним из важнейших факторов, определяющих переход цветных металлов в шлак в растворенном состоянии, является газовая атмосфера промышленных агрегатов. Действительно, равновесие реакций вполне очевидно связано с составом газовой фазы и зависит от парциальных давлений pO2, pCO2, pCO, pH2O, pH2. С увеличением pO2, pCO2 и pH2O активность оксида металла в шлаке (при прочих равных условиях) а, значит, и его концентрация будут увеличиваться.
Кроме того, все шлаки цветной металлургии представляют собой железистые расплавы. При повышении pO2 системы в шлаке повышается содержание иона трехвалентного железа Fe3+ или магнетита Fe3O4, что приводит к взаимодействию высших окислов железа с сульфидами железа и цветных металлов по суммарной реакции:
3Fe3O4 +MeS = (MeO) + 3FeO +SO2
Таким образом, возрастание парциального давления кислорода в газовой фазе приводит одновременно к увеличению содержания Fe3+ и Me2+ в шлаке.
На величину электрохимических потерь непосредственное влияние оказывает и такой фактор как температура. Влияние температуры обусловлено двумя основными причинами:
1. Температура, как известно, влияет на величину константы равновесия и в частности на Kp реакций и таким образом влияет на величину активности оксида и концентрацию цветного металла в шлаке.
2. Изменение температуры меняет и величину физической растворимости металлов в шлаках (реакции).
Так константа равновесия реакции восстановления оксида свинца
PbO +CO = Pb + CO2
с ростом температуры заметно снижается, что приводит к повышению содержания электрохимических потерь свинца в шлаке с увеличением температуры.
Величина константы равновесия обменной реакции:
(FeO) + [MeS] = (MeO) + [FeS]
для меди, никеля и кобальта также увеличивается с ростом температуры, что приводит к увеличению потерь этих цветных металлов со шлаками.
В целом можно отметить, что повышение температуры способствует увеличению содержания растворенных цветных металлов в шлаке.
Сильное влияние на величину растворенных потерь металлов в промышленных шлаках оказывает также содержание цветных металлов в штейновой или металлической фазе. С увеличением концентрации цветных металлов в штейне или металле соответственно растет их активность в этих фазах, что согласно приведенным выше уравнениям должно приводить к увеличению и активности оксида металла в шлаке.
Так для медных штейнов зависимость содержания растворенной меди в шлаках от состава штейна будет выглядеть следующим образом
Чуть более подробно остановимся на этой зависимости. При содержании меди в штейне до ~55-65 % и неизменности состава шлака содержание меди в шлаке почти монотонно увеличивается до ~0.6%. При дальнейшем увеличении концентрации меди в штейне наблюдается резкий рост содержания меди в шлаке. Принципиально, такой ход зависимости становится понятным, если обратиться к обменной реакции.
В области бедных штейнов определяющее значение играет увеличение содержания и активности Cu2S в штейне, которое увеличивается в этом диапазоне составов в десятки раз. Содержание и активность сульфида железа в области бедных штейнов снижается, однако относительная величина этих изменений незначительна по сравнению с изменениями сульфида меди.
В области рядовых штейнов ~от 30 до 60% величина (Cu) растет в результате одновременного увеличения aCu2S и снижения aFeS. При этом "темпы" роста активности сульфида меди снижаются, а "темпы" снижения активности сульфида железа увеличиваются.
На богатых штейнах (более 60% [Cu]) определяющую роль играет резкое падение концентрации и активности сульфида железа в штейне, приводящее согласно уравнению (9) к резкому увеличению активности и соответственно концентрации оксида металла в шлаке.
Итак, чем богаче штейн - тем выше электрохимические потери цветных металлов.
Большое влияние на содержание растворенных цветных металлов в шлаке оказывает состав шлака. Снова обращаясь к обменной реакции сульфида железа и окисла цветного металла, отметим, что при прочих равных условиях, повышение концентрации окислов железа как это следует из уравнения константы равновесия должно привести к смещению равновесия в сторону увеличения перехода цветных металлов в шлак. Кроме того, повышение концентрации FeO в шлаке ведет к увеличению содержания в шлаке магнетита и согласно реакции к росту оксидных потерь меди со шлаками.
Если в контакте с железосиликтными расплавами находятся не сульфиды (штейны), а черновой металл, то повышение содержания растворенных металлов с увеличением в шлаке концентрации окислов железа может быть объяснено развитием реакции:
[Me] + (Fe3O4) = (MeO) + 3(FeO)
Механические потери металлов со шлаками
Доля механических потерь во многих металлургических процессах весьма значительна и в ряде случаев достигает 60-70 % от общего количества потерь цветных металлов со шлаками. Механические потери представлены каплями металла или штейна различной крупности, которые не успели из шлаковой фазы в донную (штейн или металл) за время пребывания расплавов в металлургическом агрегате. Размер таких капель в промышленных шлаках колеблется в пределах от 0.5 мкм до 0.2 мм. Основная масса имеет размеры 10-100 мкм.
Согласно формуле Стокса (с поправками Адамара и Рыбчинсконо для случая осаждения жидких капель в жидкости), скорость осаждения капли определяется:
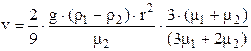
где v - скорость осаждения капли, см/с;
g - ускорение свободного падения, см/с2;
ρ1 и ρ2 - соответственно плотность более и менее плотной жидкости, г/см3;
µ1 и µ2 - вязкость более плотной и менее плотной жидкости, П;
r - радиус осаждающейся капли, см.
Так, например, при средних значениях физико-химических характеристик шлака и штейна время осаждения штейновых капель различной крупности на глубину 50 см составит:
| Крупность, мм | 0,5 | 0,2 | 0,1 | 0,05 | 0,02 | 0,01 | |
| Время осажд. | 1,7 мин. | 6,8 мин. | 42,5 мин. | 2,7 часа | 11,5 часов | 2,9 сут. | 11,6 сут. |
Время нахождения расплава в отражательных и электропечах не превышает 2-2,5 часов и основное количество капель крупнее 0,1 мм успевают отсесть из шлака в донную фазу, а более мелкие капли останутся в шлаке во взвешенном состоянии и удалятся вместе со шлаком. Возрастание вязкости шлака, снижение разности плотностей шлака и штейна и увеличение глубины шлаковой ванны затрудняют осаждение капель, повышают верхний предел и таким образом общее количество капель штейна, запутавшихся в шлаке, т.е. увеличивают механические потери цветных металлов со шлаками.
Рассмотрим причины, вызывающие диспергирование штейна или металла в шлаковом расплаве:
1. Мелкая вкрапленность и низкая концентрация сульфидов или окислов цветных металлов в исходном сырье. Мельчайшие частицы сульфидов или металлов, содержащихся в сырье, могут не иметь достаточно благоприятных условий для укрупнения в пирометаллургическом процесс, поэтому часть из них сохраняется в шлаке в мелкодисперсном состоянии.
Мелкая вкрапленность сульфидов или металлов может образоваться в процессе восстановления или сульфидирования бедных руд.
2. Чередование по времени или в разных частях аппарата процессов восстановления и окисления расплава или процессов его окисления и сульфидирования. Например, в процессе конвертирования в зоне фокуса парциальное давление кислорода в газовой струе высокое. Это приводит к окислению сульфидов, растворению в них окислов до предела насыщения и расслоения системы на сульфидно-металлическую и оксидно-сульфидную жидкость. При высоком pO2 и температуре в оксидно-сульфидной жидкости растворяется значительное количество цветных металлов. Затем обогащенная цветными металлами оксидно-сульфидная жидкость в результате перемешивания газами выносится в верхние или боковые слои расплава, где pO2 значительно ниже, чем в дутьевом факеле (весь кислород уже израсходован). В этой зоне также более низкая температура и имеется кремнезем, добавляемый в шлак в качестве флюса. Растворение кремнезема в оксидно-сульфидной жидкости и частичное восстановление магнетита сопровождается резким снижением растворимости цветных металлов и выпадением их в виде сульфидов или металла вплоть до установления нового равновесия. Этот процесс протекает по всему объему гомогенного расплава, что приводит к образованию очень мелких капель штейна в шлаке.
3. Смачивание и растекание по порам и трещинам твердых окислов жидких сульфидных материалов. Сульфидные минералы имеют более низкую температуру плавления, чем пустая порода (представленная оксидами). Как правило, жидкие сульфиды хорошо смачивают оксиды, особенно железа, цинка и марганца и за счет этого они проникают в мельчайшие капилляры и трещины оксидной фазы. После расплавления всей массы капилляры и трещины оксидной фазы закрываются, что ведет к разрыву непрерывной тонкой пленки сульфидов и образованию отдельных капель штейна, взвешенных в шлаке. Крупные капли успевают отсесть в донную фазу, а мелкие остаются во взвешенном состоянии.
4. В случае плавления веществ с высокой упругостью паров в зоне высоких температур будет происходить возгонка, а в зоне низких конденсация веществ, содержащих цветные металлы. Это существенно лишь для некоторых металлов и их соединений, характеризующихся высокой летучестью - Pb, Zn, Sb и др.
5. В некоторых случаях определенное значение в увеличении механических потерь будет иметь газовая флотация в расплавах.
Некоторые пирометаллургические реакции, например взаимодействие магнетита (Fe3O4) с сульфидом железа, сопровождаются образованием газовых пузырьков на границе штейн-шлак. К этим пузырькам под действием поверхностных сил прилипающих капельки штейна. Если подъемная сила газовых пузырей больше веса капель штейна, то прилипшие к газовому пузырьку капли штейна будут выноситься на поверхность и далее удаляться из плавильного агрегата вместе со шлаком.
Для уменьшения доли механических потерь необходимо осуществлять мероприятия, направленные на ослабление действия вышеперечисленных причин, вызывающих эмульгирование штейна в шлаке. Однако, на практике это осуществить бывает достаточно сложно. В большинстве случаев более простым оказывается путь снижения уже образовавшихся механических потерь в ходе плавки.
Снижению механических потерь цветных металлов со шлаками будут способствовать:
1. Снижение вязкости шлака
2. Увеличение разности плотностей штейна и шлака
3. Уменьшение высоты слоя шлака в металлургическом агрегате в случаях, если расслаивание фаз производится простым отстаиванием.
4. Увеличение размеров капель штейна или металла в шлаковом расплаве путем их принудительного слияния - коалесценции.
Использование последнего фактора с целью снижения потерь металлов со шлаком особенно эффективно, поскольку радиус частицы входит в формулу Стокса в квадрате.
На скорость коалесценции капель влияют различные факторы. Важнейшими из них являются межфазное натяжение на границе штейн-шлак и принудительное турбулентное перемешивание шлака и штейна.
Межфазное натяжение - способствует образованию более крупных зародышей новой фазы, их более быстрому росту и облегчает условия коалесценции капель.
Принудительное турбулентное перемешивание способствует резкому увеличению вероятности встречи капель штейна и таким образом их взаимному слиянию (коалесценции) в более крупные. Перемешивание шлака с извлекающей фазой (штейном или металлом) наиболее эффективный прием снижения количества мелких и мельчайших частиц штейна в шлаке. Без дополнительной извлекающей фазы эффективность использования перемешивания снижается, поскольку мелкие капли штейна (при перемешивании не очень богатого шлака) двигаются относительно шлака (и относительно друг друга соответственно) очень медленно и вероятность их встречи между собой и коалесценции невелика.
Роль интенсивного перемешивания шлакового расплава в снижении механических потерь наглядно видна на примере процесса Ванюкова. В ПВ за счет интенсивного перемешивания шлако-штейновой эмульсии в надфурменной зоне доля механических потерь предельно низка и в отлаженных режимах плавки не превышает 5-10% от общих потерь цветных металлов со шлаками, в то время как во всех других процессах она значительно выше.
* Гаусс сумел аналитически вывести формулу для зависимости высоты "очень большой" капли от поверхностного натяжения.
Дата добавления: 2016-02-09; просмотров: 3061;
