Тезисы лекции
Болезни органов пищеварительного тракта отличаются многообразием своих клинических и морфологических признаков. Они включают самостоятельные первичные заболевания, которые изучает наука, имеющая названия гастроэнтерология, а также другие, вторичные, которые являются проявлением ряда заболеваний инфекционной и неинфекционной природы, приобретенного или наследственного происхождения. В основе этих заболеваний могут лежать различные общепатологические процессы, такие как альтерация, воспаление, гипер- и диспластические процессы, аутоиммунные нарушения и, наконец, опухоли.
ВОСПАЛИТЕЛЬНЫЕ ЗАБОЛЕВАНИЯ ЖЕЛУДКА
Воспалительные процессы в желудке, обозначаемые гастрит (от греч. gaster – желудок), так же как и в других органах, могут быть по течению острыми и хроническими. Патогенез хронического гастрита сложен. Еще недавно считалось, что при одной из форм хронического гастрита – типе А, наблюдаются аутоиммунные реакции, а при второй форме (не иммунного гастрита типа В) воспаление возникает в результате длительного воздействия различных неспецифических раздражителей, таких как экзогенные (например, горячее питьё или острые специи), или эндогенные (например, рефлюкс желчи). Сейчас доказано, что тип В хронического гастрита является ответом на бактериальную инфекцию. Из этой группы исключен гастрит, развивающийся в результате рефлюкса желчи.
ОСТРЫЙ ГАСТРИТ
Острый гастрит чаще всего развивается после воздействия различных химических веществ, (например, алкоголя, недоброкачественными пищевыми продуктами) или некоторых лекарственных веществ (особенно нестероидных противовоспалительных веществ, содержащих аспирин). Эти вещества вызывают быструю эксфолиацию (слущивание) эпителиальных клеток и снижение секреции слизи, что сопровождается снижением функции защитного барьера против действия кислоты. В патогенезе данного процесса лежит снижение синтеза простагландинов. Определенную роль может играть и употребление острой, холодной или горячей пищи. Острый нейтрофильный гастрит является характерным для первичного ответа на инфекцию, вызванную Helicobacter pylori. Это состояние является временным, которое у большинства людей протекает субклинически и через 3-4 недели переходит в хронический гастрит. К развитию острого гастрита могут приводить и другие инфекции: сальмонеллы, стафилококк и др. Острый гастрит может развиться под воздействием токсических продуктов эндогенного происхождения, например, элиминативный гастрит при уремии.
По площади поражения различают:
острый диффузный гастрит;
острый очаговый гастрит.
Острый очаговый гастрит:
Фундальный
Антральный
Пилороантральный
Пилородуоденальный.
В зависимости от тяжести поражения изменения в слизистой варьируют от вазодилятации и отека lamina propria до эрозий и кровоизлияний. Эрозия – участок слизистой оболочки с частичным нарушением эпителия. Эрозии при остром гастрите обычно множественные, поэтому кровотечение из них может быть очень опасным. Однако обычно происходит быстрое (в течение 24-48 часов) заживление путем регенерации. При частых рецидивах острого гастрита может развиться хронический гастрит.
ХРОНИЧЕСКИЙ ГАСТРИТ
В настоящее время различают следующие формы хронического гастрита:
аутоиммунный хронический гастрит;
Helicobacter-ассоциированный хронический гастрит;
химический (рефлюкс-) гастрит;
другие формы гастрита.
Аутоиммунный хронический гастрит
У больных с данным типом хронического гастрита в крови обнаруживаются антитела против париетальных клеток желудка и против рецепторов к внешнему фактору Кастла. У этих больных наблюдается гипохлоргидрия, вплоть до анхлоргидрии, и В12-дефицитная анемия. Ассоциация аутоиммунного гастрита с макроцитарной анемией называется пернициозной анемией.
Чаще поражается тело желудка (фундальный гастрит): наблюдается повреждение специализированных париетальных (обкладочных) клеток (атрофия желез) и замена lamina propria фиброзной тканью, инфильтрация лимфоцитами и плазматическими клетками. Слизистая оболочка антрального отдела желудка остается не поврежденной. В некоторых местах покровно-ямочного эпителия фундального отдела желудка может наблюдаться кишечная метаплазия. При данном типе метаплазии продуцирующие слизь клетки замещаются бокаловидными клетками, содержащими кислые гликопротеины. В тяжелых случаях могут появляться всасывающие клетки и клетки Панета. Данная метаплазия является предопухолевым состоянием.
Helicobacter-ассоциированный хронический гастрит
Наиболее частой причиной хронического гастрита является инфекция Helicobacter pylori. Этот микроорганизм является грам-негативным, заселяет наиболее защищенное пространство, расположенное вблизи поверхности эпителия под слизистым барьером, где рН является нейтральной. Helicobacter pylori повреждает поверхностные клетки, что приводит к ускорению десквамации клеток и инфильтрации слизистой желудка полиморфноядерными лейкоцитами и клетками хронического воспаления. Helicobacter pylori обнаруживается в 90% случаев при активизации хронического гастрита типа В, но никогда не обнаруживается при типе А. Helicobacter pylori никогда не обнаруживается в слизистой оболочке 12-перстной кишки и не вызывает кишечной метаплазии.
Острый воспалительный ответ, вызываемый Helicobacter pylori, развивается в результате действия:
- компонентов комплемента, которые являются хемотаксичными для полиморфноядерных лейкоцитов;
- низкомолекулярного хемотаксического фактора, выделяемого бактериями;
интерлейкина-8, который секретируется эпителиальными клетками, макрофагами и эндотелиальными клетками. Полиморфноядерные лейкоциты выделяют протеазы и активные кислородосодержащие метаболиты, которые вызывают атрофию желез. В lamina propria обнаруживаются плазматические клетки, синтезирующие IgA, IgG и IgM против данного микроорганизма.
При Helicobacter-ассоциированном хроническом гастрите поражается весь желудок. Однако это поражение неравномерно. У большинства больных в процесс вовлекается антральный отдел и тело, в которых постепенно развиваются атрофия желез, фиброзирование и кишечная метаплазия. У больных с данной локализацией процесса увеличивается риск развития язв и опухолей желудка. Вторым типом изменений является воспаление, в основном, в антральном отделе без поражения тела желудка. У данных больных наблюдается повышенная кислотность желудочного сока, что увеличивает риск развития дуоденальных язв.
Химический (рефлюкс-) гастрит
При регургитации желчи и щелочного дуоденального сока в желудок происходит усиленная десквамация эпителия, компенсаторная гиперплазия пролиферирующих клеток в дне желудочных ямок, вазодилятация и отек lamina propria, что и является проявлением рефлюкс-гастрита. Рефлюкс-гастрит наиболее часто наблюдается:
у больных после операций, повреждающих пилорус;
как результат нарушения моторики кишечника при желчекаменной болезни и после холецистэктомии;
у больных с нарушением антро-дуоденальной моторики, которое может быть как первичным, так и вторичным в результате патологического ответа на гормоны, такие как холецистокинин и секретин, которые в норме увеличивают тонус пилоруса при повышении кислотности в 12-перстной кишке.
При рефлюкс-гастрите клетки антрального отдела желудка начинают усиленно секретировать гастрин, который блокирует действие холецистокинина и секретина на мышечные волокна пилоруса.
При длительном существовании рефлюкс-гастрита возможно образование язв.
Отдельно выделяют следующие типы хронического гастрита:
лимфоцитарный;
эозинофильный;
гранулематозный.
При лимфоцитарном гастрите основным гистологическим проявлением является наличие многочисленных зрелых лимфоцитов в поверхностных слоях эпителия. Эта форма иногда обнаруживается у больных со специфическими эрозиями, идущими вдоль увеличенных складок слизистой. Этиология и взаимоотношения с Helicobacter-ассоциированным гастритом не установлены.
Эозинофильный гастрит характеризуется отеком слизистой и наличием многочисленных эозинофилов в воспалительном инфильтрате. Предполагается, что эозинофильный гастрит – это аллергический ответ на пищевой антиген, к которому больной сенсибилизирован.
Гранулематозный гастрит – это редкая форма гастрита, при котором формируются эпителиоидно-клеточные гранулемы. Эти гранулемы могут быть проявлением болезни Крона или саркоидоза, однако в редких случаях он бывает криптогенным.
АППЕНДИЦИТ
Аппендицит – первичное воспаление червеобразного отростка слепой кишки со своеобразным клиническим синдромом.
Различают две клинико-анатомические формы аппендицита: острую и хроническую.
Острый аппендицит встречается во всех возрастных группах, однако наиболее часто – у подростков.
Причинами острого аппендицита являются обструкция просвета аппендикса фекалитом или увеличенной подслизистой оболочки в результате лимфоидной гиперплазии, а также при перегибе аппендикса. При этом в дистальном отрезке происходит усиленное размножение микроорганизмов, таких как Escherichia coli, Streptococcus faecalis и анаэробных бактерий. Эти бактерии затем проникают в слизистую и другие оболочки аппендикса, вызывая острое воспаление.
Патоморфологические изменения. Принято различать следующие основные морфологические формы острого аппендицита:
простой;
поверхностный;
деструктивный (который в свою очередь делят на флегмонозный, апостематозный, флегмонозно-язвенный, гангренозный).
Все эти формы, в сущности, являются морфологическим отражением фаз острого воспалительного процесса в аппендиксе, которое, в конечном счете, завершается некрозом. Длительность этого процесса 2-4 дня.
Для острого простого аппендицита характерно наличие стаза в капиллярах и венулах, отек, кровоизлияния, краевое стояние лейкоцитов, лейкодиапедез чаще всего в дистальном отделе аппендикса. Внешне аппендикс выглядит нормальным, однако, диагноз подтверждается при гистологическом исследовании.
Острый поверхностный аппендицит характеризуется наличием в дистальном отделе фокуса экссудативного гнойного воспаления в слизистой оболочке, обозначаемого как первичный аффект.
Изменения, свойственные простому или поверхностному аппендициту, могут быть обратимыми. Однако, как правило, они прогрессируют, и развивается деструктивный аппендицит.
К концу первых суток лейкоцитарный инфильтрат (преобладают нейтрофилы) распространяется на всю толщу стенки отростка (флегмонозный аппендицит). Макроскопически воспаленный аппендикс выглядит отечным и красным, его поверхность часто покрыта фибринозно-гнойным экссудатом. Иногда на этом фоне выявляются мелкие множественные гнойники, в таком случае такой аппендицит обозначают как аппостематозный. Острое воспаление слизистой оболочки приводит к образованию язв и воспалению мышечного слоя – это флегмонозно-язвенный аппендицит. Завершаются гнойно-деструктивные изменения развитием гангренозного аппендицита. Отросток при этой форме утолщен, стенка его серо-грязного цвета, бесструктурная со зловонным запахом, из просвета выделяется гной. Микроскопически имеют место обширные очаги некроза с колониями микробов, кровоизлияния, тромбы в сосудах. Слизистая оболочка практически на всем протяжении десквамирована.
Осложнения. Местное распространение воспалительного процесса может привести к вовлечению периаппендикулярных тканей, что проявляется развитием “аппендикулярного инфильтрата” или абсцесса. В результате перфорации может развиться перитонит. Могут также образоваться отдаленные абсцессы (например, в прямокишечно-пузырном и поддиафрагмальном пространствах). Очень редко наблюдается распространение воспаления по венам, что приводит к развитию тромбофлебита портальной вены с формированием множественных пилефлебитических абсцессов печени.
Хронический аппендицит характеризуется наличием склеротических и атрофических процессов, на фоне которых могут быть выявлены признаки воспалительно-деструктивных изменений. Возникают спайки с окружающими тканями. При рубцовой облитерации проксимального отдела в просвете червеобразного отростка может накапливаться серозная жидкость и образуется киста – водянка отростка. Если содержимое кисты представлено слизью, такое осложнение обозначают как мукоцеле. При разрыве такой кисты и попадании содержимого в брюшную полость возможна имплантация клеток на брюшине и развитии образований, напоминающих опухоль – псевдомиксома брюшины.
НЕСПЕЦИФИЧЕСКИЙ ЯЗВЕННЫЙ КОЛИТ
Неспецифический язвенный колит (НЯК) является основной причиной диарреи с примесью крови, слизи и гноя. НЯК является неспецифическим воспалительным заболеванием толстой кишки, развивающегося обычно в прямой кишке и распространяющегося затем проксимально. В отличие от болезни Крона, при НЯК поражается только толстая кишка. Поражение терминального отрезка подвздошной кишки наблюдается редко и возникает из-за развития несостоятельности илиоцекального клапана, а не является непосредственным поражением.
Этиология. Географическое распространение болезни такое же, как и при болезни Крона. Заболеваемость в западной Европе и США составляет 12-140 на 100000.
Предполагается, что имеется четкая генетическая предрасположенность к язвенному колиту; этот генетический дефект может воздействовать как на иммунный ответ, так и на структуру слизистой кишки. Предполагается, что при язвенном колите большую роль играют гены HLA-DR2 и некоторых цитокинов. Наблюдается повышение синтеза IgG2 по сравнению с IgG1. Обнаруживается повышение проницаемости слизистой оболочки и изменение состава гликопротеинов слизи. Генетическая предрасположенность подтверждается исследованиями гомозиготных близнецов, повышенной заболеваемостью определенных этнических групп и у лиц с доказанной генетической предрасположенностью к анкилозирующему спондилиту, псориазу и первичному склерозирующему холангиту.
Сейчас появляются сведения, что НЯК развивается в результате аутоиммунных процессов, а повреждение слизистой происходит в результате неадекватной активации Т-клеток и опосредованного повреждения цитокинами, протеазами и кислородными радикалами, синтезируемыми макрофагами и нейтрофилами. Подтверждением аутоиммунного процесса является наличие аутореактивных Т-клеток и аутоантител против эпителиальных клеток кишечника и антинейтрофильных цитоплазматических аутоантител (ANCA). Однако эти антитела и аутореактивные лимфоциты не приводят к повреждению тканей и НЯК не признается аутоиммунным заболеванием, при котором повреждение слизистой возникает в результате прямой иммунологической реактивности на собственные антигены.
Нецелесообразная и персистирующая активация Т-клеток может лежать в основе как НЯК, так и болезни Крона. На запуск данного процесса могут оказывать значительное влияние стресс, воспаление слизистой кишки, курение.
Вне зависимости от причины доказано, что повреждение слизистой при НЯК происходит в результате накопления в слизистой полиморфноядерных лейкоцитов, которые выделяют протеазы, оксид азота и свободные радикалы. Увеличенная проницаемость и абсорбция бактериальных антигенов лежит в основе иммунокомплексных повреждений и некоторых внекишечных осложнений.
Морфология. При НЯК наблюдается последовательный и непрерывный тип поражения. Обычно первоначально поражение возникает в прямой кишке, где наблюдается максимальная выраженность изменений, а затем распространяется на сигмовидную и ободочную кишку (рис. 1).
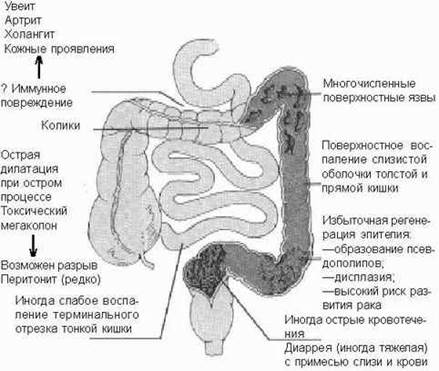
Рисунок 1. Патоморфологические изменения прямой и сигмовидной кишки при НЯК.
Язвы имеют неровные края и могут сливаться, они распространяются горизонтально на еще не поврежденные участки, образуя обширные острова поражения. Язвы поверхностные, захватывают слизистую и подслизистую оболочки, однако в тяжелых случаях могут повреждаться все слои кишки, вплоть до перфорации. В неповрежденной слизистой обнаруживается выраженная гиперемия, из язв часто возникают кровотечения.
Микроскопически определяется инфильтрация слизистой клетками острого и хронического воспаления. Полиморфноядерные лейкоциты обнаруживаются в интерстициуме, однако, в некоторых криптах они образуют агрегаты (абсцессы крипт). Развиваются широко распространенные дегенеративные изменения как поверхностных эпителиоцитов, так и в криптах, резко снижается синтез муцинов. В остром периоде может наблюдаться полная деструкция крипт. Затем начинается их регенерация, новообразованные крипты отличаются значительным расширением и часто имеют соединения с соседними криптами. Так, при биопсии прямой кишки обнаруживается атрофия и значительное расширение крипт, в которых иногда обнаруживаются признаки метаплазии эпителия. НЯК является предопухолевым заболеванием, поэтому на некоторых участках обнаруживается дисплазия эпителия.
БОЛЕЗНИ ПЕЧЕНИ
Болезни печени многообразны и могут быть первичными и вторичными (при других заболеваниях).
Благодаря широкому применению биопсии в диагностике заболеваний печени в последние годы получена возможность уточнить и дополнить наши представления о морфологических процессах, происходящих в печени на ранних этапах их развития. Это в свою очередь способствует ранней клинико-морфологической диагностике заболеваний и проведению патогенетически обоснованной терапии. В данном разделе будут рассмотрены заболевания печени, наиболее часто встречающиеся в лечебной практике болезни – гепатиты и циррозы различной этиологии. Морфология вирусного гепатита и рак печени нашли свое отражение в соответствующих главах.
ХРОНИЧЕСКИЙ ГЕПАТИТ
Хронический гепатит – это воспалительное заболевание печени, которое длится более 6 месяцев без признаков разрешения.
Этиология. Причиной хронического гепатита могут быть различные факторы. Наиболее частыми являются:
вирусы гепатита, особенно В и С;
алкоголь;
лекарственные препараты (метилдопа, оксифенизатин, галотан, изониазид, нитрофурантоин и др.);
аутоиммунные процессы;
болезнь Вильсона;
недостаточность 1-антитрипсина.
Классификация. По гистологическому принципу хронический гепатит делится на:
хронический персистирующий гепатит (ХПГ);
хронический активный гепатит (ХАГ).
Эта классификация не является чисто морфологической, т.к. каждый из этих вариантов имеет и определенное клиническое отражение: активность процесса, выраженность симптомов, прогноз. Хронический гепатит является неспецифическим проявлением многих хронических заболеваний печени. Для дифференциальной диагностики используется большое количество гистологических, лабораторных и клинических исследований, которые просуммированы в таблице 4.
Хронический персистирующий гепатит
Хронический персистирующий гепатит характеризуется:
лимфоцитарной инфильтрацией только портальных трактов;
сохранением нормальной архитектоники печени;
отсутствием или редким некрозом клеток печени;
хорошим прогнозом.
Обычно при хроническом персистирующем гепатите наблюдается излечение даже без специфического лечения. Исключение составляет ХПГ при вирусном гепатите С, при котором часто наблюдается прогрессия до ХАГ и цирроза.
Хронический активный гепатит
Хронический активный гепатит характеризуется:
пограничными (по периферии дольки на границе с портальными трактами) и мостовидными (некроз двух долек с вовлечением портального тракта, лежащего между ними) некрозами;
инфильтрацией портальных трактов и паренхимы печени;
высоким риском развития цирроза печени.
Микроскопически достоверным признаком ХАГ являются пограничные некрозы, которые являются результатом воспалительной деструкции клеток печени, расположенных рядом с воспаленным портальным трактом. Это приводит к постепенному уменьшению числа клеток в дольке и нарушении нормальной архитектоники печени. Иногда при биопсии обнаруживаются специфические признаки, указывающие на причину ХАГ: гиалин Мэллори при алкоголизме, большое количество плазмоцитов и “розеток” из набухших эпителиальных клеток при “люпоидном” нефрите.
Алкогольный гепатит
Алкоголь (этиловый спирт) является частой причиной острого и хронического повреждения печени. Поражение печени происходит в результате следующих механизмов:
клетки печени начинают извлекать энергию из более доступного источника – алкоголя, при этом останавливаются процессы окисления жирных кислот, которые являются источником энергии в норме, в результате чего они накапливаются в клетке, т.е. развивается жировая дистрофия;
алкоголь, являющийся по сути дела токсином, накапливаясь в клетке, приводит к ее повреждению, развивается воспалительная реакция вокруг погибших клеток;
алкоголь стимулирует выработку коллагена, что ведет к фиброзу, который в первую очередь наблюдается в портальных трактах и/или терминальных венулах.
Подсчитано, что алкогольный цирроз развивается при ежедневном употреблении в течение 5 лет более 120 г этилового спирта для мужчин и 90 г – для женщин.
При биопсии наблюдаются следующие изменения:
жировая дистрофия гепатоцитов;
острый гепатит с накоплением гиалина Мэллори;
нарушение архитектоники печени: портальный, а затем общий цирроз печени.
Жировая дистрофия наиболее выражена в гепатоцитах, которые расположены вокруг центральной вены. Она является неспецифическим изменением, т.к. наблюдается и при другой патологии печени. Более специфичным является накопление в гепатоцитах гиалина Мэллори, который образуется в результате накопления промежуточных филаментов. Иногда развивается острое воспаление, которое является неблагоприятным прогностическим фактором, т.к. обычно оно предвещает быстрое развитие цирроза печени.
Хронические заболевания печени, лежащие в основе хронического гепатита
К ним относятся:
перегрузка печени железом (гемохроматоз);
болезнь Вильсона (гепатолентикулярная дегенерация);
недостаточность ?1-антитрипсина;
аутоиммунные заболевания печени:
аутоиммунный (“люпоидный”) гепатит;
первичный билиарный цирроз.
Гемохроматоз
Гемохроматоз развивается в результате избыточного накопления в печени гемосидерина – богатого железом белка. Данное заболевание было достаточно хорошо рассмотрено в лекции «Смешанные дистрофии».
Аутоиммунный "люпоидный" гепатит
"Люпоидный" гепатит чаще встречается у женщин и микроскопически характеризуется наличием большого количества плазматических клеток и образованием набухшими гепатоцитами розеток. Данное состояние не имеет никакого отношения к системной красной волчанке, однако при нем также обнаруживаются антиядерные антитела. Также часто обнаруживаются антитела против гладкомышечных клеток. Также обнаруживается повышение концентрации IgG и трансаминаз в крови.
Первичный билиарный цирроз
Название данного заболевания является неточным, однако, оно все еще широко применяется. Более точным является хронический негнойный деструктивный холангит. Наиболее часто он развивается у женщин среднего возраста (90% больных – женщины, из них 75% имеют возраст 40-59 лет). Встречается заболевание довольно редко: 3,7–14,4 случаев на 100000. В патогенезе заболевания основную роль имеют антимитохондриальные антитела, которые обнаруживаются у 95% больных. Эти антитела реагируют не только с митохондриями человека, но и с таковыми некоторых микроорганизмов, например, Enterobacteriaceae, поэтому появилась гипотеза об этиологической роли и/или участии этих бактерий в патогенезе заболевания.
Заболевание развивается по следующим стадиям:
аутоиммунная деструкция эпителия желчных протоков, особенно небольших протоков, вокруг которых обнаруживаются лимфоцитарные инфильтраты и гранулемы. В поврежденных протоках наблюдается набухание выстилающего эпителия и разрывы базальной мембраны;
затем развивается холестаз, особенно в перипортальной зоне, наблюдается пролиферация небольших протоков, которые необходимы для замены разрушенных;
развиваются нарушения архитектоники печени в результате перипортального и мостовидного некроза клеток печени, на месте которых развивается фиброз;
развитие цирроза печени.
На поздних стадиях в печени также накапливается медь в результате нарушения выведения ее с желчью.
В дополнение к гистологическим изменениям наблюдаются следующие признаки заболевания:
повышение в плазме уровня щелочной фосфатазы и IgM;
антимитохондриальные антитела в плазме;
зуд кожи, желтуха и ксантелазмы;
повышение риска развития язв 12-перстной кишки в результате снижения содержания в кишке щелочных компонентов желчи;
развитие остеопороза и остеомаляции в результате нарушения всасывания витамина D из-за недостатка желчных кислот и стеатореи.
ЦИРРОЗ ПЕЧЕНИ
Печень обладает значительной регенераторной способностью, поэтому даже после обширного поражения печени может быть восстановлена нормальная архитектура и функция ее. Однако если поражение клеток повторяется многократно или возникают сильные нарушения архитектуры, например, после мостовидных некрозов, развивается цирроз печени.
Цирроз печени – заболевание неспецифическое; оно является конечной стадией заболеваний, приводящих к хроническому повреждению клеток печени. Цирроз печени – состояние нереверсивное, при нем наблюдается нарушение архитектуры печени в виде фиброза и узловой регенерации. Количество соединительной ткани резко возрастает и клетки печени не формируют ацинусы и дольки, а регенерируют в виде узелков, не имеющих правильной структуры дольки.
Классификация. Цирроз печени классифицируется по морфологическому и этилогическому принципу. По морфологическим признакам цирроз классифицируется на:
мелкоузловой – узлы до 3 мм в диаметре;
крупноузловой – узлы более 3 мм в диаметре.
Наиболее часто причиной мелкоузлового цирроза является алкоголизм. При крупноузловом циррозе, независимо от причины, наблюдается повышение риска развития рака печени.
По этиологическому принципу циррозы делятся на:
вирусный (вирусный гепатит В и С);
алкогольный;
при гемохроматозе;
аутоиммунный (“люпоидный” гепатит и первичный билиарный цирроз);
в результате обструкции желчевыводящих путей;
при болезни Вильсона.
Если выяснить причину невозможно, говорят о “криптогенном” циррозе, однако по мере развития науки все меньше случаев попадают в данную группу.
Морфологические признаки цирроза:
нарушение долькового строения печени;
дистрофия гепатоцитов (гидропическая, баллонная, жировая);
некроз гепатоцитов;
наличие узлов регенератов – ложных долек (усиление регенерации, наличие митозов и амитозов гепатоцитов);
диффузный фиброз (разрастание соединительной ткани).
Различают три морфогенетических типа цирроза:
постнекротический;
портальный;
смешанный.
Постнекротический цирроз развивается в результате массивных некрозов печеночной паренхимы. Участки некроза замещены плотной рубцовой тканью. Патогномоничным морфологическим признаком для этого цирроза является сближение портальных триад и центральных вен. Ложные дольки состоят из новообразованной печеночной ткани и содержат множество многоядерных печеночных клеток. Для гепатоцитов характерны белковые дистрофии, липиды в них обычно не выявляются. Отмечается холестаз, пролиферация холангиол. Макроскопически печень уменьшена в размерах, плотная, с крупными узлами, разделенными широкими и глубокими бороздами. Это крупноузловой цирроз. Для него характерны ранняя гепатаргия (печеночная недостаточность) и поздняя портальная гипертензия.
Портальный цирроз характеризуется однородностью микроскопической картины – тонкопетлистой соединительнотканной сетью и малой величиной ложных долек. При этом циррозе микроскопически чаще всего выявляются признаки хронического воспаления и жировая дистрофия гепатоцитов. Макроскопически печень маленькая, плотная, зернистая или мелкобугристая. Это мелкоузловой цирроз. Портальный цирроз развивается медленно (в течение многих лет), чаще всего при хроническом алкоголизме. Истинным портальным циррозом является первичный билиарный цирроз. Печень при первичном билиарном циррозе увеличена, плотная, на разрезе серо-зеленая, поверхность ее гладкая либо мелкозернистая. При вторичном билиарном циррозе, обусловленном обструкцией желчных путей камнем, опухолью, или инфекцией желчных путей и развитием халангита (холангитический цирроз), печень увеличена, плотная, зеленого цвета, на разрезе с расширенными, переполненными желчью протоками.
Смешанный цирроз обладает признаками как постнекротического, так и портального цирроза.
Внепеченочные признаки цирроза печени:
желтуха;
геморрагический синдром;
склероз воротной вены (как результат портальной гипертензии расширение и истончение порто-кавальных анастомозов);
асцит;
спленомегалия.
При развитии гепаторенального синдрома выявляется иммунокомплексный гломерулонефрит и известковые метастазы. В головном мозге дистрофические изменения нейронов.
Осложнения. Наиболее важными являются печеночная недостаточность, портальная гипертензия и печеночноклеточный рак.
В результате печеночной недостаточности наблюдается снижение синтеза альбуминов, факторов свертывания крови и других белков крови. Нарушается разрушение эндогенных продуктов, таких как гормоны, азотсодержащих веществ и т.д. Развивается энцефалопатия в результате нарушения детоксикации азотсодержащих веществ, синтезируемых бактериями в просвете кишечника; которые действуют как медиаторы (“ложные нейротрансмиттеры”) в ЦНС. Часто развивается почечная недостаточность (гепаторенальный синдром).
В результате нарушения разрушения стероидных гормонов развивается вторичный альдостеронизм, который проявляется задержкой жидкости и ионов натрия, а у мужчин исчезают вторичные половые признаки, развивается гинекомастия в результате гиперэстрогенемии. Также в результате гиперэстрогенемии развиваются “сосудистые звездочки” на коже.
Цирроз печени является наиболее распространенной причиной портальной гипертензии. При циррозе портальная гипертензия (>7 мм рт.ст.) возникает в результате комбинации следующих факторов: повышенного кровотока в портальной вене, повышенного сопротивления в сосудах печени, артерио-венозного внутрипеченочного шунтирования. В результате портальной гипертензии развивается варикозное расширение вен пищевода и геморроидальных вен, а также развивается асцит. Варикозное расширение вен пищевода является наиболее опасным осложнением, т.к. тонкие вены пищевода легко разрываются, в результате чего развивается порой фатальное кровотечение. Также характерно расширение вен на передней брюшной стенке в виде “головы медузы Горгоны”. Еще одним грозным осложнением портальной гипертензии является тромбоз портальной вены.
Цирроз печени является предопухолевым состоянием; при нем повышается риск развития печеночноклеточного рака. Опухоль часто является мультифокальной.
Литература
1. Струков А.И. Патологическая анатомия : учебник / А. И. Струков, В. В. Серов . - 5-е изд. - М., 2011. - 848 с. : ил.
2. Струков А.И. Патологическая анатомия : учебник / А. И. Струков, В. В. Серов. - 5-е изд. стереотипное. - М. : Литтерра, 2010. - 848 с. : ил
3. Повзун С.А. Патологическая анатомия в вопросах и ответах. : учебник / С. А. Повзун. - М : ГЭОТАР-Медиа, 2007. - 175 с. : ил
Дополнительная литература:
1. Тусупбекова М.М. Клиническая патоморфология : учебник / М. М. Тусупбекова . - Алматы : Эверо, 2012. - 184 с. : ил
2. Патологическая анатомия. : атлас / ред. О. В. Зайратьянц. - М : ГЭОТАР-Медиа, 2010. - 470 с. : ил
3. Маянский Д.Н.Лекции по клинической патологии : руководство / Д. Н. Маянский. - М : ГЭОТАР-Медиа, 2008. - 464 с. : ил
4. Руководство к практическим занятиям по патологической анатомии : руководство / В. В. Серов, М. А. Пальцев. - М. : Медицина, 2005/1998. - 544 с. : ил
5. Тусупбекова М.М. Морфологический атлас общепатологических процессов Алматы: Эверо, 2012
6. Пальцев М.А. Руководство по биопсийно-секционному курсу : руководство / М. А. Пальцев, В. Л. Коваленко, Н. М. Аничков. - М. : Медицина, 2004. - 256 с. : ил.
7. Серов В.В. Хазанов, А. Т. Руководство по секционному курсу [Текст] : учебник / А. Т. Хазанов, И. А. Чалисов. - 3-е изд. - М : Медицина, 1984/2002
8. Патологическая анатомия: Курс лекций /под.ред. В.В. Серова, М.А. Пальцева М: Медицина, 1998
Контрольные вопросы (обратная связь)
1.Назовите типы хронического гастрита
2. Этиологические факторы развития болезни Крона
3.Причина смерти при неспецифическом язвенном колите.
1.Тема №14: «Воздушно-капельные бактериальные инфекции. Дифтерия. Скарлатина. Кишечные бактериальные инфекции.»
2. Цель: формирование у студентов знаний о структурных основах воздушно-капельных бактериальных инфекциях, дифтерии, скарлатины, кишечных бактериальных инфекциях, морфологических проявлениях, осложнениях, исходах и дифференциальной диагностике и использовании полученных знаний в практической работе врача-стоматолога с учетом возрастных особенностей.
3. Тезисы лекции:
Инфекционные болезни до настоящего времени остаются важной проблемой. Они являются результатом взаимодействия между макро- и микроорганизмом. Инфекционные болезни отличаются от других заболеваний специфичностью, контагиозностью, цикличностью и формированием в макроорганизме постинфекционного иммунитета. Развитие инфекционного заболевания зависит от состояния макроорганизма, его восприимчивости и определяется свойствами возбудителя, такими как патогенность, вирулентность и др. Место проникновения микробов в организм получило название входных ворот инфекции. Наличие микробов в крови называется бактериемия или вирусемия. Основные группы инфекционных болезней: инфекции дыхательных путей (ОРВИ), бактериальные воздушно-капельные инфекции (дифтерия, скарлатина, менингококковая инфекция),.кишечные инфекции (шигеллёз, брюшной тиф и паратифы, сальмонеллёзы, пищевые токсикоинфекции, ботулизм, холера, вирусный гепатит); туберкулёз.
Особенности воздушно-капельных инфекций: многообразие возбудителей, воздушно-капельный путь передачи, входными воротами является слизистая оболочка дыхательных путей. Наибольшее значение имеют ОРВИ. К ним относятся грипп, парагрипп, аденовирусная и респираторно-синцитиальная инфекция. Местные изменения развиваются в верхних дыхательных путях и в лёгких, общие изменения связаны с виремией и интоксикацией и представлены воспалительными и дистрофическими изменениями внутренних органов и расстройствами циркуляции. Дифтерия – острое инфекционное заболевание, характеризующееся фибринозным воспалением в области входных ворот и общей интоксикацией. Скарлатина – заболевание стрептококковой природы, проявляется экзантемой и местными воспалительными изменениями в зеве. Менингококковая инфекция –острое инфекционное заболевание, которое проявляется в 3 основных формах: назофарингит, гнойный менингит, острейший менингококковый сепсис (менингококцемия). Кишечные инфекции – инфекционные заболевания, для которых характерны фекально-оральный путь заражения и локализация основных морфологических изменений в кишечнике. Туберкулёз – хроническое инфекционное заболевание, при котором могут поражаться все органы и ткани человека, но чаще патологический процесс развивается в лёгких. Проникновение микобактерий туберкулёза в организм происходит аэрогенным или алиментарным путём и приводит к инфицированию. В основе волнообразного хронического течения туберкулёза лежит постоянная смена иммунологических реакций. Различают три основных вида патогенетических и клинико-морфологических проявлений туберкулёза: первичный туберкулёз, гематогенный туберкулёз и вторичный туберкулёз.
Заболевания центральной нервной системы (ЦНС) чрезвычайно разнообразны. С этой патологией в своей практике регулярно сталкиваются врачи различных специальностей. Многие заболевания центральной нервной системы (ЦНС) часто заканчиваются летально либо являются причиной инвалидности пациента. Изучение болезней ЦНС необходимо врачам любого профиля для грамотной диагностики таких заболеваний и проведения патогенетически обоснованного лечения.
Заболевания ЦНС могут являться как самостоятельными нозологическими формами, так и проявлениями различных заболеваний, (например сосудистая деменция – проявление атеросклероза сосудов головного мозга).
В основе заболеваний ЦНС могут лежать дистрофические (“дегенеративные”), демиелинизирующие, воспалительные, опухолевые процессы, а также нарушения внутриутробного развития.
В этиологии болезней этой системы значительную роль могут играть различные инфекционные агенты: грибы, простейшие, бактерии, вирусы и прионы.
В неврологической практике принято делить все заболевания нервной системы на дистрофические, демиелинизирующие, метаболические, сосудистые, инфекционные, травматические повреждения, опухоли, врожденные нарушения развития.
4. Иллюстративный материал: демонстрационные таблицы, презентации, фотографии микроскопической картины патологических процессов в электронном виде.
Литература
1. Струков А.И. Патологическая анатомия : учебник / А. И. Струков, В. В. Серов . - 5-е изд. - М., 2011. - 848 с. : ил.
2. Струков А.И. Патологическая анатомия : учебник / А. И. Струков, В. В. Серов. - 5-е изд. стереотипное. - М. : Литтерра, 2010. - 848 с. : ил
3. Повзун С.А. Патологическая анатомия в вопросах и ответах. : учебник / С. А. Повзун. - М : ГЭОТАР-Медиа, 2007. - 175 с. : ил
Дополнительная литература:
1. Тусупбекова М.М. Клиническая патоморфология : учебник / М. М. Тусупбекова . - Алматы : Эверо, 2012. - 184 с. : ил
2. Патологическая анатомия. : атлас / ред. О. В. Зайратьянц. - М : ГЭОТАР-Медиа, 2010. - 470 с. : ил
3. Маянский Д.Н.Лекции по клинической патологии : руководство / Д. Н. Маянский. - М : ГЭОТАР-Медиа, 2008. - 464 с. : ил
4. Руководство к практическим занятиям по патологической анатомии : руководство / В. В. Серов, М. А. Пальцев. - М. : Медицина, 2005/1998. - 544 с. : ил
5. Тусупбекова М.М. Морфологический атлас общепатологических процессов Алматы: Эверо, 2012
6. Пальцев М.А. Руководство по биопсийно-секционному курсу : руководство / М. А. Пальцев, В. Л. Коваленко, Н. М. Аничков. - М. : Медицина, 2004. - 256 с. : ил.
7. Серов В.В. Хазанов, А. Т. Руководство по секционному курсу [Текст] : учебник / А. Т. Хазанов, И. А. Чалисов. - 3-е изд. - М : Медицина, 1984/2002
8. Патологическая анатомия: Курс лекций /под.ред. В.В. Серова, М.А. Пальцева М: Медицина, 1998
Контрольные вопросы (обратная связь)
1. Общее понятие об инфекционных болезнях, классификация.
2. Характеристика ОРВИ.
3. Процессы, лежащие в основе заболеваний ЦНС.
1.Тема №15: «Болезни мочевыделительной системы. Болезни нервной системы.»
2. Цель: формирование у студентов знаний о структурных основах болезней мочевыделительной и нервной систем, морфологических проявлениях, осложнениях, исходах и дифференциальной диагностике и использовании полученных знаний в практической работе врача-стоматолога с учетом возрастных особенностей.
3. Тезисы лекции:
Почки выполняют в организме жизненно важные функции. Заболевания почек можно разделить на две большие группы: гломерулопатии и тубулопатии.
Гломерулопатии – заболевания с первичным и преимущественным поражение клубочкового аппарата. Воспалительные гломерулопатии представлены гломерулонефритами – группой заболеваиний инфекционно-аллергической или неустановленной этиологии. Они характеризуются двусторонним негнойным воспалением клубочков с развитием почечных и внепочечных симптомов. Невоспалительные гломерулопатии представлены нефротическим синдромом. Для него характерны массивная пртеинурия, гипоальбуминемия, генерализованные отёки. Наибольшее значение среди тубулопатий имеет некротический нефроз, который клинически выражается синдромом острой почечной недостаточности.
В исходе хронических двусторонних заболеваний почек развивается хроническая почечная недостаточность. Её морфологическим субстратом является сморщивание почек – нефросклероз. Пиелонефрит – инфекционное заболевание, при котором в процесс вовлекается лоханка, чашечки, вещество почки с преимущественным поражением интерстиция. Почечно-каменная болезнь – заболевание, при котором в почечных чашечках, лоханках и мочеточниках образуются камни.
Острый гломерулонефрит
Первая из рассматриваемых групп гломерулярных заболеваний характеризуется воспалительными повреждениями почечных клубочков, а клинически — острым нефритом. У больных нефритом обычно обнаруживают гематурию, цилиндры из эритроциты в моче, азотемию, олигурию и слабую или умеренно выраженную гипертензию.
Острый постстрептококковый (пролиферативный) гломерулонефрит. Это диффузное глобальное заболевание клубочков развивается обычно через 1—4 нед после стрептококковой инфекции глотки или кожи и чаще встречается у детей в возрасте 6— 10 лет, однако могут болеть и взрослые любого возраста.
Нефритогенными являются лишь некоторые штаммы гемолитического стрептококка группы А. Постстрептококковый гломерулонефрит — иммунологический обусловленное заболевание.
Схема 18.6. Острый диффузный пролиферативный гломерулонефрит
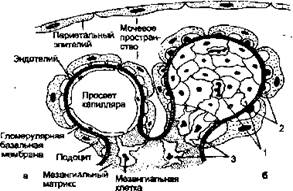
] Нормальный клубочек | | Острый постинфекционный гломерулонефрит |
Обозначения: 1— пролиферация эндотелиальнык клеток и инфильтрация петель нейтрофилами; 2 — субэпителиальные депозиты; 3 — пролиферация мезангиальных клеток.
Латентный период между инфекцией и началом нефрита сравним с временем, необходимым для образования антител. Повышенные титры антител к одному или более продуктам жизнедеятельности стрептококков обнаруживают у подавляющего большинства больных. Наличие гранулярных иммунных депозитов в клубочках позволяет предполагать включение в процесс иммунокомплексного механизма. Идентифицированы антигенные компоненты стрептококка, ответственные за развитие иммунной реакции. В пораженных клубочках выявлены цитоплазматический антиген эндострептозин, а также некоторые катионные антигены, включая протеиназу, связанную со стрептококковым токсином. Однако они представляют собой внедренные антигены или часть циркулирующих иммунных комплексов, а может быть, и то и другое. Гломерулярная базальная мембрана и иммуноглобулины, поврежденные стрептококковыми ферментами, одновременно выступают в роли антигенов.
Классическая морфологическая картина представлена увеличенными, многоклеточными, относительно малокровными клубочками. Гиперклеточность связана с 4 главными причинами: пролиферацией и набуханием эндотелиальных клеток; отложением глыбок иммунных комплексов на эпителиальной стороне гломерулярной базальной мембраны; присутствием нейтрофилов в просвете капиллярных петель; незначительной пролиферацией мезангиальных клеток (схема 18.6). Пролиферация и лейкоцитарная инфильтрация имеют диффузный характер и вовлекают в патологический процесс все дольки всех клубочков. Комбинация пролиферации, набухания и лейкоцитарной инфильтрации ведет к облитерации просвета капилляров. Мелкие депозиты фибрина в просвете капилляров и мезангий можно обнаружить с помощью специальной гистологической окраски. Помимо этого, в строме (интерстиции) возникают отек и воспаление, а канальцы с признаками дистрофии эпителия содержат' в просвете цилиндры из эритроцитов. При иммунофлюоресцентной микроскопии в мезангий и вдоль базальной мембраньг обнаруживаются гранулярные депозиты IgG, IgM и СЗ-компонента комплемента. При электронной микроскопии электронно-лотные депозиты на эпителиальной стороне мембраны часто имеют вид «горбов»
Нестрептококковый острый гломерулонефрит. Сходная форма гломерулонефрита возникает спорадически в связи с другими бактериальными инфекциями, например стафилококковым эндокардитом, пневмококковой пневмонией и менингококкемией, вирусными заболеваниями, например гепатитом В, свинкой, ветрянкой, инфекционным мононуклеозом и паразитарными инфекциями (малярией, токсоплазмозом).
Быстро прогрессирующий (полулунный) гломерулонефрит (RPGN-Rapidly Progressive Glomerulonephritis). Он проявляется
Схема 18.7, Быстро прогрессирующий полулунный гломерулонефрит
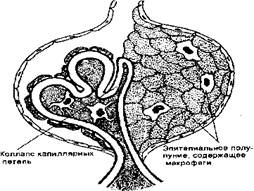
в быстром и прогрессирующем снижении функции почек (нередко с тяжелой олигурией и анурией) в течение нескольких недель или месяцев, обычно приводящей к необратимой почечной недостаточности. Все случаи быстро прогрессирующего гломерулонефрита сопровождаются формированием эпителиальных полулуний в большинстве почечных клубочков (схема 18.7).
Быстро прогрессирующий гломерулонефрит подразделяют на 3 группы: постинфекционный (постстрептококковый); при системных заболеваниях; идиопатический (так называемый первичный, или изолированный) быстро прогрессирующий гломерулонефрит. Не существует единого патогенетического механизма, который мог бы объяснить все случаи быстро прогрессирующего гломерулонефрита. При системной красной волчанке и в случае постстрептококковых форм быстро прогрессирующий гломерулонефрит связан с иммунными комплексами.
Быстро прогрессирующий гломерулонефрит, связанный с синдромом Гудпасчера (см. ниже), — классический пример антительного нефрита. При этом заболевании циркулирующие антитела к гломерулярной базальной мембране обнаруживают более чем в 95 % случаев. Эти антитела, перекрестно реагирующие с базальными мембранами легочных альвеол, обусловливают появление клинической картины легочных кровоизлияний, сопровождающихся почечной недостаточностью. Линейные депозиты IgG и во многих случаях СЗ-компоненты комплемента можно выявить вдоль гломерулярной и альвеолярной базальных мембран с помощью иммуногистохимических методов.
Идиопатический быстро прогрессирующий гломерулонефрит встречается примерно в 50 % наблюдений. Он может быть связан с различными патогенетическими механизмами: иммунными комплексами, антителами к гломерулярной базальной мембране, ANCA. Во всех случаях в почечных клубочках находят наиболее выраженные гломерулярные повреждения.
Макроскопически почки увеличены в размерах, бледные, часто с петехиальными кровоизлияниями на поверхности. В зависимости от причины повреждения в клубочках могут развиваться фокальный некроз, диффузная или очаговая пролиферация эндотелия и пролиферация мезангия. В гистологической картине доминирует, однако, образование характерных клеточных фигур — полулуний (рис. 18.6). Последние образуются в результате пролиферации париетальных клеток и миграции моноцитов и макрофагов в пространство между капсулой и капиллярным клубочком. Полулуния окончательно облитерируют указанное пространство и сдавливают почечный клубочек. Между слоями клеток в полулуниях обнаруживают полоски фибрина. С помощью электронной микроскопии у некоторых пациентов выявляют субэпителиальные депозиты, однако во всех случаях наблюдают отчетливые разрывы гломерулярной базальной мембраны. Со временем большинство полулуний склерозируется.
Нефротический синдром
Некоторые гломерулярные заболевания (мембранозная гломерулопатия, липоидный нефроз, фокально-сегментарный гломерулосклероз) всегда сопровождаются развитием нефротического синдрома.
Для нефротического синдрома характерны массивная протеинурия с ежедневными потерями 3,5 г и более белка, гипоальбуминемия с уровнем альбумина в плазме крови менее 3 г/ 100 мл, генерализованный отек и гиперлипидемия. Все это является следствием увеличения проницаемости гломерулярной капиллярной стенки для белков плазмы из-за потери отрицательного заряда гломерулярным фильтром.
Тяжелая протеинурия ведет к падению концентрации альбумина в сыворотке крови, связанному со снижением функциональных возможностей печени синтезировать альбумин, а также к гипоальбуминемии и нарушению альбумин-глобулинового индекса. Генерализованный отек свидетельствует об уменьшении коллоидного осмотического давления крови и аккумуляции жидкости в интерстициальных тканях. Задержка ионов натрия и воды усиливает отек. Все эти проявления обусловлены несколькими факторами: компенсаторной секрецией альдостерона, вызванной секрецией антидиуретического гормона в ответ на гиповолемию; стимуляцией симпатической системы; снижением секреции натрийуретических факторов, таких как предсердные пептиды.
Механизм развития гиперлипидемии при нефротическом синдроме достаточно сложен. У большинства больных возрастает содержание холестерина, триглицеридов, липопротеинов низкой плотности и апопротеинов. В некоторых случаях наблюдается снижение липопротеинов высокой плотности. Эти дефекты, видимо, частично обусловлены повышенным синтезом липопротеинов в печени, аномальным транспортом циркулирующих липидных частиц и сниженным катаболизмом. Липидурия развивается вслед за гиперлипидемией, так как не только молекулы альбуминов, но и липопротеины проникают сквозь стенку гломерулярных капилляров. Липиды появляются в моче в виде свободного жира или овальных жировых телец, представляющих собой липопротеин, резорбированный эпителиальными клетками канальцев, а затем потерянный подвергшимися дистрофии клетками. Такие больные особенно подвержены инфекциям.
4. Иллюстративный материал: демонстрационные таблицы, презентации, фотографии микроскопической картины патологических процессов в электронном виде.
Литература
1. Струков А.И. Патологическая анатомия : учебник / А. И. Струков, В. В. Серов . - 5-е изд. - М., 2011. - 848 с. : ил.
2. Струков А.И. Патологическая анатомия : учебник / А. И. Струков, В. В. Серов. - 5-е изд. стереотипное. - М. : Литтерра, 2010. - 848 с. : ил
3. Повзун С.А. Патологическая анатомия в вопросах и ответах. : учебник / С. А. Повзун. - М : ГЭОТАР-Медиа, 2007. - 175 с. : ил
Дополнительная литература:
1. Тусупбекова М.М. Клиническая патоморфология : учебник / М. М. Тусупбекова . - Алматы : Эверо, 2012. - 184 с. : ил
2. Патологическая анатомия. : атлас / ред. О. В. Зайратьянц. - М : ГЭОТАР-Медиа, 2010. - 470 с. : ил
3. Маянский Д.Н.Лекции по клинической патологии : руководство / Д. Н. Маянский. - М : ГЭОТАР-Медиа, 2008. - 464 с. : ил
4. Руководство к практическим занятиям по патологической анатомии : руководство / В. В. Серов, М. А. Пальцев. - М. : Медицина, 2005/1998. - 544 с. : ил
5. Тусупбекова М.М. Морфологический атлас общепатологических процессов Алматы: Эверо, 2012
6. Пальцев М.А. Руководство по биопсийно-секционному курсу : руководство / М. А. Пальцев, В. Л. Коваленко, Н. М. Аничков. - М. : Медицина, 2004. - 256 с. : ил.
7. Серов В.В. Хазанов, А. Т. Руководство по секционному курсу [Текст] : учебник / А. Т. Хазанов, И. А. Чалисов. - 3-е изд. - М : Медицина, 1984/2002
8. Патологическая анатомия: Курс лекций /под.ред. В.В. Серова, М.А. Пальцева М: Медицина, 1998
Контрольные вопросы (обратная связь)
1. Классификация заболеваний почек.
2. Клинико-морфологическая характеристика гломерулопатий и тубулопатий, почечно-каменной болезни.
3. Нефросклероз. Патологическая анатомия.
1.Тема №16: « Болезни эндокринной системы. Болезни опорно- двигательной системы, кожи и придатков.»
2. Цель: формирование у студентов знаний о структурных основах эндокринной и опорно-двигательной систем, морфологических проявлениях, осложнениях, исходах и дифференциальной диагностике и использовании полученных знаний в практической работе врача-стоматолога с учетом возрастных особенностей.
3. Тезисы лекции:
Сахарный диабет – хроническое заболевание, обусловленное абсолютной или относительной инсулиновой недостаточностью, приводящей к нарушению всех видов метаболизма, прежде всего углеводного. Сахарный диабет является самым распространенным эндокринным заболеванием, которым, по данным ВОЗ, во всем мире страдает более 100 млн. человек. Следует отметить, что заболеваемость сахарным диабетом (СД) в экономически развитых странах ежегодно увеличивается на 6-10 %. В связи с этим СД наряду с сердечно-сосудистыми заболеваниями и онкологическими болезнями вошел в группу болезней, являющихся самыми частыми причинами смерти и инвалидности больных.
Диабет – греческое слово, использовавшееся для обозначения заболеваний, сопровождающихся образованием большого количества мочи – полиурии. Диабет по-гречески – это сифон или процесс протекания жидкости насквозь. В XVIII веке было установлено, что в большинстве случаев диабета моча содержит сахар, и такой вариант диабета назвали сахарным диабетом – diabetes melitus от латинского mellitus (подслащенный медом) в отличие от несахарного диабета – diabetes insipidus, при котором полиурия не сочетается с глюкозурией.
Классификация СД. В соответствии с классификацией ВОЗ (1999 года) выделяют СД I типа, проявляющийся деструкцией β-клеток панкреатических островков с абсолютной инсулиновой недостаточностью (аутоиммунный и идиопатический); СД II типа, в основе которого лежат изменения β-клеток, приводящие к недостаточности и резистентности к инсулину; другие специфические типы диабета – генетические дефекты в действии инсулина, необычные формы иммуноопосредованного диабета; гестационный СД (диабет беременных).
При СД I типа выделяют два вида: иммунный и неиммунный. В основе иммунного СД лежит деструкция β-клеток клетками иммунной системы. В большинстве случаев определяются антитела к глутаматдекарбоксилазе (маркер β-клеток островков Лангерганса), GAD65, клеткам островков или инсулину. Заболевание строго ассоциировано с тканевыми антигенами HLA2RH, HLADR3 и другими аутоиммунными заболеваниями, такими как болезнь Грейвса, Хашимото, Аддисона. Неиммунный СД I типа является вторичным и осложняет, например, панкреатит.
Сахарный диабет II типа (инсулиннезависимый СД) представляет собой группу гетерогенных нарушений углеводного обмена и это объясняет отсутствие единой общепринятой теории патогенеза данного заболевания. Генетические аспекты ИНСД в развитии заболевания подтверждаются следующими фактами: у однояйцевых близнецов ИНСД развивается почти всегда (95-100 %), однако генетический дефект, определяющий развитие ИНСД, до конца пока не расшифрован. Вместе с тем, имеются факты, свидетельствующие о том, что два независимых гена вовлечены в патогенез ИНСД: один отвечает за нарушение секреции инсулина, второй – вызывает развитие инсулинорезистентности. Рассматривается также вариант наличия общего дефекта в системе узнавания глюкозы β-клетками или периферическими тканями, в результате чего имеет место или снижение транспорта глюкозы или снижение глюкозостимулированного ответа β-клеток. Риск развития СД II типа возрастает от 2 до 6 раз при наличии СД у родителей или ближайших родственников. Риск развития ИНСД увеличивается в два раза при ожирении I степени, в 5 раз при ожирении средней степени, в случаях ожирения III степени риск увеличивается в 10 раз! Особое значение для развития ИНСД имеет ожирение с отложением жира в области живота – абдоминальное распределение жира. Следует отметить, что такое распределение жира более тесно связано с развитием метаболических нарушений, включая гиперинсулинемию, гипертензию, гипертриглицеридемию, резистентность к инсулину и СД II типа, чем периферическое распределение жира или распределение его в типичных частях тела.
В последние годы значительный интерес вызывает гипотеза «дефицитного» фенотипа: недостаточное питание в период внутриутробного развития или ранний постнатальный период является одной из основных причин замедленного развития эндокринной функции поджелудочной железы и предрасположенности к ИНСД.
Метаболические нарушения при СД I типа разнообразны: дефицит инсулина приводит к гипергликемии, глюкозурии, полиурии, снижению объема циркулирующей крови, развитию диабетической комы. Дефицит инсулина приводит к усиленному липолизу, увеличению содержания жирных кислот и кетоацидозу.
Классическими симптомами СД I типа являются полиурия, полидипсия, полифагия с парадоксальным снижением массы тела. Основными висцеральными проявлениями СД являются периферическая и автономная нейропатия, а также сосудистые изменения.
В таблице 1 приведены основные дифференциально-диагностические признаки СД I и II типов.
Патоморфология СД. Независимо от формы СД у большинства больных, страдающих диабетом в течение десятков лет, выявляются морфологические изменения в сосудах микроциркуляторного русла (повышение проницаемости базальных мембран, плазморагия, гиалиноз мелких артерий и капилляров мышц, кожи, сетчатки глаз, нервных стволов). Такие изменения сосудов микроциркуляторного русла входят в понятие диабетическая микроангиопатия. Основная причина микроангиопатии – гипергликемия. Наиболее выражены и имеют определенную специфику морфологические проявления диабетической микроангиопатии в почках. Они представлены диабетическим гломерулонефритом и гломерулосклерозом, в основе которых лежит пролиферация мезангиальных клеток в ответ на засорение мезангия продуктами обмена и иммунными комплексами. В финале развиваются гиалиноз мезангия и гибель клубочков (синдром Кимельстила-Уильсена).
Таблица 1.
Дата добавления: 2015-09-02; просмотров: 1534;
