Флюоресцентные красители
Данзилхлорид выпускается в виде двух кристаллических
форм: кристаллы красного цвета плавятся при 70°, желтые—-
при 73°. Они хорошо растворяются в ацетоне. Максимум их пог-
лощения в растворе лежит в области 330—360 нм, флюоресцен-
ции — 510 нм. Молярная экстинкция E=4,3 · 106.
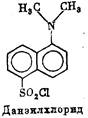
В щелочной среде, отщепляя ион хлора, данзильный остаток
присоединяется к аминокислотам, пептидам и белкам, главным
образом, по их концевой аминогруппе. При этом его способность
флюоресцировать сохраняется.
Данзилирование белков и пептидов позволяет следить эа хо-
дом их миграции при электрофорезе путем освещения гелей
длинноволновым ультрафиолетовым светом, достаточно хорошо
проникающим через пирексовое стекло. Скорость миграции бел-
ков при данзилировании практически не изменяется, поэтому не-
большие примеси данзилированных препаратов можно исполь-
зовать в качестве маркеров при разделении неокрашенных бел-
ковых смесей.
Данзилирование не мешает протеолизу белка, что позволяет
проводить пептидный анализ данзилированных белков после их
разделения электрофорезом в ПААГ и элюции из геля. При этом
удается обнаруживать по флюоресценции не только концевые,
но и внутренние пептиды. Дело в том, что Данзилирование, хотя
и намного менее эффективно, чем по концевым аминогруппам,
происходит (в порядке ослабления) по SH- и ОН-группам цис-
теина и тирозина, e-NН3-группам лизина и по гистидину. Цен-
ным является то обстоятельство, что автолиз неданзилирован-
ных протеаз не создает никаких помех при картировании пепти-
дов.
Недавно описано Данзилирование белков для последующего
разделения ступенчатым электрофорезом в комплексе с ДДС-Na
(в системе Лэммли) [Tijssen, Kurstak, 1979]. Белки растворяют
до концентрации 2 мг/мл в 0,1 М Трис-ацетатном буфере (рН
8,2) с 10% ДДС-Na, добавляют 1/15 объема 10%-ного. раствора
данзилхлорида в ацетоне и, закрыв пробирку парафильмом, ин-
кубируют в течение 15 мин на водяной бане при 50°. Свободный
данзилхлорид нерастворим в водном ацетоне и образует мутно-
желтую суспензию, тем не менее Данзилирование в ней происхо-
дит. Раствор просветляется после добавления 1/15 объема (b-мер-
каптоэтанола и дополнительной инкубации в течение 15 мин.
Меркаптоэтанол связывает и растворяет избыток данзилхло-
рида.
Инкубационную смесь можно без дальнейшей очистки под-
вергать электрофорезу. Ярко люминесцирующие побочные про-
дукты данзилирования быстро отделяются от белков и уходят
вперед. В работе описан и препаративный вариант разделения
белков под контролем данзилированных аликвот. При этом ис-
пользуется электрофоретическая элюция белковых полос из ге-
ля. Описан также пептидный анализ разделенных белков элек-
трофорезом в системе Лэммли с градиентом пористости рабоче-
го геля. Несколько ранее препаративный электрофорез белков
под контролем данзилированных аликвот был описан Стефенсом
[Stephens, 1975].
Флюоресцамин (иногда поставляется под фирменным наиме-
нованием «Fluram») — желтовато-белый порошок, хорошо раст-
воримый в ацетоне, диметильсульфоксиде и ацетонитриле. Хра-
нить раствор следует не более двух недель: он неустойчив, осо-
бенно при рН<4 и рН>10. При взаимодействии с первичными
аминами (концевыми аминогруппами, e-NH2-группами лизина)
в водной среде флюоресцамин дает сильно флюоресцирующие
продукты в соответствии с представленной ниже схемой.
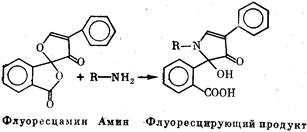
Реакция идет успешнее в щелочной среде. Продукт реакции
имеет два максимума поглощения (при 300 и 390 нм) и макси-
мум флюоресценции при 480 нм. Замечательно, что ни сам флюо-
ресцамин, ни продукты его распада в растворе не флюоресци-
руют. При окрашивании белков и пептидов флюоресцамином не
создается флюоресцирующего фона и окрашенный продукт мож-
но не отделять от красителя, что чрезвычайно удобно. При ис-
пользовании флюоресцамина для окраски белков или пептидов
перед электрофорезом следует иметь в виду, что он вносит до-
полнительный отрицательный заряд (за счет образующегося
карбоксила) и этим изменяет электрофоретическую подвижность
окрашенного белка. В случае разделения белков, обработанных
ДДС-Na, этот единичный заряд практической роли не играет.
В недавней работе [Jackowski, Liew, 1980] флюоресцамин использовали
для окраски белков после их двумерного фракционирования влектрофокуси-
ровкой и электрофорезом по методу 0'Фаррела. Белки фиксировали в пласти-
не геля, вымачивая ее в течение ночи в 10%-ной уксусной кислоте с 50% ме-
танола (одновременно вымывались амфолины, которые окрашиваются флюо-
ресцамином). Гель споласкивали в 7%-ной уксусной кислоте, помещали на
1 ч в диметилсульфоксид (ДМСО) и на 2ч — в 0,04 М раствор борной кисло-
ты в ДМСО, титрованный NaOH до рН 10. Затем добавляли равный объем
раствора флюоресцамина (0,5 мг/мл) в ДМСО и встряхивали смесь в течение
8 ч. Белковые пятна проявлялись уже через 2 ч. Их фотографировали при ос-
вещении длинноволновым ультрафиолетовым светом.
Хранить гель в ДМСО следует в темноте: на свету способ-
ность к флюоресценции за 24 ч падает до нуля. Чувствитель-
ность и разрешающая способность окраски флюоресцамином
примерно такие же, как и СВВ R-250, но линейный участок за-
висимости интенсивности окраски (флюоресценции) от количе-
ства белка больше — вплоть до 7 мкг белка на 1 см2 в пятне или полосе. Для окраски СВВ R-250 линейность сохраняется не да-
лее, чем для 3 мг/см2.
Окрашивание белка флюоресцамином перед электрофорезом
было использовано значительно раньше [Eng, Parkers, 1974].
Белок, обработанный ДДС-Na, растворяли до концентрации
0,5—1 мг/мл в 0,017 М Na-фосфатном буфере (рН 8,5) с 5%
ДДС-Na. К 100 мкл этого раствора добавляли 5 мкл раствора
флюоресцамина в ацетоне и встряхивали. Затем без дальнейшей
очистки 10 мкл этой смеси вносили в трубку для электрофореза.
Замечено, что ДДС-Na уменьшает эффективность окраски
флюоресцамином. По-видимому, он создает препятствия для
контакта красителя с аминогруппами белка. Аналогично исполь-
зовали флюоресцамин и для окраски пептидов перед электрофо-
резом [Rosemblatt et al., 1975]. В 1976 г. было описано исполь-
зование для окрашивания белков перед электрофорезом родст-
венного флюоресцамину препаратаМДФФ (2-метокси-2,2-ди-
фенил-3-фуранона) [Barger et al., 1976]. Как и флюоресцамин,
этот препарат реагирует с первичными аминами, давая сильно
флюоресцирующие продукты, в то время как сам он в растворе
не флюоресцирует. Схема реакции представлена ниже.
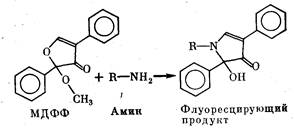
В отличие от флюоресцамина МДФФ не привносит с собой
дополнительного заряда. Он хорошо растворим в ацетоне и
абсолютном метаноле. Максимум возбуждения флюоресцирую-
щего продукта — при 390 нм, флюоресценции — при 745 нм.
Реакция идет лучше в щелочной среде (рН 9,5.) Продукт устой-
чив в интервале рН 2—10. Интенсивность флюоресценции—в
2,5 раза выше, чем при окраске флюоресцамином. Она лишь не-
значительно уменьшается в случае предварительной обработки
белка ДДС-Na и b-меркаптоэтанолом при 100°. Чувствитель-
ность метода очень высока: по утверждению авторов, им удава-
лось обнаруживать до 0,001 мкг белка в полосе. В отличиеот
флюоресцамина окраска не ослабевает в течение нескольких ме-
сяцев. Однако есть данные, что с длинными полипептидными
цепями МДФФ реагирует слабее, чем флюоресцамин. Окраши-
вание ведут в 0,01 М боратном буфере (рН 9,5), энергично пере-
мешивая раствор белка с избытком раствора МДФФ в ДМСО.
Недавно [Chen, Thomas, 1980] МДФФ был использован для
окраски бромциановых пептидов альдолазы перед их разделе-
нием электрофорезом в 15%-ном ПААГ с ДДС-Na. Пептиды,
обработанные ДДС-Na и р-меркаптоэтанолом, окрашивали в
0,1 М Li-боратном буфере (рН 9,5), добавляя к ним в пятикрат-
ном избытке МДФФ, растворенный в абсолютном метаноле.
Ортофталевый альдегид (ОФА) в присутствии b-меркапто-
этанола реагирует с первичными аминами белков и пептидов,
давая сильно флюоресцирующий продукт в соответствии с при-
веденной ниже схемой.
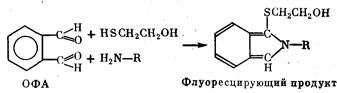
ОФА растворим в воде, но лучше—в метаноле, этаноле, аце-
тоне и диоксане. Реакция присоединения хорошо идет при
рН 8—9. При использовании ОФА его сначала растворяют в
одном из перечисленных органических растворителей, а потом
смешивают с избытком водного буфера нужной концентрации и
значения рН. Максимум возбуждения флюоресцирующего про-
дукта — при 340 нм, флюоресценции — при 445 нм. Раствор са-
мого ОФА не флюоресцирует. Чувствительность метода — выше,
чем в случае флюоресцамина, но и фон флюоресценции побочных
продуктов выражен сильнее.
Использование ОФА для окрашивания комплексов белок—
ДДС-Na перед их электрофорезом описано еще в 1973 г. [Wei-
dekamm et al., 1973]. Реакцию проводили в 0,025 М Na-фосфат-
ном буфере (рН 8,5) в присутствии 5% ДДС-Na и 2% b-меркап-
тоэтанола. Сначала белок растворяли в этой смеси и прогревали
при 100° для полной денатурации и восстановления, затем туда
добавляли 1/5 объема 1%-ного раствора ОФА в метаноле и вы-
держивали в темноте 2—3 ч.
Дата добавления: 2015-10-21; просмотров: 927;
