Реакции ароматических кислот
Рассмотренные ароматические кислоты вступают во все реакции, характерные для органических кислот:
- взаимодействуют с основаниями с образованием солей; соли щелочных металлов хорошо растворимы в воде. Бензоаты натрия и аммония обладают бактерицидными свойствами и находят применение в качестве консервантов в пищевых продуктах и антисептиков в медицине;
- легко реагируют с низкомолекулярными спиртами (метиловым, этиловым) с образованием сложных эфиров;
- при высоких температурах подвергаются декарбоксилированию. Наиболее подвержена декарбоксилированию коричная кислота; уже при температуре 150 0С она превращается в стирол:

Бензойная кислота теряет карбоксильную группу лишь при
нагревании до 370 0С.
Как и другие ароматические соединения, ароматические кислоты способны к реакциям электрофильного замещения по бензольному ядру. Карбоксильная группа бензойной кислоты (заместитель второго рода) замедляет подобные реакции и ориентирует замещение в мета-положение. В фенилуксусной и коричной кислотах акцепторное влияние карбоксила ослабевает. Коричная кислота нитруется с образованием смеси орто-, мета- и пара-нитрокоричных кислот; сульфирование происходит, в основном, в пара-положение.
Коричная кислота, имея двойную связь в боковой цепи, проявляет свойства алкенов: легко присоединяет галогены, восстанавливается до дигидрокоричной кислоты, сильными окислителями окисляется до бензойной кислоты:
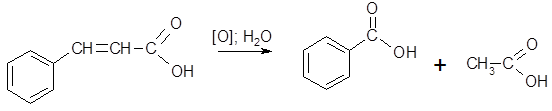
Фенилуксусная кислота, как и фенилацетальдегид, отличается высокой реакционной активностью метиленовой группы. Кроме характерных для α-звена реакций замещения водорода на галоген, метиленовая группа обладает свойствами СН-кислоты, что проявляется в способности присоединяться по карбонильной группе оксосоединений. Примером может служить конденсация ФУК с о-нитробензальдегидом, являющаяся первой стадией широко известного синтеза фенантрена по методу Пшорра. Конденсация протекает в условиях реакции Перкина (высокая температура; катализотор – натриевая или калиевая соль ФУК):
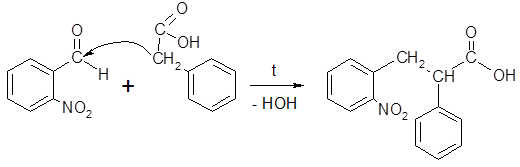
Антраниловая кислота, как и другие аминокислоты, отличается амфотерными свойствами (кислотными – за счет карбоксильной группы, основными – за счет аминогруппы) и образует соли как с кислотами, так и с основаниями:
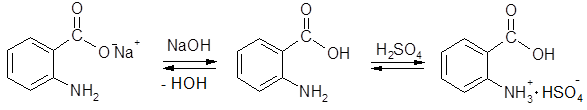
С многовалентными металлами антраниловая кислота образует нерастворимые в воде соли. Осаждение в форме медной соли используют в количественном анализе антраниловой кислоты.
Метилантранилат обладает свойствами сложных эфиров и аминосоединений. Как сложный эфир он омыляется растворами щелочей, что используют для его количественного определения. За счет аминогруппы метилантранилат реагирует с альдегидами с образованием шиффовых оснований:
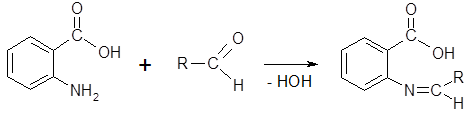
Полученные производные вследствие наличия в структуре протяженной системы сопряжения оказываются окрашенными соединениями. Протекание подобной реакции в парфюмерных композициях при наличии в них альдегидов приводит к появлению нежелательной окраски и ограничивает использование метилантранилата. В то же время данная реакция позволяет получать новые душистые вещества, например, так называемый гринамин:
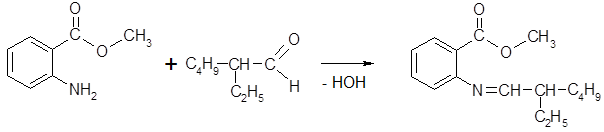
гринамин
Гринамин представляет собой вязкую жидкость ярко-желтого цвета с очень сильным и стойким запахом, напоминающим запах цветов черемухи.
Дата добавления: 2015-09-29; просмотров: 4344;
