Вывод основного уравнения молекулярно кинетической теории идеального газа
(уравнения Клаузиуса)
Согласно молекулярно-кинетической теории газ есть совокупность огромного числа молекул, хаотически движущихся и сталкивающихся друг с другом и со стенками сосуда. Многочисленные удары о стенку сосуда создают непрерывно действующую на нее силу, которая, будучи поделена на площадь стенки, дает давление газа р. Эта сила, а следовательно, и давление зависит от скорости движения молекул:
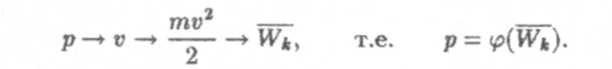
Это и есть в общем виде уравнение Клаузиуса, предложенное немецким физиком-теоретиком Рудольфом Юлиусом Эмануэлем Клаузиусом, профессором Цюрихского университета. Конкретный вид этого уравнения нам предстоит найти.
Сделаем следующие упрощающие предположения относительно газа.
а) Молекулы — абсолютно упругие шарики пренебрежимо ма-
лого размера (материальные тонки). Они отскакивают от стен-
ки, изменял только направление, но не величину скорости.
 б) Силы притяжения между молекулами пренебрежимо ма-
б) Силы притяжения между молекулами пренебрежимо ма-
лы, а собственным объемом молекул можно пренебречь (так как
в среднем расстояние между молекулами газа гораздо больше
размеров молекул).
Газ, обладающий такими свойствами, называют идеальным газом. Очевидно, что реальный газ при условиях близких к нормальным, а также при высокой температуре (Т) и при низком давлении (р) весьма близок по своим свойствам к идеальному.
Выведем уравнение Клаузиуса. Пусть в сосуде с плоскими стенками находится идеальный газ, число молекул которого в единице объема обозначим через п. Массу каждой молекулы будем считаь равной т. Вследствие хаотичности движения молекул газа можно полагать, что вдоль каждого из основных направлений в пространстве (х, у, z) движется в среднем 1/3 всех молекул, и соответственно в положительном направлении оси х — 1/6 всех молекул газа.
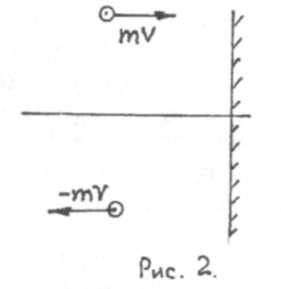
Рассмотрим результат удара одной такой молекулы о стен-
|
ку сосуда (рис. 2), полагая, что последняя расположена перпендикулярно к оси х. До удара молекула обладала импульсом mv; после удара он стал равным (—mv). В результате удара стенка получила импульс ∆к = 2mv. За время t до стенки долетят молекулы, находящиеся от нее на расстоянии l= vt.
Рассмотрим участок стенки площадью ∆S; тогда за время t до нее долетят молекулы, заключенные в цилиндрическом объеме площадью основания ∆S с длиной образующей l, движущиеся в положительном направлении оси х. Очевидно, что число таких молекул N будет равно:

За время t эти молекулы передадут стенке импульс
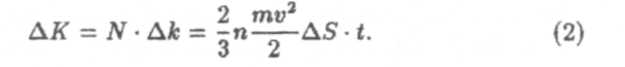
Импульс, передаваемый этими молекулами в единицу времени, численно равен силе, действующей на стенку со стороны газа придут в


| Величина mv2/2в формуле (4) есть величина средней энергии поступательного движения молекул Wk-Отсюда получим уравнение Клаузиуса |
Давление газа пропорционально средней кинетической анергии поступательного движения молекул газа и числу молекул в единице объема.
Итак, уравнение Клаузиуса выражает макроскопическую характеристику газа р через его микроскопическую характеристику Wk. Естественно предположить, что и другая макрохарактеристика газа — его термодинамическая температура Т тоже связана с микрохарактеристикой Wk (поскольку энергия зависит от скорости, а скорость от температуры). Эта связь наблюдается в уравнении Больцмана.
Дата добавления: 2015-08-11; просмотров: 1576;
