Водородная связь и ее свойства.
Атом водорода – самый маленький и самый легкий из всех существующий атомов. Имеет заряд +1. С наиболее электроотрицательными элементами (F, О, N) водород образует дополнительные связи, которые называют водородными. Водородная связь возникает между водородом и кислородом, которые принадлежат к различным молекулам и ковалентно между собой не связаны. Водородную связьобозначают точками.
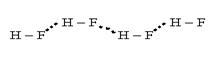 Водородная связь близка к межмолекулярным связям. Все межмолекулярные связи имеют низкую энергию. Энергия водородной связи низкая: 8 ÷ 40 кДж/моль. Наиболее высокая энергия водородной связи у водорода с фтором (25÷ 40 кДж/моль), ниже - с О (13÷ 29 кДж/моль) и еще ниже с N (8 ÷ 21 кДж/моль). Водородная связь характерна для спиртов, карбоновых кислот, в том числе высших и нуклеиновых, белков, поэтому, несмотря на низкую энергию связи, водородная связь крайне важна для жизни на Земле. Комплементарность - пространственная взаимодополняемость молекул или их частей, приводящая к образованию водородных связей. Комплементарность лежит в основе ферментативного катализа, самосборки биологических структур, матричного синтеза полинуклеотидов, молекулярных механизмов иммунитета. Например, в строении нуклеиновых кислот две полинуклеотидные цепи в результате комплементарного взаимодействия пар пуриновых и пиримидиновых оснований (А-Т, Г-Ц) образуют двуспиральную молекулу.
Водородная связь близка к межмолекулярным связям. Все межмолекулярные связи имеют низкую энергию. Энергия водородной связи низкая: 8 ÷ 40 кДж/моль. Наиболее высокая энергия водородной связи у водорода с фтором (25÷ 40 кДж/моль), ниже - с О (13÷ 29 кДж/моль) и еще ниже с N (8 ÷ 21 кДж/моль). Водородная связь характерна для спиртов, карбоновых кислот, в том числе высших и нуклеиновых, белков, поэтому, несмотря на низкую энергию связи, водородная связь крайне важна для жизни на Земле. Комплементарность - пространственная взаимодополняемость молекул или их частей, приводящая к образованию водородных связей. Комплементарность лежит в основе ферментативного катализа, самосборки биологических структур, матричного синтеза полинуклеотидов, молекулярных механизмов иммунитета. Например, в строении нуклеиновых кислот две полинуклеотидные цепи в результате комплементарного взаимодействия пар пуриновых и пиримидиновых оснований (А-Т, Г-Ц) образуют двуспиральную молекулу.
4.6.Металлическая связь и ее свойства. 
 4.7Упражнения для самоконтроля направлены на закрепление следующих понятий:
4.7Упражнения для самоконтроля направлены на закрепление следующих понятий:
Дата добавления: 2015-08-08; просмотров: 1279;
