Ионная связь и ее свойства
Ионная связь объясняется следующим образом: атом - типичный металл - теряет свой валентный электрон, превращаясь в катион. Атом – типичный неметалл - принимает электрон, превращаясь в анион.
Na0 – 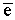 = Na+ (катион)
= Na+ (катион)
Cl0 + 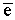 = Cl-- (анион)
= Cl-- (анион)
Ионная связь является максимально полярной. Она образуется атомами тех элементов, которые имеют максимально различные электроотрицательности, т. е. ионная связь образуется щелочными и щелочно-земельными металлами и галогенами:KF; CaCl2; NaI. Ионная связь имеет два основных свойства:
· ненаправленность,
· ненасыщаемость.
Эти два свойства тесно связанны между собой. Два иона: катион и анион полностью не могут компенсировать силовые поля друг друга, поэтому для компенсации своих зарядов каждый ион вынуждает притягивать из пространства дополнительные ионы противоположного знака. В этом заключается ненасыщаемость. Так как электрическое поле иона имеет сферический характер, то для ионной связи характерна ненаправленность. Благодаря тому, что энергия ионизации больше энергии сродства к электрону, полного перехода электронов не происходит даже в случае атомов с очень большой разностью электроотрицательности. Таким образом, соединений с чисто ионной связью не существует. Можно говорить лишь о доле ионной связи. В силу особенностей ионной связи, т.е. её полярности, ненаправленности и ненасыщаемости, молекулы с ионной связью являются достаточно относительным понятием. В водных растворах и расплавах ионные молекулы полностью диссоциированы на ионы: AB=A++B-. Двух- и трёхионных соединений не существует, а весь кристалл ионного соединения можно рассматривать как молекулу, состоящую из огромного числа ионов:АmBn .
Дата добавления: 2015-08-08; просмотров: 6840;
