Термодинамическая вероятность
Вообразим следующий эксперимент, реальное проведение которого невозможно.
В системе (возможно, ею окажется идеальный газ) каким-то образом пометим и сфотографируем все молекулы с таким расчетом, чтобы можно было определить их энергию. Результаты такого эксперимента представим в виде таблицы, в которой приводятся все возможные значения энергии молекул в системе и число молекул с каждым значением энергии.
Таблица 11 - 1.
Условное распределение молекул по энергиям
| Значения энергии | e1 | e2 | e3 | ¼ | ¼ | ei | ¼ | ¼ |
| Число молекул с данным значением энергии | N1 | N2 | N3 | ¼ | ¼ | Ni | ¼ | ¼ |
Если молекулы помечены, т.е. различимы, то появляется возможность подсчитать число способов распределения молекул по значениям энергии наподобие того, как рассчитывается размещение жильцов по домам (см. приложение). Для этого воспользуемся формулой
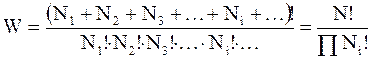 . (11 - 1)
. (11 - 1)
Число способов распределения молекул по энергиям W называется также числом способов реализации данной системы или (что наиболее распространено) термодинамической вероятностью .
Отметим, что термодинамическую вероятность с математической вероятностью объединяет название и единственное свойство, с которым познакомимся при дальнейшем рассмотрении этого понятия. Различия между ними весьма существенны. Минимальное значение математической вероятности равно 0 (невозможное событие), а максимальное равно 1 (абсолютно достоверное событие). Минимальное значение термодинамической вероятности составляет 1 (молекулы могут быть распределены по энергиям единственным способом). Верхнего предела для термодинамической вероятности нет.
Если бы значения чисел были невелики, то для расчетов термодинамической вероятности можно было воспользоваться уравнением (11 - 1) в исходной форме. Для больших чисел, а именно с ними приходится сталкиваться, оперируя с числом молекул в системе, применяется замечательное приближение
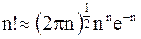 , (11 - 2)
, (11 - 2)
называемое формулой Стирлинга .
Можно воспользоваться более грубым, но достаточным для наших целей приближением, учитывающим, что для больших чисел n>>2p и ln n<<n,
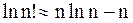 . (11 - 3)
. (11 - 3)
Расчетная формула для термодинамической вероятности системы с реальным числом частиц принимает следующий вид:
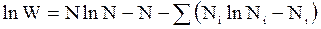 .
.
Так как SNi=N, то формула становится еще проще:
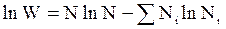 . (11 - 4)
. (11 - 4)
Найдем термодинамическую вероятность системы, образованной сложением равновесных подсистем, одна из которых содержит aN частиц, а другая содержит bN частиц. Относительное распределение частиц по энергиям в равновесных системах совпадает. Поэтому расчет термодинамической вероятности по составной формуле (11 - 4) приводит к следующему:
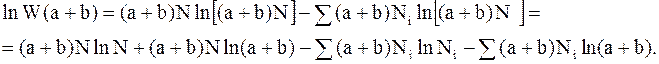
Принимая во внимание, что число подсистем значительно меньше числа частиц в каждой из них, т.е. a+ b<<Ni, получим
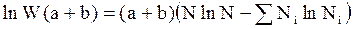
или
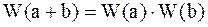 , (11 - 5)
, (11 - 5)
так как  .
.
Формула (11 - 5) показывает, что термодинамическая вероятность системы, полученной сложением подсистем, равна произведению термодинамических вероятностей подсистем. Это свойство термодинамической вероятности называется мультипликативностью .
Мультипликативность характерна и для математической вероятности. Как известно, математическая вероятность исхода нескольких независимых событий равна произведению вероятностей исхода каждого из них.
Дата добавления: 2015-07-24; просмотров: 811;
