Фазовая диаграмма системы с двумя компонентами, неограниченно растворимыми друг в друге в жидком виде и абсолютно нерастворимыми в твердом
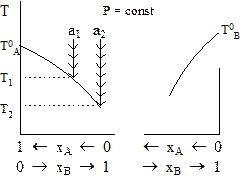 Рис. 8 - 7.К построению диаграммы состав - температура плавления для двухкомпонентной системы.
Рис. 8 - 7.К построению диаграммы состав - температура плавления для двухкомпонентной системы.
|
Плоскую диаграмму этого типа можно построить при условии постоянного давления. Координатами для нее служат состав системы, выражаемый молярной долей одного из веществ хА или другого хВ, причем хВ=1-хА, и температура.
На плоской диаграмме состав - температура для веществ, неограниченно растворимых друг в друге в жидком виде и нерастворимых в твердом, проявляется закономерность, установленная для криометрии: с повышением содержания растворенного вещества в растворе понижается его температура замерзания.
Принцип построения полной диаграммы заключается в следующем.
Вначале выполняют построения для фрагмента, в котором растворителем является вещество А (рис.8 - 7).
Чистую жидкость А охлаждают до появления твердого вещества, а на оси ординат, которой отвечают хА=1 и хВ=0, откладывают температуру замерзания 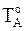 . Далее раствор, взятый в точке а1, охлаждают до выделения первого кристаллика при температуре Т1. Точку начала кристаллизации отмечают на графике. Дальнейшее охлаждение раствора приводит к выделению вещества А и повышению концентрации вещества В в остающемся растворе. Взяв раствор в точке а2, находят температуру начала его кристаллизации Т2. Соединив все точки начала кристаллизации, получают линию, выше которой находится гомогенная система - жидкий раствор. Любая точка под линией относится к гетерогенной системе, содержащей раствор и кристаллы чистого вещества А. Отношение количеств вещества в обеих фазах можно найти по правилу рычага, для чего проводят горизонтальный отрезок через эту точку. Часть отрезка от данной точки до оси ординат характеризует относительное количество вещества в растворе, а другая часть отрезка от этой точки до точки на линии начала кристаллизации - количество чистого вещества А в твердой фазе.
. Далее раствор, взятый в точке а1, охлаждают до выделения первого кристаллика при температуре Т1. Точку начала кристаллизации отмечают на графике. Дальнейшее охлаждение раствора приводит к выделению вещества А и повышению концентрации вещества В в остающемся растворе. Взяв раствор в точке а2, находят температуру начала его кристаллизации Т2. Соединив все точки начала кристаллизации, получают линию, выше которой находится гомогенная система - жидкий раствор. Любая точка под линией относится к гетерогенной системе, содержащей раствор и кристаллы чистого вещества А. Отношение количеств вещества в обеих фазах можно найти по правилу рычага, для чего проводят горизонтальный отрезок через эту точку. Часть отрезка от данной точки до оси ординат характеризует относительное количество вещества в растворе, а другая часть отрезка от этой точки до точки на линии начала кристаллизации - количество чистого вещества А в твердой фазе.
Вторая часть построения относится к фрагменту, в котором растворителем является вещество В (см. рис. 8 - 7). Температура кристаллизации вещества В равна 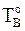 . Второй фрагмент подобен предыдущему.
. Второй фрагмент подобен предыдущему.
Сдвигая оба фрагмента, получают полную фазовую диаграмму (рис.8 - 8).
Линии начала кристаллизации обоих фрагментов соприкасаются в точке Е. Так как эта точка принадлежит двум линиям, то в ней содержатся обе твердые фазы (кристаллы А и кристаллы В) и раствор. Точка Е называется эвтектической точкой, а отвечающий ей состав системы - эвтектической смесьюили эвтектикой.
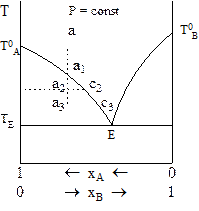 Рис. 8 - 8. Фазовая диаграмма систем с эвтектикой.
Рис. 8 - 8. Фазовая диаграмма систем с эвтектикой.
|
Рассчитаем число степеней свободы в эвтектической точке, исходя из того, что число компонентов системы равно 2, число фаз равно 3 и имеется один переменный внешний параметр (температура):
f = 2 - 3 + 1 = 0.
Таким образом, в точке эвтектике и система нонвариантна.
В области над обеими ветвями линии начала кристаллизации система имеет две степени свободы (К=2; Ф=1). В точках на линии начала кристаллизации и под ней система моновариантна (К=2; Ф=2).
Рассмотрим, какие изменения происходят при охлаждении системы, состав которой соответствует точкам, лежащим левее и правее точки эвтектики и над точкой эвтектики.
Охлаждение системы, состав которой соответствует точке ана рис. 8 - 7, приводит к появлению первых кристаллов в точке а1. Дальнейшее охлаждение приводит к увеличению массы выделяющихся кристаллов чистого вещества А и обогащению веществом остающегося раствора. В точке а2 состав раствора соответствует точке с2. Относительные массы фаз определяются по правилу рычага. В точке а3 .состав раствора определяется точкой с3 на линии начала кристаллизации. Последняя капля раствора имеет состав эвтектической смеси и кристаллизуется при температуре ее замерзания ТЕ. Ниже этой температуры, называемой эвтектической температурой, жидкий раствор в системе не существует; в ней присутствуют только кристаллы веществ А и В.
Охлаждение эвтектической смеси вплоть до температуры ТЕ приводит к одновременному выделению кристаллов А и В.
Системы с эвтектикой образуют разнообразные вещества. Хорошо изучены эвтектические смеси солей с водой. Некоторые из них используются в качестве охлаждающих смесей. В частности, эвтектическая смесь, содержащая 22,4 % хлорида натрия, замерзает при температуре на 21 К ниже температуры замерзания чистой воды. Понижение температуры замерзания эвтектической смеси триоксида хрома с водой по сравнению с чистой водой превышает 100 К. Твердые эвтектические смеси воды с солями называют криогидратами. Состав такой смеси называют криогидратным, а температуру ее кристаллизации - криогидратной температурой.
Смешиваемые вещества А и В могут образовывать химические соединения. Если химическое соединение устойчиво и не разлагается при температуре плавления, то фазовую диаграмму можно рассматривать как сочетание частных диаграмм для вещества А и химического соединения и вещества В и химического соединения.
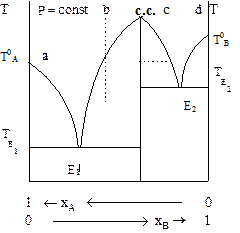 Рис. 8 - 9. Фазовая диаграмма системы температура - состав в случае образования устойчивого химического соединения.
Рис. 8 - 9. Фазовая диаграмма системы температура - состав в случае образования устойчивого химического соединения.
|
На рис. 8 - 9 показана диаграмма системы с устойчивым химическим соединением, плавлению которого отвечает максимум с.с.. Химическое соединение образует две эвтектические смеси: одну с веществом А (ей отвечает точка Е1), а другую с веществом В (ей отвечает точка Е2). При охлаждении раствора, состав которого отвечает точке а, выделяются кристаллы вещества А, и остается жидкий раствор химического соединения и вещества А. Охлаждение системы от точки b приводит к появлению кристаллов химического соединения, а оставшийся раствор содержит вещество А и химическое соединение. При охлаждении раствора от точки с выделяются кристаллы химического соединения, а остающийся раствор состоит из химического соединения и вещества В. Наконец, охлаждение от точки d приводит к выделению кристаллов вещества В, а остающийся раствор содержит химическое соединение и вещество В. Очень устойчивое химическое соединение характеризуется острым максимумом на диаграмме плавления (его точка называется конгруэнтной). Если соединение при плавлении частично разлагается на вещества А и В, то они должны присутствовать с обеих сторон от максимума, форма которого становится более плавной.
Возможно образование ряда химических соединений веществ А и В. Если в системе образуется n химических соединений, то она должна содержать n+1 эвтектических точек.
Если химическое соединение разлагается ниже температуры плавления, то эвтектическая смесь содержит одно из веществ (А или В) и химическое соединение.
Дата добавления: 2015-07-24; просмотров: 911;
