Поглощение окислов азота серной кислотой.
Растворимость NO в H2SO4 незначительна, лучше растворяется N2O3 (NO+NO2).
В жидкой фазе протекают следующие реакции:
1). NO + NO2 +H2O = 2HNO2 Kp
2). HNO2 + H2SO4 = HNOSO4 + H2O K2
принимая, что [H2SO4] = const
V = K2[HNO2][H2SO4] = K2’[HNO2]
где K2’ = K2[H2SO4]. Отсюда, учитывая, что [NO] = [NO2] и [H2O] = const, получаем
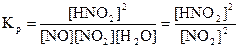
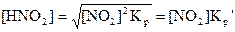
где 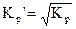
В результате
V = Kp’K2’[NO2]
Скорость процесса будет определяться концентрацией NO2 в жидкой фазе при стационарном процессе, то есть, диффузией.
Можно перевести данный процесс в кинетическую область (увеличить скорость), увеличив объёмную скорость газа. При этом процесс определяется второй стадией:
V = K[HNO2][H2SO4]
и K увеличивается с увеличением T.
Дата добавления: 2015-06-17; просмотров: 920;
