Равновесие в гетерогенных системах.
При выводе закона действующих масс было сделано допущение о том, что все реагенты - газообразные вещества, а рассматриваемая реакция 3H2 + N2 = 2NH3 является гомогенной химической реакцией. Если же в реакции участвуют жидкие или твердые вещества, не образующие растворов друг с другом, то их парциальные давления при постоянной температуре постоянны как постоянны давления насыщенных паров веществ при постоянной температуре. эти постоянные величины вводятся под знак константы равновесия, которая в этом случае будет определяться только давлением газообразного реагента.
Результат применения этого положения на примере реакции диссоциации СаСО3:
СаСО3(ТВ) 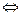 СаO(ТВ) + СО2(Г).
СаO(ТВ) + СО2(Г).
В этом случае:
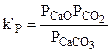 ,
,
но так как СаО и СаСО3 - конденсированные вещества, то при Т = const  и
и 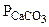 также величины постоянные, поэтому:
также величины постоянные, поэтому:
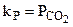 ,
,
где  - упругость диссоциации или давление диссоциации СаСО3.
- упругость диссоциации или давление диссоциации СаСО3.
| Рис. 4.7. Температурная зависимость упругости диссоциации ряда соединений. |
 В условиях химического равновесия при соответствующей температуре давление диссоциации совершенно определенная величина.
В условиях химического равновесия при соответствующей температуре давление диссоциации совершенно определенная величина.
При изменении температуры изменяется и давление диссоциации. Характер этой зависимости позволяет сделать заключение об устойчивости данного соединения против разложения.
Например для реакций диссоциации некоторых оксидов:
2Ag2O(ТВ) 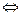 4Ag(ТВ) + О2(Г),
4Ag(ТВ) + О2(Г),  ,
,
2CuO(ТВ) 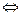 2Cu(ТВ) + О2(Г),
2Cu(ТВ) + О2(Г),  ,
,
2Cu2O(ТВ) 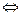 4Cu(ТВ) + О2(Г),
4Cu(ТВ) + О2(Г), 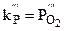 ,
,
температурная зависимость упругостей диссоциации схематично представлена на рис.4.7.
Точки пересечения изобары, соответствуют парциальному давлению кислорода в земной атмосфере (0,21  105 Па), с соответствующими кривыми упругостей диссоциации дает температуры, выше которых соединения будут легко диссоциировать, а при более низких температурах диссоциация будет подавляться наличием парциального давления кислорода воздуха. Анализ кривых на рис. 4.7 приводит также к заключению, что наиболее устойчивым является Сu2О, а наименее - Ag2O. Аналогичные рассуждения могут быть проведены для оценки поведения тех же соединений в атмосфере чистого кислорода.
105 Па), с соответствующими кривыми упругостей диссоциации дает температуры, выше которых соединения будут легко диссоциировать, а при более низких температурах диссоциация будет подавляться наличием парциального давления кислорода воздуха. Анализ кривых на рис. 4.7 приводит также к заключению, что наиболее устойчивым является Сu2О, а наименее - Ag2O. Аналогичные рассуждения могут быть проведены для оценки поведения тех же соединений в атмосфере чистого кислорода.
Дата добавления: 2015-05-21; просмотров: 768;
