Химическое сродство.
Для реакции (4.87) ход рассуждений, использованный в параграфе 12 в условиях V, T=const дает:
 (4.91)
(4.91)
или сокращенно
 , (4.92)
, (4.92)
где 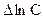 - алгебраическая сумма логарифмов начальных концентраций, каждое из слагаемых
- алгебраическая сумма логарифмов начальных концентраций, каждое из слагаемых
которой умножено на соответствующий коэффициент.
Замена концентраций парциальными давлениями дает в условиях P, T = const:
 . (4.93)
. (4.93)
Уравнения (4.92) и (4.93) - уравнения изотермы химической реакции или уравнения Вант-Гоффа.
Способность различных веществ взаимодействовать между собой с образованием новых веществ была замечена давно и получила наименование химического сродства. Критерий оценки химического сродства был найден не сразу. Несостоятельным оказалось предположение о равенстве теплового эффекта реакции и сродства.
Голландский физико - химик Вант-Гофф предложил новую теорию химического сродства, которая, не объясняя его природу, дает возможность количественно оценить его: в качестве мерила химического сродства предложено использовать полную максимальную работу реакции, если реакция протекает при V = const:
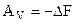
или максимальную полезную работу, если реакция протекает в условиях p = const:

где значения AV и AP могут быть рассчитаны и по уравнениям изотермы химической реакции (4.94).
Для того, чтобы иметь возможность сравнивать сродство различных веществ, было введено понятие нормального (стандартного) сродства.
К уравнению нормального сродства легко подойти, если начальные парциальные давления или концентрации реагентов равны единице.
Тогда:
 и
и
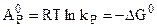 . (4.95)
. (4.95)
Сравнивая 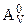 или
или  различных веществ, получают характеристику удаленности данной системы от состояния равновесия.
различных веществ, получают характеристику удаленности данной системы от состояния равновесия.
Замечание. Для растворов правильнее пользоваться не молярными концентрациями (Сi) в случае расчета химического сродства, а мольными долями компонентов.
Дата добавления: 2015-05-21; просмотров: 1446;
