Шаталова Галина 7 страница
По отношению к температуре склеивания клеи делятся на термореактивные и термопластичные. Термореактивные клеи могут быть однокомпонентными. Они образуют клеевой шов при отверждении под действием повышенных температур. Двух или многокомпонентные термореактивные клеи отверждаются под действием катализатора или отвердителя при нормальной или повышенной температуре. Основой таких клеев являются термореактивные смолы. Они в результате химической реакции отверждаются, превращаются в трехмерные твердые вещества. При нагревании они не плавятся, в растворителях не растворяются, а при перегревании разлагаются. К таким смолам относятся эпоксидные, полиэфирные, феноло-формальдегидные, полиуретановые, кремнийорганические и др. Эти смолы являются основой большинства конструкционных клеев. Термопластичные клеи могут быть в виде раствора или дисперсий. Они образуют клеевую пленку вследствие выделения из раствора воды или растворителей. К ним относят также клеи-расплавы, которые склеивают после охлаждения склеиваемых друг с другом деталей до температуры ниже температуры размягчения клея. Термические смолы (поливиниловые, полиакриловые, полиамидные и др.) используются для соединения металлов или пластмасс и обладают хорошей адгезией. Однако обычно их используют в качестве специальных клеев.
По химическому составу конструкционные клеи можно разделить на следующие группы:
1. Феноло-каучуковые (марки ВК-3, ВК-4, ВК-13, ВК-32-200 и др.), дающие прочность при сдвиге 15-25 МПа, теплостойкость 200-300 °С;
2. Фенолополивинилацетатные (марки БФ-2, БФ-4, БФ-6, ВС-10Т и др.), прочность соединений при сдвиге 15-30 МПа, теплостойкость 85-180 °С, низкая стоимость;
3. Полиуретановые (марки ПУ-2, Вилад-11к и др.), прочность при сдвиге 10-20 МПа, теплостойкость 75-125 °С, высокая ударная вязкость, отверждение водой;
4. Кремнийорганические (марки ВК-8, ВК-15 и др.), прочность при сдвиге 10-17,5 МПа, теплостойкость 400-600 °С (длительно), 1000-1200 °С (кратковременно);
5. Эпоксидные (марки ЭДП, Д-9, ВК-1, ВК-9, эпоксид П и ПР и др.), прочность при сдвиге 5-30 МПа, теплостойкость 60-125 °С. Они имеют самое широкое распространение, т.к. отверждаются без выделения побочных веществ и обладают малой усадкой. Прочность соединения не зависит от толщины клеевого слоя. Они стойки к действию влаги и растворителей, пригодны для склеивания широкого класса веществ.
Эпоксидные смолы могут быть использованы в виде растворов, замазок, прутков, порошков и пленок. В процессе отверждения клеевая композиция из стадии вязкотекучего состояния, когда она хорошо смачивает склеиваемые поверхности и проникает в поры, переходит в желеобразное и затвердевает. Эпоксидные клеи в зависимости от применяемого отвердителя могут быть холодного и горячего отверждения.
К отвердителям холодного отверждения относятся полиэтиленполиамин (ПЭПА), АФ-2, Л-20 и др. Их вводят в количестве 8…16 весовых частей на 100 весовых частей смолы. Отверждение при комнатной температуре происходит за 24 часа. Ускорить отверждение можно путем подогрева склеиваемого соединения (при 60 °С выдержка 5 ч, при 120 °С – 30 минут, дальнейший подогрев охрупчивает склейку). Клеевые соединения на эпоксидных клеях холодного отверждения проще в изготовлении, однако менее прочны, чем при соединении на клеях горячего отверждения.
В качестве отвердителей горячего отверждения используют ангидриды некоторых органических кислот (малеиновой, фталевой и др.). Их вводят в смолу в количестве до 70 весовых частей на 100 весовых частей смолы. Отверждение клея начинается при температуре выше 100 °С (при 130 °C выдержка 3 часа, при 260 °С выдержка 20 минут).
Ангидриды кислот могут вводиться в клеевые композиции задолго до иx применения без опасности самопроизвольного отверждения при комнатных температурах.
Количество вводимого отвердителя существенно влияет на свойства клеевых соединений, поэтому уточняется опытным путем и тщательно контролируется при приготовлении клея.
3. МАТЕРИАЛЫ И ОБОРУДОВАНИЕ
Материалы
1. Образцы из сплава АМг.
2. Наждачная бумага
3. Смола эпоксидная модифицированная.
4. Отвердитель.
5. Ацетон технический или бензин.
6. Вата техническая.
Оборудование
1. Пипетка.
2. Разновесы.
3. Лабораторные весы.
4. Стеклянная палочка.
5. Емкость для смешивания компонентов клея.
6. Приспособление для установки образцов в печь.
7. Муфельная печь МП-2УМ.
8. Пирометрический милливольтметр с термопарой ХК.
9. Пинцет.
10. Разрывная машина УММ-5.
4. ПРОГРАММА РАБОТЫ
1. Подготовить две пары заготовок для склеивания листовых нахлесточных образцов из алюминиевого сплава АМг, удалить заусенцы на кромках, зачистить склеиваемые поверхности наждачной бумагой (на длине 15 мм от одного из концов образца), обезжирить ацетоном, сушить 10 минут на воздухе.
2. В емкости для смешивания взвесить 2,5±0,1 г эпоксидной смолы и с помощью пипетки по каплям добавить 0,3±0,1 г (3 полновесные капли) отвердителя, тщательно перемешать стеклянной палочкой в течение 7 минут.
3. Приготовленный клей нанести стеклянной палочкой на зачищенные концы образцов, соединить образцы внахлестку без усилия, используя пинцет, величина нахлестки 15±1,5 мм. Лишний клей, выдавливаемый при сжатии образцов удалить ватным тампоном.
4. Поместить образцы в приспособление для установки образцов в печь, выдержать приспособление с образцами в течении 10-12 минут на печи (при T≈50-80 °С), подсоединить термопару и загрузить приспособление с образцами в печь, нагретую до 120…130 °С, где выдержать их в течении 30 минут, считая с момента достижения в клеевом соединении температуры 125±5 °С, согласно показаниям потенциометра. По окончании выдержки приспособление вынуть из печи и разобрать.
5. Образцы установить на разрывной машине таким образом, чтобы расстояние между зажимами составляло 50±2 мм, а нахлестка образца располагалась симметрично по отношению к обоим зажимам. Продольная ось образца должна совпадать с направлением растягивающего усилия, включить машину и отметить показание нагрузок в момент разрушения образца.
Предел прочности при сдвиге τ (в МПа) рассчитать по формуле:
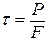 ,
,
где Р- разрушающая нагрузка, Н;
F- площадь склеивания, м2.
Примечание: 1 МПа = 106 Н/м2 или 1 Па = 1 Н/м2, 1 кг = 981 Н.
Результаты испытаний занести в табл. 4.1.
Таблица 4.1
Результаты механических испытаний склеенных алюминиевых образцов
(клей ЭДП, ТУ 6-15-1070-82)
| № п/п | Размеры склейки | Разрушающее усилие Р, Н | Предел прочности τср, МПа | Ср. значение предела прочности, МПа | ||
| ширина нахл., м | длина нахл., м | площадь, м² | ||||
5. СОДЕРЖАНИЕ ОТЧЕТА
1. Цель и задача работы.
2. Описание хода работы и выявленных технологических особенностей склеивания металлов эпоксидным клеем.
3. Вывод по работе.
6. ВОПРОСЫ ДЛЯ САМОКОНТРОЛЯ
1. Назовите основные типы клеев и их свойства.
2. Какова область применения, преимущества и недостатки склеивания металлов?
3. В чем заключаются особенности технологии склеивания эпоксидными клеями?
4. Сравните свойства паяных и клееных соединений из сплава AМг.
Лабораторная работа № 2
ОПРЕДЕЛЕНИЕ КОРРОЗИОННОЙ АКТИВНОСТИ
ПОВЕРХНОСТИ ПАЯНЫХ СОЕДИНЕНИЙ
1. ЦЕЛЬ РАБОТЫ
Изучить методику определения электродных потенциалов поверхности паяных соединений под каплей электролита, углубить теоретические знания об особенностях коррозии соединений, выполненных различными способами пайки.
2. ОСОБЕННОСТИ ЭЛЕКТРОХИМИЧЕСКОГО МЕТОДА
ОЦЕНКИ КОРРОЗИОННОЙ АКТИВНОСТИ ПОВЕРХНОСТИ
Коррозией называют разрушение металлов и сплавов под воздействием внешней среды.
Большинство разрушений паяных соединений в агрессивных средах имеет электрохимическую природу. Поэтому изучение электрохимических характеристик этих соединений имеет важное значение для оценки скорости коррозии и склонности к коррозионному разрушению.
Возникновение коррозионных (гальванических) элементов связано с дифференциацией поверхности паяного соединения на участке с более низким потенциалом и более высоким положительным потенциалом. Первые становятся благодаря этому анодными, вторые – катодными, и коррозия протекает с определенной локализацией активного развития коррозионных поражений.
В связи с таким распределением поверхности на анодные и катодные зоны схему коррозионного процесса можно представить в следующем виде:
анодная зона: Me→Me++e-
катодная зона: Ox+e-→Red
Таким образом, поверхность паяного соединения, помещенного в агрессивную среду, можно уподобить совокупности большого количества отдельных гальванических пар, замкнутых накоротко.
Различия в химическом составе, структуре и напряженном состоянии отдельных зон обуславливают высокую степень электрохимической неоднородности поверхности паяных соединений, что в условиях агрессивной коррозионной среды может явиться причиной ускорения процессов разрушения. Так как паяные соединения являются сложной неоднородной системой, характеризующейся наличием зон металла с различной стойкостью к разрушениям в агрессивных средах, то, очевидно, зная электрохимические характеристики поверхности, можно определить наименее стойкую к коррозии зону соединения.
При нагружении паяного соединения в электролит в результате взаимодействия поверхности металла с раствором возникает разность электрических потенциалов, которую называют электродным потенциалом. Электродный потенциал φ дает представление о термодинамической устойчивости металла в данном электролите, степени пассивного состояния поверхности, зависимости коррозионной стойкости соединения от свойств среды и др.
Электродный потенциал любого отдельного i-го участка паяного соединения может быть представлен в виде функционала:
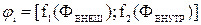 ,
,
где 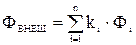 ;
; 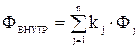 - функциональные зависимости, характеризующие суммарное влияние на электродный потенциал φ соответственно внешних и внутренних факторов.
- функциональные зависимости, характеризующие суммарное влияние на электродный потенциал φ соответственно внешних и внутренних факторов.
Достаточно четкое представление об ожидаемом поведении паяных соединений в заданных эксплуатационных условиях можно получить, используя электрохимические методы исследования коррозии. Они сводятся к нахождению электродных потенциалов участков соединений. В связи с наличием неоднородностей (металла, поверхности, напряженного состояния), вызванных воздействием процесса пайки, соединения характеризуются повышенной по сравнению с основным металлом электрохимической неоднородностью; при этом возможны различные соотношения между электродными потенциалами различных зон и, следовательно, различная стойкость против коррозионных разрушений.
Для определения величины местного электродного потенциала на электрохимически неоднородной поверхности соединения применяют капельный метод определения электродных потенциалов. Измеренные капельным методом потенциалы различных участков паяного соединения позволяют выделить анодные участки и определить тем самым ожидаемые зоны разрушения.
Капля раствора диаметром от 1 до 3 мм наносится на исследуемый участок поверхности и после выдержки её до установления более или менее стабильного значения потенциала φ производится его измерение в соответствии со схемой, приведенной на рис. 4.3. Время выдержки капли коррозионного раствора до установления стабильных значений φ определяется опытным путем. Например, установлено, что для алюминиевых сплавов оптимальное время выдержки капли 3%-ного водного раствора NaCl составляет 10…15 минут, а для сталей – 15…20 минут. С целью сопоставления полученных результатов для соединений одной и той же группы сплавов время выдержки под каплей раствора должно быть одно и то же. При измерениях электродных потенциалов в качестве электрохимического щупа, с помощью которого сканируют поверхность паяного соединения, широко используют хлорсеребряный электрод, обладающий постоянным и хорошо воспроизводимым потенциалом. При измерениях хлорсеребряный электрода помещают в специальный стакан и с помощью манипулятора перемещают носик электрода относительно поверхности образца (рис. 4.2).
3. МАТЕРИАЛЫ И ОБОРУДОВАНИЕ
Материалы
1. Нахлесточные паяные образцы меди, стали и алюминия.
2. KCl – насыщенный раствор.
3. NaCl – раствор.
Оборудование
1. Вольтметр универсальный ВК7 – 15.
2. Индикаторная головка часового типа.
3. Хлорсеребряный электрод.
4. Установка для измерения электродных потенциалов.
4. ПРОГРАММА РАБОТЫ
1. Ознакомиться с конструкцией и особенностями работы установки для измерения электродных потенциалов (рис. 4.1).
2. Ознакомиться с устройством, органами управления и работой вольтметра универсального ВК7-15 (см. прил. в конце раздела).
3. Подготовить прибор к измерениям.
4. Ознакомиться с особенностями образца и определить характерные зоны соединения.
5. Установить образец на столик установки.
6. Подвести кончик хлорсеребряного электрода к исследуемой зоне соединения и осуществить контакт электрода с поверхностью образца (рис. 4.2).
7. После выдержки участка поверхности под каплей раствора в течение 3 минут, произвести отсчет показаний по шкале стрелочного индикатора вольтметра.
8. Занести результат измерения в таблицу.
9. Поднять хлорсеребряный электрод при помощи манипулятора.
10. Осушить поверхность измерения фильтровальной бумагой.
11. Определить следующую зону измерения и повторить п.п. 6 – 10.
12. Построить эпюры распределения электродных потенциалов в характерных зонах соединения (рис. 4.3).
13. Определить зоны соединения, наименее стойкие в коррозионных средах, объяснить причины возникновения этих зон.
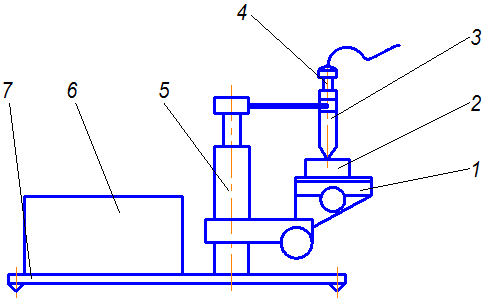
Рис. 4.1. Схема установки для измерения электродных потенциалов:
1 – манипулятор; 2 – образец; 3 – стакан; 4 – электрод хлорсеребряный;
5 – стойка; 6 – вольтметр универсальный В7-15; 7 – станина
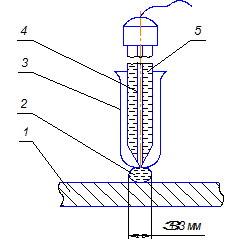
Рис. 4.2. Схема электрохимического шнура:
1 – образец; 2 – капля раствора; 3 – стакан; 4 – электрод хлорсеребряный; 5 – 3%-ный раствор NaCl
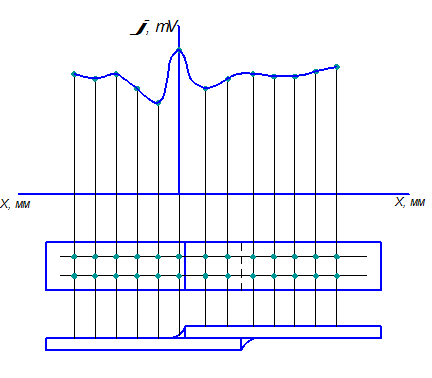
Рис. 4.3. Схема измерения электродных потенциалов
5. СОДЕРЖАНИЕ ОТЧЕТА
1. Цель работы.
2. Программа работы.
3. Описание установки для проведения исследований, краткая техническая характеристика блока измерений.
4. Особенности методики и результаты исследований.
5. Выводы.
6. ВОПРОСЫ ДЛЯ САМОКОНТРОЛЯ
1. Схема процесса электрохимической коррозии соединений.
2. Что такое «электродный потенциал»?
3. Характерные зоны паяного соединения.
Лабораторная работа № 3
ОПРЕДЕЛЕНИЕ ВЛИЯНИЯ ВНЕШНИХ РАСТЯГИВАЮЩИХ
НАПРЯЖЕНИЙ НА КОРРОЗИОННУЮ АКТИВНОСТЬ ПОВЕРХНОСТИ
ПАЯНЫХ СОЕДИНЕНИЙ
1. ЦЕЛЬ РАБОТЫ
Изучить методику определения электродных потенциалов поверхности паяных соединений под каплей электролита, углубить теоретические знания об особенностях коррозии различных типов соединений.
2. Особенности ЭЛЕКТРОХИМИЧЕСКОЙ коррозии
металлических материалов
Как показано Г.В.Акимовым, скорость коррозии (сила тока коррозионного элемента) определяется как:
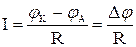 ,
,
где φА - потенциал анода при отсутствии тока;
φК - потенциал катода при отсутствии тока;
R - общее сопротивление процессу разрушения.
Величина числителя в этом уравнении является характеристикой термодинамической нестабильности данного коррозионного элемента (паяного соединения) и определяется видом неоднородностей этого элементa.
Роль растягивающих напряжений сводится прежде всего к созданию между отдельными микроучастками поверхности металла разности потенциалов Δφ, способствующих образованию коррозионных элементов «катод – анод». Эту разность потенциалов Δφ, можно рассматривать как электрохимический показатель склонности металлических материалов и соединений к коррозионному разрушению. Образование разности потенциалов при приложении растягивающих напряжений может происходить за счет выпадения новой фазы, разрушения защитной пленки и др. Некоторые исследователи считают, что смещение электродного потенциала φвотрицательную сторону при приложении растягивающих напряжении связано с увеличением свободной энергии металла.
Н.Д.Томашов отмечает, что наличие в металле механических напряжений (внешних или внутренних) приводит к изменению электрохимических характеристик (в том числе электродного потенциала φ)и скорости коррозии.
Ряд исследователей считает, что растягивающие напряжения способствуют смещению электродного потенциала φв отрицательную сторону. С течением времени потенциал напряженного металла становится более отрицательным, чем ненапряженного, причем с увеличением растягивающих напряжений (не превышающих предела текучести σ0,2 материала) смещение φ вотрицательную сторону увеличивается.
В ряде работ отмечается, что растягивающие напряжения оказывают незначительное влияние на интенсивность коррозии.
По данным Э.М. Гутмана изменение равновесного электродного потенциала при приложении механических напряжений зависит от абсолютной величины гидростатической части тензора напряжений (сжатия или растяжения):
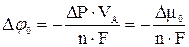 , (4.1)
, (4.1)
где Δφ0 – изменение стандартного электродного потенциала;
VА – объем грамм-атома металла;
n – валентность металла;
F – число Фарадея;
ΔР – избыточное гидростатическое давление;
Δμ – изменение химического потенциала.
В соответствии с формулой (4.1) смещение электродного потенциала в отрицательную сторону и, следовательно, облегчение процесса коррозионного разрушения связаны с увеличением химического потенциала. В области упругой деформации химический потенциал атомов металла увеличивается при приложении растягивающих и сжимающих напряжений. Отсюда следует, что скорость коррозии металла (и паяных соединении) также должна увеличиваться при приложении механических напряжений.
Технологически наиболее простым является способ, при котором контакт металла с электролитом обеспечивается через каплю электролита. Так как капля покрывает множество зерен металла, их границ, различных включений, дефектов кристаллической решетки и т.п., то измеренная величина электродного потенциала φоказывается усредненной, относящейся к макроскопическому участку, соответствующему размеру капли. Обычно диаметр капли электролита рекомендуют выдерживать в пределах от 1 до 3 мм.
Капельный метод особенно удобен в тех случаях, когда необходимо определить величину местного стационарного потенциала φ на электрохимически неоднородной поверхности. Капля электролита наносится на исследуемый участок поверхности и после выдержки до установления более или менее стабильного значения потенциала производится его измерение φ. Время выдержки капли коррозионного раствора до установления стабильных значений потенциалов определяется опытным путем. Не следует излишне увеличивать это время, так как происходит испарение воды и в связи с этим изменение концентрации электролита.
Электродный потенциал любого i-го участка соединения может быть представлен в виде функционала:
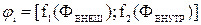 ,
,
где 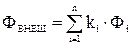 ;
; 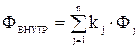 - функциональные зависимости, характеризующие суммарное влияние на электродный потенциал φсоответственно внешних и внутренних факторов.
- функциональные зависимости, характеризующие суммарное влияние на электродный потенциал φсоответственно внешних и внутренних факторов.
Для создания растягивающих напряжений при испытаниях на изгиб нагрузка прикладывается в двух точках на одинаковом расстоянии от опор (рис. 4.4).
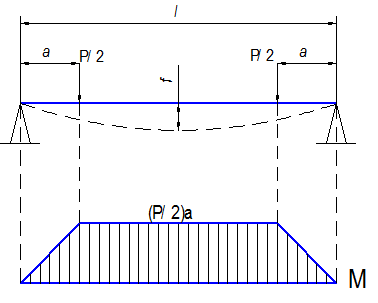
Рис. 4.4. Схема нагружения образца
Такая схема «чистого изгиба» во многих случаях обеспечивает достаточно надежные результаты, поскольку максимальный изгибающий момент в этом случае возникает на определенном участке длины образца, а не в одном сечении.
В широких образцах (с отношением ширины к высоте сечения более трех) создается двухосное напряженное состояние из-за затруднения поперечной деформации. Нижняя часть образца оказывается растянутой, верхняя - сжатой. Максимальные напряжения возникают вблизи поверхности.
При работе металла в упругой стадии можно вычислить возникающие в нем напряжения и деформации по обычным формулам сопротивления материалов. Для определения нормальных напряжений в крайних точках сечения пользуются формулой:
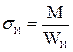 ,
,
где σИ - нормальные напряжения от изгиба в точке, наиболее удаленной от
центральной оси сечения;
WИ - момент сопротивления сечения.
Для прямоугольного сечения:
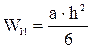 ,
,
где а – ширина;
h – высота сечения.
Стрела прогиба f (рис. 4.4) связана с относительным удлинением δкрайнего растянутого волокна в изогнутом образце зависимостью:
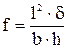 . (4.2)
. (4.2)
На образцах в специальной скобе (рис. 4.5) можно создавать различные
уровни напряжений, изменяя стрелу прогиба. Применение вкладыша позволяет создать более равномерное распределение напряжений по рабочей длине образца. В этом случае нагрузка прикладывается к образцу в двух точках.
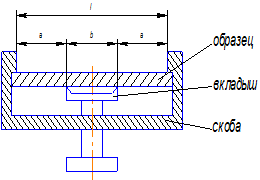
Рис. 4.5. Скоба нагружающая
Стрелу прогиба определяют экспериментально при помощи измерительной головки часового типа или расчетом как:
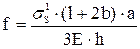 , (4.3)
, (4.3)
где Е - модуль упругости;
b -расстояние между внутренними опорами;
l - расстояние между внешними точками опоры;
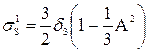 ;
;
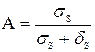 ;
;
a=(l – b)/2;
δs – 0,002;
σs –предел текучести;
h – толщина образца.
При нагружении по схеме чистого изгиба упругие растягивающие напряжения образца прямоугольного сечения рассчитывают по формуле:
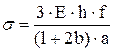 . (4.4)
. (4.4)
Рабочие напряжения рассчитывают как часть предела текучести при из- гибе 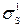 ( 0,90; 0,75; 0,50 и т.д.).
( 0,90; 0,75; 0,50 и т.д.).
3. МАТЕРИАЛЫ И ОБОРУДОВАНИЕ
Материалы
1. Нахлесточные паяные образцы меди, стали и алюминия.
2. KCl – насыщенный раствор.
3. NaCl – раствор.
Оборудование
1. Нагружающее устройство.
2. Вольтметр универсальный ВК7 – 15.
3. Индикаторная головка часового типа.
4. Хлорсеребряный электрод.
5. Установка для измерения электродных потенциалов.
4. ПРОГРАММА РАБОТЫ
1. Изучить конструкцию и особенности работы установки для измерения электродных потенциалов (рис. 4.6).
2. Ознакомиться с устройством, органами управления и работой вольтметра универсального ВК7 – 15 (см. прил. в конце раздела).
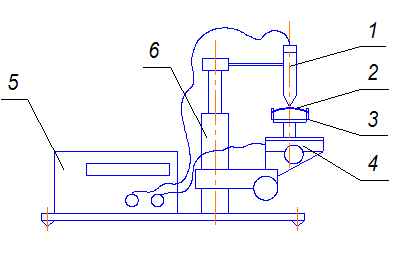
Рис. 4.6. Схема установки для измерения электродных потенциалов:
1 – электрод хлорсеребряный; 2 – образец; 3 – скоба; 4 – манипулятор;
5 – прибор измерительный; 6 – стойка
3. Подготовить измерительный прибор.
4. Подготовить поверхность изучаемого образца к проведению исследований.
5. Определить геометрические характеристики образца (рис. 4.7). Материал образца - сплав МНЖМц 30 - 0,8 - 1 (табл. 4.2).
6. Поместить образец в нагружающее устройство (рис. 4.8).
7. Установить нагружающее устройство с образцом на столик установки (рис. 4.6).
8. Подвести хлорсеребряный электрод к исследуемой зоне соединения и осуществить контакт электрода с поверхностью образца (рис. 4.9).
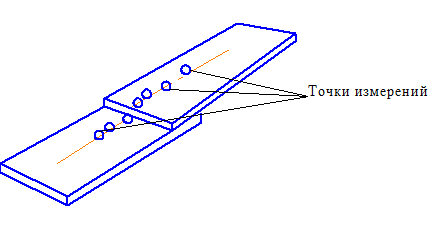
Рис. 4.7.Образец для испытаний
Таблица 4.2
Химический состав (в %) и механические свойства (в отожженном состоянии) медно-никелевого сплава МНЖМц 30 - 0,8 - 1
 Ni Ni
| Fe | Мn | Сu | σв кг/мм2 | σ0,2 кг/мм2 | δ, % | Е·10-3, кг/см2 (20 ºС) |
| 29... 33 | 0,6..1,0 | 0,8..1,3 | ост. |
9. Определить время установления стационарного значения электродного потенциала φ;представить результаты измерений в координатах φ – t (t – продолжительность измерений) (рис. 4.10). Количество измерений не менее пяти.
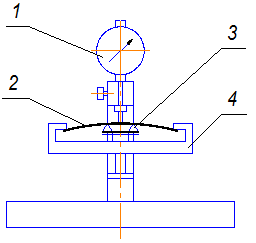
Рис. 4.8. Нагружающее устройство:
1 – головка измерительная часового типа;
2 – образец; 3 – вкладыш; 4 – скоба
10. Поднять измерительный электрод с помощью манипулятора (рис. 4.6).
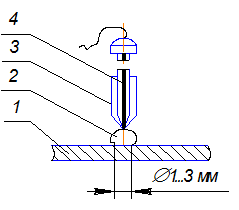
Рис. 4.9. Схема измерительного электрода: 1 – образец;
2 – капля раствора; 3 – чехол защитный; 4 – электрод хлорсеребряный
11. Осушить поверхность измерения фильтровальной бумагой.
12. Снять нагружающее устройство со столика измерительной установки.
13. Используя зависимости (4.3) и (4.4), определить величину прогиба f образца, соответствующую механическим растягивающим напряжениям величиной 0,7 от предела текучести материала образца.
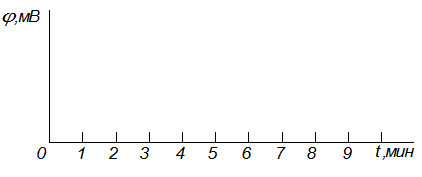
Рис. 4.10. Продолжительность установления стационарного электродного
потенциала
14. С учетом п. 13 создать в поверхностных объемах образца механические напряжения при помощи нагружающего устройства (рис. 4.8).
15. Установить нагружающее устройство с образцом на столик измерительной установки.
16. Определить величины электродного потенциала φ в соответствующих характерных зонах образца (рис. 4.7) (продолжительность измерения выбирать с учетом предварительно полученных результатов (п. 9 и рис. 4.10).
17. Результаты измерений представить в виде таблицы.
18. Снять нагружающее устройство со столика измерительной установки.
19. Очистить поверхность образца от загрязнений.
20. Создать в поверхностных слоях образца растягивающие напряжения величиной 1,2 от предела текучести материала образца.
21. Повторить пункты 15...19 программы работ.
22. Разгрузить образец в нагружающем устройстве и снять его с приспособления.
23. Привести в порядок рабочее место.
24. Построить эпюры распределения электродных потенциалов в характерных зонах соединения при различных уровнях механических напряжений σ=0; σ=0,7 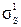 и 1,2
и 1,2 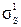 (
( 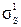 - предел текучести при изгибе материала образца).
- предел текучести при изгибе материала образца).
Дата добавления: 2015-01-29; просмотров: 1225;
