Особенности описания микрочастиц
Корпускулярно-волновой дуализм свойств материи.
Одной из наиболее спорных проблем в истории естествознания была проблема природы лучистой энергии – электромагнитного излучения. Взгляды физиков на природу света (волна или поток частиц), начиная с Исаака Ньютона (Newton), периодически менялись. К концу XIX века общепринятым считалось, что электромагнитное излучение имеет волновую природу. Однако к началу XX века встала проблема описания явления излучения света нагретыми телами. Не удавалось создать на основе классической электродинамики модель, объясняющую излучательную способность нагретых тел. Макс Планк (Planck) предложил гипотезу о квантовой природе процесса излучения (1900), согласно которой излучение энергии нагретым абсолютно черным телом происходит не непрерывно, как того требовала классическая теория, а дискретными порциями – квантами. Минимальная энергия – величина энергии кванта – пропорциональна частоте излучения:
E = h×n,
где h = 6,6262×10-34 Дж×с – постоянная Планка, n – частота излучения, с-1.
Альберт Эйнштейн (Einstein) высказал предположение о том, что идея квантования энергии относится не только к процессам поглощения и испускания света нагретыми телами, но и к излучению как таковому. То есть электромагнитное излучение распространяется в виде дискретных частиц с энергией E = hn, названых впоследствии фотонами. Такие радикальные изменения во взглядах на природу света, предложенные Планком и Эйнштейном, нашли экспериментальное подтверждение в исследовании фотоэффекта – испускания электронов веществом под действием света. И особенно корпускулярные свойства электромагнитного излучения проявились в рассеянии рентгеновского излучения различными веществами – эффект Комптона, все особенности которого можно объяснить упругим столкновением фотонов рентгеновского излучения со слабосвязанными электронами.
Таким образом, поток электромагнитного излучения, с одной стороны, является волной, что наблюдается при интерференции и дифракции, а с другой стороны, – потоком частиц, что экспериментально проявляется в процессах испускания, поглощения и рассеяния излучения твердыми телами.
Используя выражение Планка для энергии кванта излучения и формулу Эйнштейна, показывающую взаимосвязь энергии частицы и ее массы (E = mc2), можно связать характеристики фотона (масса, импульс) и характеристики волны (длина волны и частота):
E = hn E = mc2 ® hn = mc2
n = c/l ® hc/l = mc2 ® m = h/cl ® l = h/mc
p = m×c ® 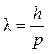 ;
;
h – постоянная Планка; n – частота излучения; m – масса фотона, кг; c– скорость света в вакууме; l – длина волны излучения, м; p – импульс фотона.
Так все же фотон – волна или частица? Скорее всего, сущность этой проблемы связана с ограниченностью наших жизненных представлений. Мы живем в макромире, где только по отдельности встречаются процессы, имеющие корпускулярную и волновую природу. Нигде в повседневной жизни мы не встречаемся с движением, которое было бы результатом наложения этих двух форм, но это не значит, что его не существует. Из этой дилеммы возник совершенно новый подход к описанию физических и химических процессов микромира.
В 1924 г. Луи де Бройль (de Broglie) выдвинул гипотезу о том, что корпускулярно-волновой дуализм свойственен не только электромагнитному излучению, а является общим свойством материи. При этом он ввел понятие о волнах материи. Так, любому материальному объекту, обладающему массой m и движущемуся со скоростью v, соответствует волновой процесс с длиной волны l. По аналогии с электромагнитным излучением, где l=h/p, длина волны частицы (часто называется длиной волны де Бройля) вычисляется по уравнению
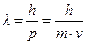 .
.
Так, электроны, испускаемые нагретым катодом, разгоняются в электрическом поле напряжением » 100 В, приобретают кинетическую энергию »100 эВ. При этом в случае, если формула де Бройля верна, электронам должна соответствовать длина волны 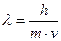 .Если
.Если 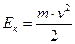 , то
, то 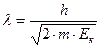 . При Eк = 100 эВ,l = 1,2 Å.
. При Eк = 100 эВ,l = 1,2 Å.
Если электроны обладают волновыми свойствами, то их пучок должен испытывать дифракцию на дифракционной решетке, постоянная которой a соизмерима с длиной волны электрона (постоянная решетки − сумма ширины щели и ширины промежутка между щелями). Так как длина волны электрона мала (l=1.2 Å), то роль дифракционной решетки, у которой a » l, могут играть кристаллические плоскости монокристаллов. В частности, была использована металлическая фольга (никель). Причем положение дифракционных полос должно определяться условием Уильяма Брэгга (Bragg): n×l = 2×a×sinJ (n − номер дифракционной полосы; J − угол, под которым пучок электронов попадает на дифракционную решетку).
Экспериментальное подтверждение волновых свойств электрона было получено в 1927 г. Клинтоном Девиссоном (Devisson) и Лестером Джермером (Gemmer) и независимо от них Джоржем Томсоном (Thomson) (1928 г.) в опытах по рассеянию электронов. Действительно, при пропускании пучка электронов через металлическую фольгу была получена дифракционная картина в виде концентрических колец, положение которых изменялось в зависимости от кинетической энергии электронов (ускоряющего напряжения) – их длины волны, согласно условию Брэгга (рис. 2.2).
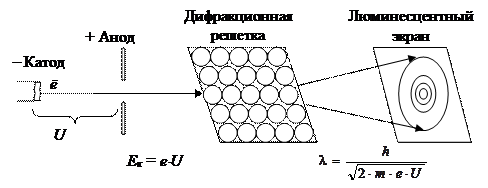 |
Рис. 2‑2 Схема опыта дифракции электронов: U (В) – напряжение ускоряющего электрического поля
Позднее наблюдали дифракцию и более тяжелых частиц, например протонов, нейтронов, атомов гелия.
Можно предположить, что и движению макрообъекта соответствует также волновой процесс. Движению тела массой m = 1г со скоростью v=1см/с соответствует волновой процесс с длиной волны l=6,6×10-29м. Но нет таких дифракционных решеток, чтобы наблюдать этот процесс.
Корпускулярно-волновой дуализм свойств электрона,как и других микрообъектов, является первым фундаментальным положением, на котором строится волновая механика – механика объектов атомных и субатомных размеров.
Принцип неопределенности
Вторым фундаментальным положением, на котором строится волновая механика, является принцип неопределенности Гейзенберга. Поскольку электрон обнаруживает одновременно свойства волны и частицы, возникают трудности, связанные с измерением корпускулярных свойств электрона, а именно одновременного определения координат и импульса электрона.
Вернер Гейзенберг (Heisenberg) в 1927 г. сформулировал следующее положение: для микрочастицы невозможно одновременно точно определить ее координаты и импульс. Ограничения в точности определения даются соотношением Гейзенберга:
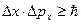 ,
, 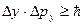 ,
, 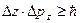 ,
, 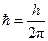 – постоянная Планка.
– постоянная Планка.
Из принципа неопределенности следует вероятностный подход к описанию механики микрообъектов. Точное определение координат частицы и ее импульса заменяется определением вероятности нахождения частицы в какой-то области пространства. Для движущейся частицы с вполне определенной энергией, а следовательно, и импульсом мы не можем указать точные значения координат (траектории движения), а можем говорить лишь о вероятности нахождения ее в какой-либо части пространства.
Вероятностный характер механики микрочастиц следует также из опытов по дифракции электронов. Если пропускать не поток, а последовательно по одному электрону, то каждый из них попадет в какое-то определенное место экрана и дифракционной картины не будет. В какое конкретное место попадет следующий электрон, мы не знаем, но знаем, где вероятность его появления максимальна (кольцо) и где минимальна (между кольцами) рис. 2.2. И только большое число электронов, пропущенных последовательно друг за другом, создадут на экране дифракционную картину.
Основные понятия волновой механики
Волновое уравнение
Уравнение, которое будет описывать движение электрона, должно удовлетворять следующим требованиям: отражать волновой характер движения электрона и содержать характеристики электрона как частицы.
Для описания волновых свойств электрона можно использовать известное из математики и физики дифференциальное уравнение второго порядка (уравнение волнового процесса):
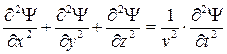 ,
,
v – скорость распространения волны.
Y(x,y,z,t) – пси-функция – волновая функция, которая зависит от координат и времени и может быть представлена в виде синуса, косинуса, экспоненты или любой другой функции, являющейся решением дифференциального уравнения волнового процесса.
Для простоты написания левую часть уравнения представляют обычно в операторной форме:
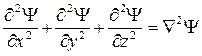
где 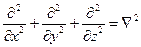 – оператор Лапласа (читается "набла два"), тогда волновое уравнение приобретает вид:
– оператор Лапласа (читается "набла два"), тогда волновое уравнение приобретает вид:
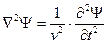 .
.
Чаще всего интерес представляют стационарные процессы (стоячие волны). Описывающее их уравнение содержит функцию, не зависящую от времени. Для стоячей волны уравнение имеет вид:
Ñ2Y(x,y,z) + (4p2n2/v2)×Y(x,y,z) = 0.
Поскольку частота волнового процесса (ν) равна скорости распространения волны (v), деленной на длину волны: 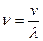 , и соответственно
, и соответственно 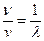 , то
, то
Ñ2Y(x,y,z) + (4p2/l2) ×Y(x,y,z) = 0
В полученном уравнении, используя соотношение де Бройля, можно заменить длину волны такими характеристиками частицы, как масса и кинетическая энергия.
Длина волны де Бройля 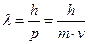 .
.
Кинетическая энергия электрона 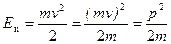 ,
,
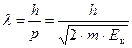 ,
, 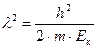
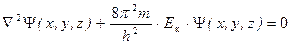 .
.
Как правило, при описании состояния электрона определяют его полную энергию. Поскольку кинетическая энергия электрона (Eк) равна разности между полной (E) и потенциальной энергией (V): Eк = E – V, то можно записать
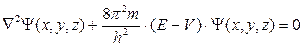 .
.
Таким образом, получают волновое уравнение, независимое от времени, содержащее в качестве параметра массу электрона. Это уравнение известно как уравнение Шрёдингера, названное по имени австрийского физика Эрвина Шрёдингера (Schrödinger), который его предложил в 1926 г. для описания состояния микрочастицы в потенциальном поле.
Прежде чем решать уравнение Шрёдингера для конкретных систем, выясним физический смысл волновой функции. Раскрыть его достаточно непросто, поскольку в макромире нет аналогий корпускулярно-волновым свойствам микрообъектов. И до некоторой степени волновая функция представляет собой математическую абстракцию.
В 1926 г. Макс Борн (Born), применив вероятностные идеи принципа неопределенности, дал общепринятую в настоящее время трактовку физического смысла волновой функции: квадрат волновой функции пропорционален вероятности нахождения (dP) частицы в элементарном объеме (dV).
dP = Y2(x,y,z)×dV.
Примечание. В общем случае, если Y-функция комплексная величина, вероятность нахождения частицы (dP) в элементарном объеме (dV) пропорциональнаквадрату ее модуля: dP = |Y|2×dV = Y*∙Y×dV
Величина 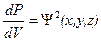 называется плотностью вероятности и характеризует вероятность нахождения частицы в элементарном объеме пространства с координатами x,y,z. Для электрона ее часто называют электронной плотностью.
называется плотностью вероятности и характеризует вероятность нахождения частицы в элементарном объеме пространства с координатами x,y,z. Для электрона ее часто называют электронной плотностью.
Вероятность нахождения частицы в каком-либо конечном объеме V равна интегралу квадрата волновой функции по данному объему:
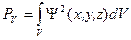 .
.
Вероятность должна выражаться действительным положительным числом, меньшим или равным единице. Сама же волновая функция может быть положительной, отрицательной или мнимой, поэтому в общем виде используется не ее квадрат волновой функции, а произведение комплексно сопряженных функций.
Вероятностное толкование физического смысла волновой функции является одним из постулатов квантовой механики. Правомерность такой интерпретации подтверждается соответствием экспериментально определенного взаимного расположения атомов в молекулах и квантово-механического расчета.
Из условия, что вероятность события не может быть больше единицы, следует принцип нормирования волновых функций. Вероятность нахождения частицы во всем рассматриваемом объеме должна быть равна единице (частица находится в этом объеме – событие достоверное):
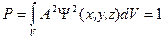 ,
,
А – нормирующий множитель, коэффициент, входящий в волновую функцию, который подбирается таким образом, чтобы выполнялось условие нормировки.
1.5.2 Решение уравнения Шрёдингера для простейших случаев
Решение уравнения Шрёдингера даже для относительно простых реальных объектов, таких как атомы и молекулы, содержащих два и более электронов представляет собой сложную математическую задачу. Для того чтобы понять характер и особенности результатов квантово-механического описания состояния электрона в атомах и молекулах, решим строго простейшую задачу нахождения электрона в так называемом "потенциальном ящике" – некоторой ограниченной области пространства, вне которой потенциальная энергия электрона обращается в бесконечность. Электрон не может покинуть пределы "потенциального ящика", то есть находится в связанном состоянии. Это, по сути своей, является моделью нахождения электрона в атоме.
Электрон в одномерном потенциальном ящике.
Рассмотрим состояние электрона в одномерном потенциальном ящике.
Движение электрона происходит только вдоль оси X (рис. 2.3). Внутри ящика потенциальная энергия частицы принимается равной нулю (потенциальную энергию можно отсчитывать от любого выбранного уровня), вне его она равна бесконечности, то есть частица находится внутри ящика и не может покинуть его пределы.
С точки зрения классической механики частица, находящаяся в потенциальном ящике, может иметь в принципе любую энергию и находиться в любой точке ящика. При квантово-механическом рассмотрении ситуация меняется. Состояние электрона описывает уравнение Шрёдингера, и его характеристики (энергия и вероятность нахождения в пространстве) получают при решении этого уравнения.

Рис. 2‑3. Электрон в одномерном потенциальном ящике: a − параметр (размер) потенциального ящика
Как и любое дифференциальное уравнение, уравнение Шрёдингера имеет бесконечное множество решений, но физический смысл имеют лишь некоторые из них. В нашем случае волновая функция описывает реальную физическую систему, поэтому она должна соответствовать определенным условиям:
конечность – вероятность нахождения электрона в пространстве не может быть больше единицы;
однозначность – вероятность нахождения электрона в точке однозначна;
непрерывность – нет особых точек в пространстве.
Поскольку электрон находится внутри одномерного «ящика» (V=0), уравнение Шрёдингера приобретает вид
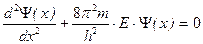 .
.
Известно, что решением данного типа уравнения может быть функция 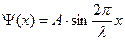 – общее решение. В принципе вид функции может быть и другим.
– общее решение. В принципе вид функции может быть и другим.
Используя общее решение, граничные условия нашей задачи и принцип нормировки, можно получить волновую функцию, описывающую состояние электрона в потенциальном ящике.
Граничными условиями является равенство волновой функции нулю на стенках: 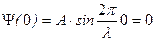 ,
, 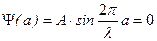 .
.
Поскольку амплитуда волновой функции не равна нулю, то из второго условия следует:
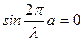 ,
, 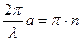 , n=1,2,3…,
, n=1,2,3…, 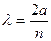 ,
, 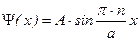 .
.
Значение амплитуды А находят из условия нормировки. Поскольку электрон находится в потенциальном ящике, то интеграл квадрата волновой функции по координате ящика (от 0 до a) равен единице:
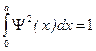 ,
, 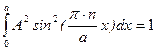 ,
, 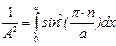 ,
,
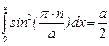
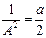
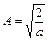
Таким образом, выражение для волновой функции электрона в одномерном потенциальном ящике имеет вид
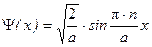 ,
,
где a – параметр потенциального ящика; n = 1,2,3…– целочисленный параметр. То есть состоянию электрона в потенциальном ящике соответствует набор волновых функций, отличающихся целочисленным параметром n, называемым квантовым числом.
Для определения энергии электрона проделаем следующие математические операции.
1. Поскольку в уравнение Шрёдингера входят волновая функция, и ее вторая производная, запишем их:
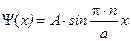 ,
,
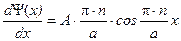 ,
,
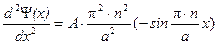 .
.
2. Подставим выражения волновой функции и ее второй производной в уравнение Шрёдингера, описывающее состояние электрона внутри потенциального ящика:
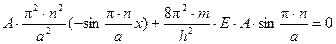 ,
,
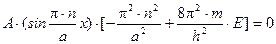 .
.
3. Поскольку волновая функция внутри ящика не равна нулю ( 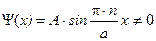 ), то
), то 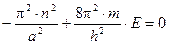 , и
, и
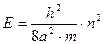 , n=1,2,3…
, n=1,2,3…
Следовательно,набору волновых функций соответствует набор величин энергий (рис.2.4).
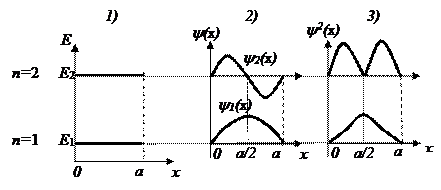
Рис. 2‑4. Первое и второе энергетическое состояние электрона в одномерном потенциальном ящике. Полная энергия Еi (1), соответствующая ей волновая функция Yi(x) (2) и плотность вероятности Yi2(x) (3) электрона
Из полученных результатов решения следуют особенности квантово-механического описания состояния электрона в потенциальном ящике:
1. Электрон, находясь в потенциальном ящике, может иметь только дискретные значения полной энергии E1, E2, E3…, величины которых определяет целочисленный параметр n = 1,2,3…, называемый квантовым числом. То есть энергия связанного электрона квантована.
2. Распределение вероятности нахождения электрона в объеме потенциального ящика (плотность вероятности) определяется его энергией.
3. Величина энергии и соответствующая ей волновая функция, характеризующая распределение вероятности нахождения электрона в объеме (Еi -Yi), определяют энергетическое состояние электрона. Каждому энергетическому состоянию соответствует квантовое число (n).
Электрон в трехмерном потенциальном ящике. Вырожденные энергетические состояния.
Задача о нахождении частицы в трехмерном потенциальном ящике аналогична предыдущей задаче. Граничные условия полностью совпадают: волновая функция на границах ящика обращается в ноль, потенциальная энергия внутри ящика равна нулю (V=0), а за пределами ящика – бесконечности (V=¥), то есть частица не может покинуть потенциальный ящик. Единственным отличием является то, что волновая функция является функцией трех пространственных координат: Y(x,y,z).
Уравнение Шрёдингера для данного случая представляет собой дифференциальное уравнение в частных производных с тремя переменными:
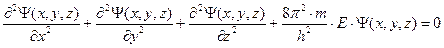 .
.
Стандартным приемом, которым пользуются при решении такого типа уравнений, является разделение переменных: представление волновой функции в виде произведения трех функций, каждая из которых зависит только от одной координаты:
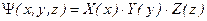 ,
,
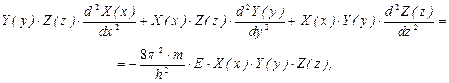
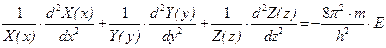 .
.
Поскольку правая часть уравнения не зависит от координат, то можно представить полную энергию электрона как сумму трех энергий: E=Ex+Ey+Ez. Уравнение Шрёдингера при этом преобразуется в три дифференциальных уравнения, аналогичных волновым уравнениям электрона в одномерном ящике, решение которых уже получено:
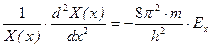 ,
,
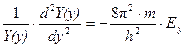 ,
,
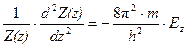 .
.
Для волновой функции:
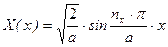 ,
, 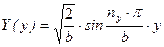 ,
, 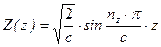 ,
,
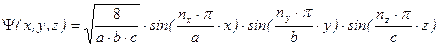 ,
,
a,b,c – параметры трехмерного потенциального ящика (размеры – длина, ширина, высота); nx, ny, nz – целочисленные параметры – «квантовые числа». Необходимо отметить, что каждой координате соответствует свое квантовое число.
Для энергии:
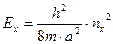 ,
, 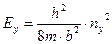 ,
, 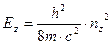 ,
,
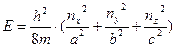 .
.
Из полученных результатов решения следует:
1. Энергия электрона в трехмерном потенциальном ящике квантована.
2. Каждое энергетическое состояние электрона определяется набором из трех квантовых чисел.
Однако в реальных системах часто встречается ситуация, когда определенное энергетическое состояние (энергия частицы) может быть описано не единственным набором квантовых чисел, то есть более чем одной волновой функцией. Тогда говорят о вырождении энергетического состояния.
Проиллюстрировать явление вырождения по энергии можно на примере частицы в трехмерном потенциальном ящике. Если рассмотреть энергетические состояния частицы в ящике, который представляет собою куб (а=b=c), то выражение для энергии приобретает вид
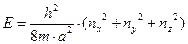
а – параметр куба (величина ребра).
 Составим энергетическую диаграмму состояния частицы в таком ящике, откладывая по вертикальной оси энергию частицы в единицах
Составим энергетическую диаграмму состояния частицы в таком ящике, откладывая по вертикальной оси энергию частицы в единицах 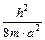 (рис.2.5).
(рис.2.5).
Рис. 2‑5. Энергетическая диаграмма электрона в трехмерном потенциальном ящике: [nx, ny, nz] – набор квантовых чисел, соответствующий данному энергетическому состоянию
В кубическом потенциальном ящике почти все энергетические состояния в той или иной степени вырождены. Степень вырождения − число вариантов наборов квантовых чисел (число волновых функций), при помощи которых можно описать данное энергетическое состояние. Снятие вырождения является важной проблемой квантово-механического описания системы. В случае трехмерного потенциального ящика вырождение снимается частично (a=b¹c) или полностью (a¹b¹c) при изменении параметров ящика. В реальных системах проблема снятия вырождения является более сложной проблемой.
Энергетическое состояние электрона в кулоновском поле ядра достаточно близко соответствует ситуации нахождения электрона в трехмерном потенциальном ящике. Поэтому все закономерности, которые были получены, а главное дискретность энергетических состояний, распространяются и на атом.
Дата добавления: 2017-02-20; просмотров: 1288;
