Лекция 4. Концентрации растворов
Ключевые слова: массовая доля растворенного вещества, молярная концентрация, молярная концентрация эквивалента, эквивалент вещества, молярная масса эквивалента, фактор эквивалентности, титр вещества, титр по определяемому веществу, поправочный коэффициент.
Важной характеристикой любого раствора является его концентрация. Под концентрацией раствора понимают количество вещества, растворенного в единице объема или массы раствора. В титриметрии используют следующие способы выражения концентраций.
1. Массовая доля растворенного вещества (ω(B)) показывает, сколько граммов растворенного вещества B содержится в 100 г раствора, определяется как отношение массы данного вещества в растворе (m(B)) к общей массе раствора m, выражается либо в долях (безразмерная величина), либо в процентах:
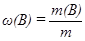 или
или 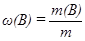 ∙100%.
∙100%.
2. Молярная концентрация (СМ(B))– показывает, сколько молей растворенного вещества содержится в 1 л раствора, рассчитывается как отношение количества растворенного вещества в молях (n(B)) к объему раствора (V) в литрах (моль/л; М):
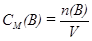 .
.
3. Молярная концентрация эквивалента(нормальная концентрация) (NB = СН(B)=С(1/z·B) показывает, сколько молей эквивалентов растворенного вещества (B) содержится в 1 л раствора, рассчитывается как отношение количества эквивалентов вещества к объему раствора (моль/л, н.):
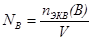 ,
,
где nэкв(В) - количество эквивалентов вещества B.
Эквивалентвещества - реальная или условная частица вещества, которая может присоединять, высвобождать или быть каким-нибудь другим образом эквивалентна одному иону водорода в кислотно-основных реакциях или одному электрону в окислительно-восстановительных реакциях.
Молярной массой эквивалента вещества – М(ЭВ) - называют массу одного моля эквивалента этого вещества, она рассчитывается по формуле
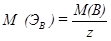 , и следовательно
, и следовательно 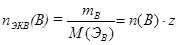 ,
,
где 1/z = fэкв – фактор эквивалентности – число, показывающее, какая доля реальной частицы соответствует 1 иону водорода или 1 электрону в данной реакции; fэкв – безразмерная величина, причем fэкв ≤1, например:
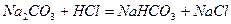 ;
; 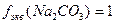 ,
, 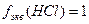 ,
,
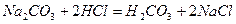 ;
; 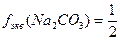 ,
, 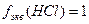 ,
,
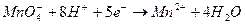 ;
;  (кислая среда).
(кислая среда).
Количество эквивалентов вещества выражают в молях, а М(Э) – в г/моль.
Дата добавления: 2016-09-20; просмотров: 1645;
