Шунтирующие операции
Началом хирургического лечения портальной гипертензии считают конец XIX века, когда стали разрабатываться два направления - сосудистый портокавальный анастомоз - Н.В. Экк и метод оментопексии - A.S. Talma.
В 1877 году Н.В. Экк в эксперименте разработал сосудистый портокавальный анастомоз. Пять лет спустя, в 1882 г., E. Vidal впервые успешно выполнил портокавальный анастомоз «конец-в-бок» у больного с кровотечением из вен пищевода. Кровотечение было остановлено.
В 1947 г. R.R. Linton предложил проксимальный спленоренальный анастомоз для лечения больных циррозом печени. Положительным моментом операции являлось радикальное устранение гиперспленизма. Однако у больных очень быстро нарастала печеночная недостаточность.
Blakemore в 1948 г. описал использование аутовенозной вставки для создания Н-образного портокавального анастомоза, который в меньшей степени, чем прямой вызывал уменьшение портальной перфузии печени.
В последующие годы в мировой практике получили распространение так называемые парциальные сосудистые портокавальные анастомозы. Основная идея этих операций - это ограничение диаметра создаваемого портокавального соустья.
В номенклатуре обозначений и терминологии применяются анатомическое и таксаномическое (комбинация функционального и анатомического) обозначения. При анатомическом обозначении принципиальными шунтирующими процедурами являются портокавальное, мезентерикокавальное и спленоренальное шунтирование. При этом первая часть слова указывает на донорский сосуд, вторая – принимающий сосуд. Такое обозначение вариантов шунтирования является не полным, поскольку не отражает функциональные свойства шунта.
Таксономическая номенклатура использует более понятный хирургический лексикон. В нем заключено обозначение места наложения шунта – центрально или дистально и селективно или неслективно. Центральное шунтирование предусматривает использование в качестве донорского сосуда портальную вену (портокавальный шунт). При дистальном шунтировании в качестве донорского сосуда используются притоки v.portae (спленоренальный или мезентерикокавальный).
При наложении селективного шунта достигается задача декомпрессии варикозных расширенных пищеводных вен путем отведения крови из бассейна брыжеечных вен. Неселекстивный шунт отводит кровь из портальной системы в нижнюю полую вену. Селективными шунтами является дистальный спленоренальный шунт и Н-шунт малого диаметра между портальной и нижней полой венами. Неселективными шунтами являются портокавальные шунты бок-в-бок и конец-в-бок, мезентерикокавальный и проксимальный спленоренальный шунты.
Принятым обозначением селективного шунта называть дистальный спленоренальный шунт. Названия вариантов шунтов имеют аторские синонимы. Например, дистальный спленоренальный шунт (Warren и Millican, 1981), проксимальый спленоренальный шунт (Linton), мезентерикокавальный шунт (Clatworthy, 1975), мезентерикокавальный шунт с использованием протеза из дакорона (Drapans, 1975) и портокавальный шунт с применением протеза из PTFE (Sarfen, 1986). У неселективных шунтов имеется два важнейших недостатка – прогрессирование печеночной недостаточности и энцефалопатия. Селективное отведение части крови от варикозных вен пищевода без полного выключения или значимого выключения венозного кровотока сохраняет функцию печени и снижает риск развития энцефалопатии.
Портокавальное шунтирование - осуществляет сброс крови из системы воротной вены в систему нижней полой вены, что приводит к снижению портального давления. Портокавальный анастомоз конец в бок - воротную вену пересекают с перевязкой проксимального участка, а дистальный вшивают в нижнюю полую вену (рис. 355)
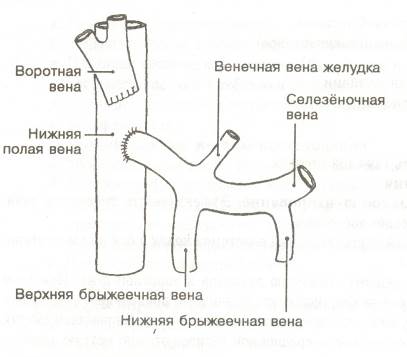
Рис. 355. Портокавальный анастомоз конец в бок (Bruce E. Jarrell, 1997)
Мезентерикокавальный шунт(Clatworthy,1975) выполняется наложением анастомоза между проксимальным отделом нижней полой вены и верхней брыжеечной веной. В 1975 году Drapans предложил накладывать анастомоз с помощью Н-образного шунта (рис. 356). Он формируется при помощи сосудистого протеза диаметром 16-18 мм между верхней брыжеечной и нижней полой венами
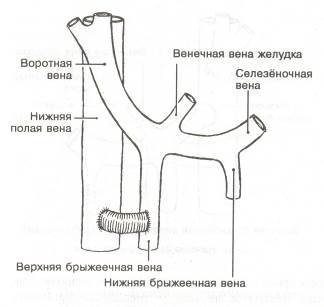
Рис. 356. Мезентерикокавальный Н-образный анастомоз (Bruce E. Jarrell, 1997)
Дистальный спленоренальный шунт –селективный портосистемный анастомоз. Предложил и технически разработал Warren в конце 60-х годов (рис. 357). Отток крови из варикозных расширенных вен пищевода происходит из коронарной вены, далее в селезеночную вену, затем через анастомоз в левую почечную и нижнюю полую вены.
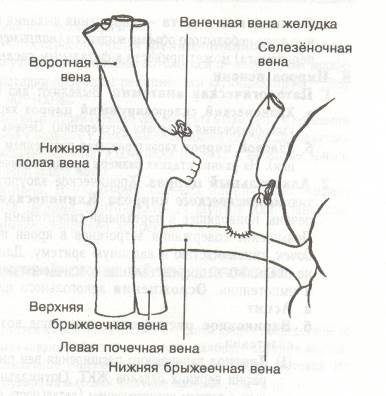
Рис. 357. Спленоренальный анастомоз Уоррена (Bruce E. Jarrell, 1997).
Эндоваскулярное лечение, как и открытая хирургическая операция, направлено на снижение давления в воротной вене. К ним относится эндоваскулярный метод - TIPS (Transjugular Intrahepatic portosystemic Shunts) - Трансъюгулярное Интрапеченочное Портосистемное Шунтирование*.
(* ссылка – Материалы по - TIPS (Transjugular Intrahepatic portosystemic Shunts) взяты с Электронного ресурса. Интернет-сайта «отделения рентгенохирургии российского государственного медицинского университета»)
TIPS является альтернативой хирургическим методам лечения портальной гипертензии и имеет ряд преимуществ перед достаточно тяжелыми хирургическими шунтирующими операциями. Они менее травматичны и малоинвазивны. TIPS может сочетаться с другими эндоваскулярными методиками - эмболизация варикознорасширенных вен пищевода и желудка, эмболизация печеночной артерии и др.
Для TIPS (ТИПС) существуют строго определенные показания:
1. Портальная гипертензия.
2. Острое кровотечение из варикозно-расширенных вен пищевода и желудка.
3. Повторное пищеводно-желудочное кровотечение.
4. Рефрактерный асцит (асцит неподдающийся медикаментозной терапии).
5. Печеночный гидроторакс (скопление асцитической жидкости в плевральной полости).
6. Синдром Бадда-Киари (сдавление нижней полой вены в инфраренальном отделе узлами регенератами).
Трансъюгулярное интрапеченочное портосистемное шунтирование (TIPSS). TIPSS выполняется под местной анестезией, через прокол на коже в области шеи, не требует широких разрезов, как при хирургической операции, и позволяет избежать использование эндотрахеального наркоза. Доступом через правую внутреннюю яремную вену, расположенную на боковой поверхности шеи, производят катетеризацию одной из печеночных вен, как правило средней печеночной вены (рис. 358). Из ее просвета иглой Rosch, через печеночную паренхиму, выполняют пункцию левой ветви воротной вены и затем катетеризацию последней. Измеряют градиент давления между воротной и печеночной венами.
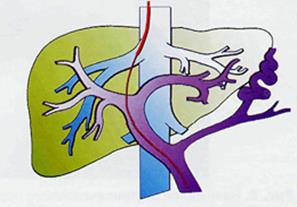
Рис. 358. Первый этап TIPSS. Введение проводника.
Этап баллонной дилатации. По проводнику, проведенному через ткань печени, в пункционный канал вводят баллонный катетер с диаметром баллона сначала 5 мм, а затем - 10 мм и выполняют поэтапную дилатацию ткани печени между печеночной и воротной венами (рис. 359). Созданный канал значительно снижает повышенное давление воротной вены (портальную гипертензию), за счет сброса крови из воротной вены с повышенным давлением в печеночную вену. Для того что бы этот канал в печени не "схлопывался" переходят к следующему этапу ТИПС.
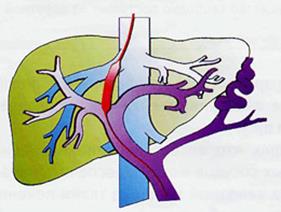
Рис. 359. Второй этап TIPSS. Баллонная дилатация ткани печени.
Этап установки металического стента. Затем во внутрипеченочный канал имплантируют саморасширяющийся или баллоннорасширяемый стент (металлический эндопротез напоминающий пружинку), который за счет упругих свойств металла не даст ткани печени "схлопнуться" (рис. 360). После имплантиции стента кровь системы воротной вены без препятственно попадает в печеночную вену, что устраняет портальную гипертензию и симптомы ею вызываемые. Выбор модели стента при наложении TIPSS (ТИПС) зависит лишь от личного предпочтения хирурга. При этом дистальный конец стента размещают в левой ветви воротной вены, а проксимальный конец - в печеночной вене вдоль ее просвета.
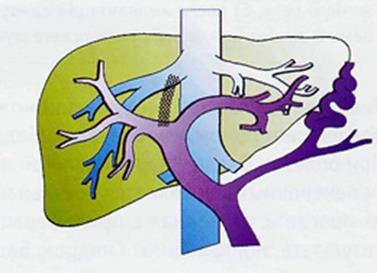
Рис. 360. Третий этап TIPSS. Установка стента.
Этап повторной дилатации стента (рис. 361). При необходимости выполняют повторную дилатацию имплантированного стента баллонным катетером с диаметром баллона 10-16 мм. Как правило, это необходимо для более плотной фиксации стента в созданном интрапеченочном канале, а также для создания большего отверстия между двумя венами. При контрольной портографии выявляется, что между левой ветвью воротной вены и правой печеночной веной имеется шунт достаточно большого диаметра, равного размеру имплантированного стента
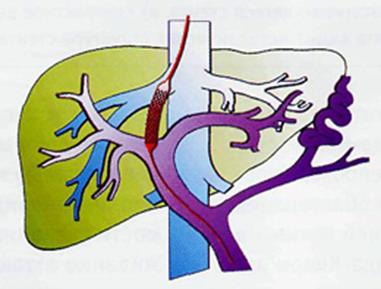
Рис. 361. Этап дилатации стента.
Этапы операции TIPSS на экране Rg-телевизора. Наложение внутрипеченочного порто-кавального шунта: а) этап пункции и катетеризации воротной вены через печеночную вену, б) после имплантации саморасширяющегося стента, в) контрастное вещество свободно поступает из воротной вены в печеночную вену, г) в просвете шунта видна металлическая структура стента (рси. 362).Показателем эффективности наложения TIPSS является градиент давления между воротной веной и печеночной веной, который должен быть не более 10-12 мм вод. ст.
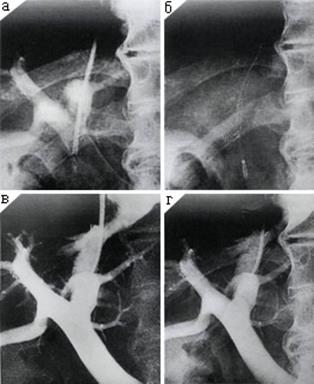
Рис. 362. Рентгенограммы этапов постановки стента
Клинически эффективность отценивается по прекращению или уменьшению проявлений портальной гипертензии - прекращение пищеводно-желудочного кровотечения, уменьшение количества асцитической жидкости, спадение варикозно расширенных вен передней брюшной стенки. В послеоперационном периоде больным проводится стандартный курс инфузионной, гемостатической и диуретической терапии.
Рентгеноэндоваскулярная эмболизация сосудов портальной системы. Эффективными методами снижения портального давления и остановки кровотечения является рентгеноэндоваскулярная эмболизация сосудов портальной системы и варикознорасширенных вен пищевода и кардиального отдела желудка
Профилактика рецидива кровотечения из варикозно-расширенных вен пищевода и кардии:
1. Устранение факторов, повышающих внутрибрюшное давление, которое способствует усилению притока крови к органам пищеварения и в портальную систему.
2. Больные, выжившие после первого эпизода кровотечения из ВРВП, нуждаются в профилактическом лечении неселективными
b-адреноблокаторами или в выполнении эндоскопической перевязки варикозных узлов
3. По возможности гемодинамический эффект применения β-адреноблокаторов необходимо мониторировать: если не удается достичь снижения градиента давления в печеночных венах на 20% от исходного или менее 12 мм рт. ст., рационально присоединение к β-адреноблокаторам изосорбида мононитрата
4. Больным, у которых первый эпизод кровотечения из ВРВП развился на фоне приема р'-адреноблокаторов, вторичная профилактика должна быть комплексной и включать наряду с {5-адреноблока-торами также эндоскопическое лигирование варикозных узлов.
Контрольные вопросы по изучаемой теме
· Определение термина – «портальная гипертензия».
· Портокавальные анастомозы, их локализация.
· Классификация портальной гипертензии.
· Этиология различных форм портальной гипертензии.
· Клиника, диагностика и дифференциальная диагностика.
· Лечение портальной гипертензии, показания к хирургическому лечению.
· Консервативная предоперационная терапия.
· Хирургическое лечение портальной гипертензии.
· Послеоперационные осложнения.
· Современные принципы этапного хирургического лечения портальной гипертензии, и ее осложнений.
· Исходы лечения синдрома портальной гипертензии.
· Этиологическая классификация цирроза печени.
· Классификация степени тяжести цирроза по Чайльду – Пью.
· Тактика ведения больного с циррозом печени.
· Портальная гипертензия и желудочно-кишечные кровотечения.
· Факторы риска первого эпизода кровотечения из варикозно расширенных вен пищевода.
· Профилактика кровотечений: фармакотерапия, эндоскопическая терапия, хирургическое лечение. Баллонная тампонада, как средство остановки кровотечения.
· Асцит – современные подходы к классификации и лечению.
· Печеночная энцефалопатия: определение и классификация; патогенез; клиническая картина; диагностика и дифференциальная диагностика; дополнительные методы диагностики; лечение.
ОСНОВНАЯ ЛИТЕРАТУРА
1. Глава 63. Портальная гипертензия. А.К. Ерамишанцев, А.Г Шерцингер, ЕА.Киценко, стр. 626/ Клиническая хирургия. Национальное руководство: в трех томах, Т. 2/ под ред. В. С. Савельева. - М.: ГЭОТАР - Медиа, 2009. - 832 с.
2. Хирургические болезни: Учеб. В 2 т. / Под ред. акад. РАН и РАМН В.С. Савельева и чл.-корр. РАМН А.И. Кириенко – М.: ГЭОТАР-Медицина, 2005. – Т. 2. – 400с
ДОПОЛНИТЕЛЬНАЯ ЛИТЕРАТУРА
1. Болезни печени и желчевыводящих путей: Руководство для врачей / Под ред. В.Т. Ивашкина. – М.: ООО «Издат. дом «М-Вести», 2002. – 416с.: ил. ISBN 5-901598-03-2
2. Шерлок Ш., Дули Дж. Заболевания печени и желчных путей: Практич. рук.: Пер. с англ. / Под ред. З.Г. Апросиной, Н.А. Мухина. – М.: Гэотар Медицина, 1999. – 864с.
Дата добавления: 2016-07-09; просмотров: 3210;
