Тепоємність рідин і твердих речовин.
Нині існують точні методи вимірювання теплоємності в широкому інтервалі температур. Досягнуто певних успіхів у розробці теорії теплоємності для простої твердої речовини і для газоподібного її стану при невисоких тисках. Що ж для задовільної теорії теплоємності складної твердої або рідкої речовини, то її досі не існує.
У тому разі, коли для конденсованих речовин відсутні експериментальні дані щодо теплоємності. То користуються двома наближеними емпіричними правилами.
1. Правило Дюлонга і Пті. Атомна теплоємність при постійному об’ємі для будь-якої твердої простої речовини наближено дорівнює 25,94 Дж/моль К.
Це правило більш чи менш поширюється на елементи, атомна маса яких вища ніж у калію. І при порівнянно високих температурах, близько до температур плавлення твердої речовини.
Якщо припустити незмінність теплоємності елементів при утворенні хімічної сполуки, то теплоємність такої сполуки, Дж/моль К:
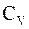 = 25n,
= 25n,
де n– кількість атомів, що входять у молекулу даної сполуки.
Для легких елементів значення атомних теплоємностей, відмінні від 25,94 Дж/моль К.
2. Правило адитивності. Молярна теплоємність складних твердих і рідких речовин дорівнює сумі молярних теплоємностей усіх елементів, тобто є величиною адитивною:
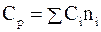 ,
,
де С-атомна теплоємність і-го елемента; n – кількість атомів і-го елемента в молекулі.
Для твердих і рідких речовин 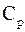 ≈
≈ 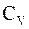 .
.
Дата добавления: 2016-06-02; просмотров: 1108;
