Залежність теплового ефекту хімічної реакції від температури
Розглянемо рівняння Кірхгофа, що описує залежність ентальпії реакції від температури:
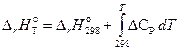 , (34)
, (34)
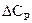 – різниця між сумою теплоємностей продуктів реакції й вихідних речовин помножених на стехіометричні коефіцієнти.
– різниця між сумою теплоємностей продуктів реакції й вихідних речовин помножених на стехіометричні коефіцієнти.
Для обчислення інтеграла необхідно знати залежність теплоємності від температури для всіх речовин, що не завжди можливо. Тому рівняння Кірхгофа застосовують у трьох наближеннях.
1. При найбільш грубому наближенні DСp = 0, тобто вважають рівними сумарні теплоємності продуктів і вихідних речовин. Тоді 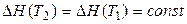 ,
,
т.ч. тепловий ефект уважається не залежним від температури. Цим наближенням користуються, якщо теплоємності деяких учасників реакції невідомі.
2. У другому наближенні вважають різницю теплоємностей постійною величиною DСР = const. Тоді
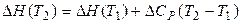 . (35)
. (35)
Це рівняння застосовують тільки для невеликого інтервалу температур Т2 – Т1, у якому відомі величини теплоємностей.
3. У найбільш точному наближенні використовують залежність всіх СРi від температури. Якщо теплоємності речовин дані у вигляді поліномів, наприклад (34), то рівняння Кірхгофа можна проінтегрувати, після чого воно буде мати такий вигляд:
 . (36)
. (36)
Другий закон термодинаміки. Ентропія. Обчислення зміни ентропії для різних процесів. Постулат Планка. Енергія Гіббса й енергія Гельмгольца. Рівняння Гіббса-Гельмгольца. Мимовільне протікання хімічних реакцій. Розрахунок зміни енергії Гіббса в хімічних реакціях. Хімічний потенціал. Активність і летючість.
Дата добавления: 2016-06-02; просмотров: 2436;
