Заміщення гідроксильної групи на галоген.
При взаємодії спиртів з HCl, HBr тощо, відбувається заміщення НО-групи на галоген:
С2Н5—ОН + НСІ  С2Н5—СІ + Н2О
С2Н5—СІ + Н2О
Легше всього вступають у реакцію третинні спирти за механізмом SN1:
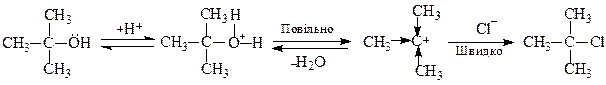
потім вторинні і нарешті первинні (механізм SN2):
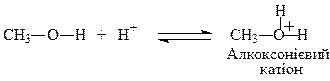
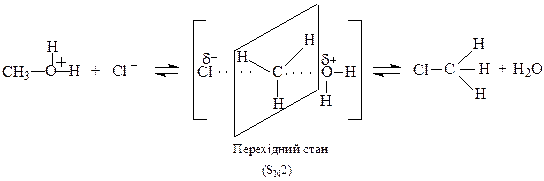
Взаємодія з галогенонуклеофілами PCl5, PCl3, SOCl2, також веде до утворення алкілгалогенідів з майже кількісним виходом:
С2Н5—ОН + РСІ5  С2Н5—СІ + РОСІ3 + НСІ
С2Н5—СІ + РОСІ3 + НСІ
Оксохлорид
фосфору
3. Реакція утворення естерів (естерифікація):
При взаємодії спиртів з органічними кислотами утворюються естери, які можна розглядати як похідні спиртів, у яких атом водню ОН-групи замінено на залишок кислоти –ацил:
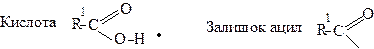 .
.
Тому таку реакцію ще називають реакцією ацилювання спиртів:
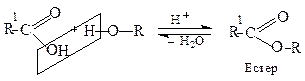
Естерифікація протікає у присутності каталізаторів – сильних мінеральних кислот (конц.H2SO4, H3PO4 тощо). Реакція естерифікації є зворотньою і називається гідролізом естеру.
Методом мічених атомів (ізотоп С13) встановлено, що в реакції естерифікації вода завжди утворюється за рахунок (НО) кислоти та (Н) спирту. Тому первинні спирти легко реагують з карбоновими кислотами, вторинні уже з меншою швидкістю, третинні спирти реагують важко.
4. Дегідратація спиртів (реакція Е)
Реакцією дегідратації зі спиртів отримують алкени та алкадієни. Дегідратація протікає при нагріванні спирту з концентрованою сульфатною або фосфатною кислотами (а також АІ2О3, кислих солей цих кислот та ін.).
Встановлено, що легше дегідратуються третинні спирти за механізмом Е1, потім вторинні і далі первинні – за механізмом Е2.
Дегідратація третинного спирту за механізмом Е1 протікає через стадію утворення карбокатіона і часто супроводжується реакцією SN1:
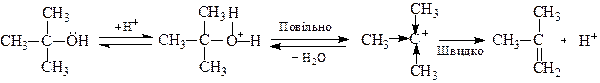 Алкоксонієвий Стабільний
Алкоксонієвий Стабільний
катіон карбокатіон
Дегідратація спиртів складної будови підпорядковується правилу Зайцева. Відщеплення водню (для утворення води) відбувається від сусіднього найменше гідрогенізованого атома вуглецю:
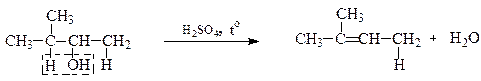
Реакції дегідратації бувають не тільки внутрішньомолекулярними але і міжмолекулярними. В результаті міжмолекулярної дегідратації утворюються етери:
Н+
С2Н5-ОН + НО-С2Н5  С2Н5-О-С2Н5
С2Н5-О-С2Н5
-Н2О Диетиловий етер
Перегрупування Вагнера-Мейєрвейна.
У реакціях, які протікають за механізмом Е1 з утворенням карбокатіонів, можлива міграція алкільних груп (ретропінаколінове перегрупування). Перегрупування такого типу характерні для тих випадків, коли замісники (НО, НаІ тощо) перебувають в α-положенні до четвертинного атома вуглецю:
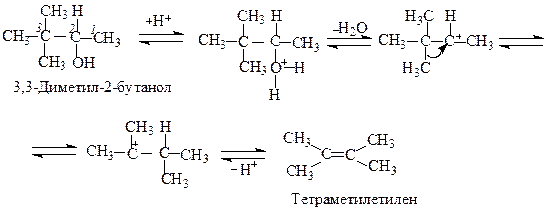
Окиснення спиртів.
При окисненні спиртів за допомогою KMnO4, K2Cr2O7, CrO3 або О2 у присутності Сu утворюються альдегіди, кетони або карбонові кислоти залежно від природи спиртів.
Первинні спирти утворюють альдегіди. Останні можуть в умовах реакції окиснюватися до карбонових кислот:
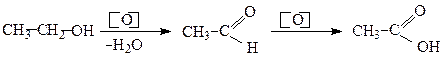
Оцтовий альдегід Оцтова кислота
Вторинні спирти утворюють кетони:
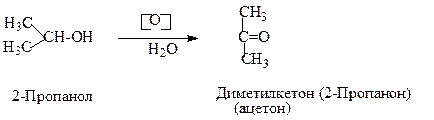
Третинні спирти окиснюються важко з розривом зв’язку С-С та з утворенням суміші кислот і кетонів:
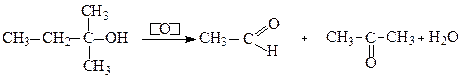
2-Метил-2-бутанол
Дата добавления: 2016-02-13; просмотров: 1209;
