Связь эквивалентной электрической проводимости со степенью диссоциации электролита и скоростями движения ионов.
Аррениус вывел формулу для электрической проводимости растворов, на которой основаны многие теоретические расчеты. Рассмотрим вывод этой формулы на примере бинарного электролита, состоящего из двух однозарядных ионов.
Предположим, что какой-то раствор содержит С кмоль/м3 растворенного вещества эквивалента. Степень электролитической диссоциации электролита равна а, скорости движения катиона и аниона, выраженные в м/с, соответственно равны ик и иа. Весь раствор помещен в сосуд цилиндрической формы с площадью сечения S м2 и находится между электродами, расположенными друг от друга на расстоянии l м (рис. 4.6).

|
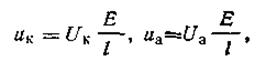
где Uки Uа — абсолютные скорости катиона и аниона, т. е. скорости движения ионов при градиенте напряжения 1 В на 1 м

| 4.37 |
Эквивалентная электрическая проводимость раствора при данном разбавлении пропорциональна степени электролитической диссоциации раствора электролита и сумме абсолютных скоростей катиона и аниона. Число Фарадея является в данном случае коэффициентом пропорциональности.
Уравнение (4.37) известно в литературе под названием уравнения Аррениуса. Из этого уравнения вытекает целый ряд очень важных следствий, которые играют большую роль в теории электрической проводимости растворов.
Дата добавления: 2016-02-20; просмотров: 1202;
