Реакции с С-Н-кислотами
Среди реакций терпеновых оксосоединений с С-Н-кислотами наиболее важными являются реакции конденсации цитраля с низкомолекулярными кетонами – пропаноном (ацетоном) и бутаноном (метилэтилкетоном). Эти реакции лежат в основе методов получения иононных препаратов – группы ценных душистых веществ с запахом фиалки.
Рассмотрим реакцию цитраля с ацетоном. Процесс протекает в щелочной среде при комнатной температуре. Как и в других реакциях альдегидов с кетонами, роль С-Н-кислоты играет ацетон, от α-звена которого под действием щелочи отщепляется протон:
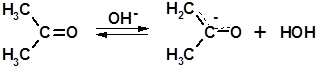
Образующийся карбанион является энергичным нуклеофилом и присоединяется по карбонильной группе цитраля:
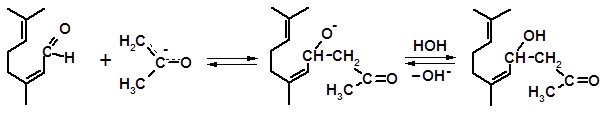
Реакция завершается дегидратацией кетола 1, приводящей к псевдоионону:
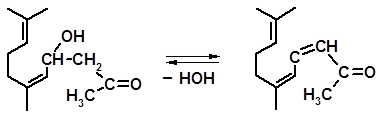
1 псевдоионон
Псевдоионон не обладает парфюмерными достоинствами и является лишь промежуточным продуктом в синтезе ионона. Превращение псевдоионона в ионон осуществляется циклизацией в присутствии кислот, как это было рассмотрено ранее (см. 3.1.3.1 ).
При конденсации цитраля с метилэтилкетоном возможны два направления реакции – за счет метильной и метиленовой групп молекулы кетона. Конденсация по метильной группе протекает в тех же условиях, что и реакция с ацетоном, и приводит к образованию псевдометилионона:
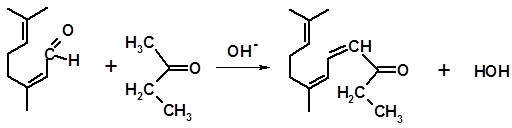
псевдометилионон
Чтобы направить конденсацию по метиленовой группе, реакцию проводят в менее щелочной среде, которую создают раствором сульфита натрия, и при повышенной температуре. В этих условиях основным продуктом конденсации оказывается изо-псевдометилионон:
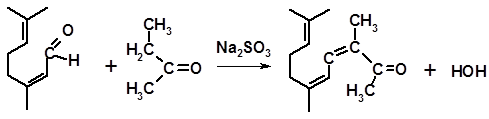
изо-псевдометилионон
Следует отметить, что добиться идеальной селективности конденсации по метильной или метиленовой группе не удается. Псевдометилионон всегда содержит примеси изопродукта и наоборот.
Циклизация псевдопродуктов позволяет получить смесь α-, β-, γ-изомеров метилионона или изометилионона. Наиболее высокую парфюмерную оценку имеет изо-α-метилионон, который отличается особенно тонким и приятным запахом фиалки.
Интересны превращения цитраля в щелочной среде. Под действием щелочей цитраль не только претерпевает самоконденсацию, как и другие альдегиды, но и способен к расщеплению с образованием ацетальдегида и метилгептенона:
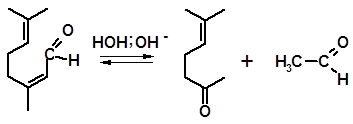
6-метил-5-гептен-2-он ацетальдегид
Протекание данной реакции становится понятным, если учесть, что структура цитраля соответствует продукту перекрестной конденсации метилгептенона и ацетальдегида, где С-Н-кислотой выступает ацетальдегид, а карбонильным соединением – метилгептенон. Хотя на практике такую конденсацию осуществить затруднительно из-за низкой селективности процесса (обычно кетон присоединяется по карбонильной группе альдегида), обратная реакция протекает легко (даже в присутствии К2СО3).
Дата добавления: 2015-09-29; просмотров: 1399;
