Реакции по ароматическому ядру. Реакции электрофильного замещения (SE)
Реакции электрофильного замещения (SE). Под влиянием нитро-группы (–I; –М) понижается реакционная способность бензольного ядра в реакциях электрофильного замещения. Так, нитробензол не алкилируется в условиях реакции Фриделя – Крафтса, но может вступать в реакции нитрования, галогенирования, сульфирования с образованием мета-замешенных нитроаренов:
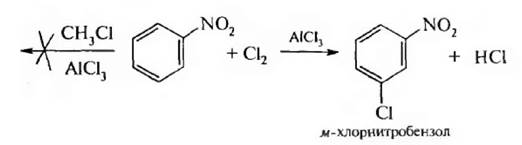
Реакции нуклеофильного замещения (SN). Пониженная электронная плотность в ароматическом ядре нитроаренов создает возможность для протекания реакции нуклеофильного замещения в аренах. В реакциях S нитрогруппа направляет заместитель в орто- и пара-положения:
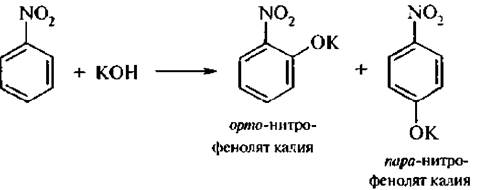
Соединения, содержащие две и более нитрогруппы, придают повышенную подвижность атомам водорода, находящимся в орто- и пара-положениях бензольного ядра. Так, сам нитробензол не окисляется, а динитробензол окисляется легко.
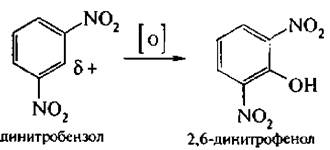
По этой же причине легко замешается атом хлора в молекуле о-нитрохлорбензола. Это позволяет получать различные нитропроизводные ароматического ряда:
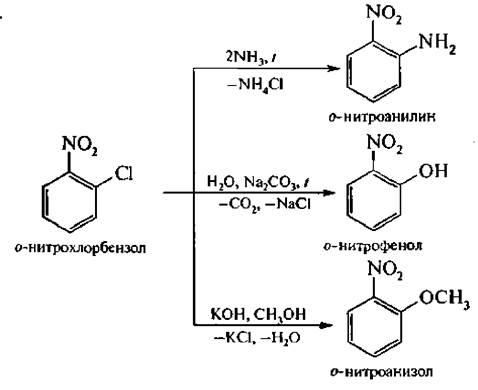
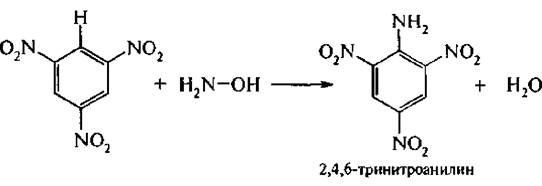
При действии на три нитробензол гидроксиламина атом водорода легко замещается на аминогруппу:
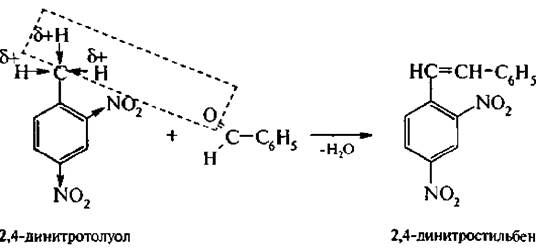
В молекуле динитрозамешенного толуола две нитрогруппы активируют атомы водорода метильной группы. Такие соединения могут вступать в реакции с ароматическими альдегидами:
Нитросоединения ароматического ряда и имеют большое значение. Это исходные вещества в производстве синтетических красителей, полимеров, моюших средств и ингибиторов коррозии. Ряд нитросоединений находят применение в качестве биологически активных веществ.
16. АМИНЫ
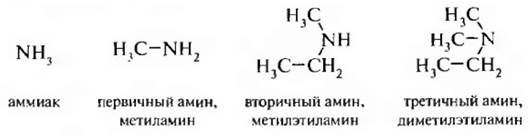
Амины – производные аммиака, в молекуле которого один, два или три атома водорода замещены углеводородными радикалами. По числу замещенных атомов водорода они делятся на первичные, вторичные и третичные амины.
Существуют и четвертичные аммониевые соли, например хлорид тетраметнламмония [(CH3)4N+]Cl-, соответствующее ему основание – гидроксидтетраметиламмония [(CH3)4N+]OH-, который представляет собой сильное основание, аналогичное гидроксидам щелочных металлов, так как связь с гидроксильной группой здесь ионная.
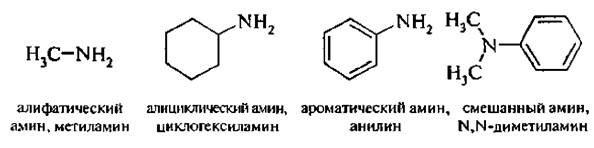
В зависимости от природы углеводородных радикалов амины подразделяются на алифатические, ал и циклические, ароматические и смешанные (имеющие алифатический и ароматический радикалы):
Для аминов характерна метамерия:
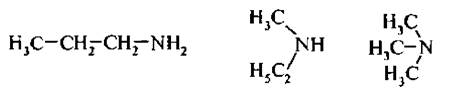
Эти соединения имеют общую формулу С, H^N, но отличаются друг от друга строением углеводородных радикалов.
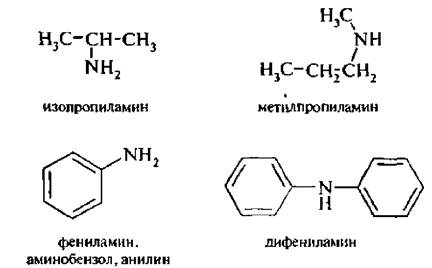
Названия простых построению аминов образуют от названий соответствующих углеводородных радикалов, связанных с атомом азота, добавляя в конце корень -амин. Кроме того, многие ароматические амины имеют тривиальные названия.
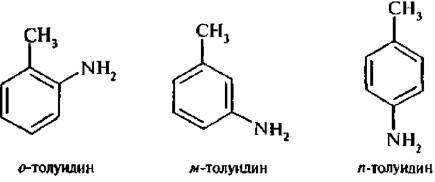
Производные толуола, содержащие аминогруппу в бензольном ядре, называются толуидинами;
АМИНЫ АЛИФАТИЧЕСКОГО РЯДА (АЛКИЛАМИНЫ)
Дата добавления: 2015-09-29; просмотров: 4825;
