Химические свойства
Для ариламинов характерны реакции с участием атома азота и реакции с участием атомов углерода ароматического ядра.
Основность. Ароматические амины обладают основным характером. Однако они слабее, чем амины жирного ряда и даже слабее аммиака.
Снижение основности обусловлено сопряжением неполеленной пары электронов атома азота с π-электронной системой ароматического ядра:
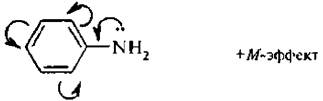
Основные свойства падают в ряду:
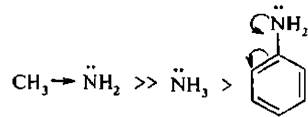
Являясь слабыми основаниями, ариламины образуют соли только с сильными минеральными кислотами:
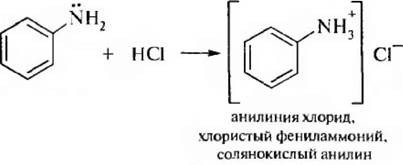
Анилин не образует соли с Н2СО3
На основность ариламинов существенное влияние оказывают заместители в бензольном кольце. Электронодонорные заместители увеличивают основность, а электроноакиепторные – уменьшают ее.
При переходе от первичных к третичным основность ароматических аминов снижается.
1. Реакция алкилирования. Первичные и вторичные ариламины реагируют с галоген алканам и, образуя N-алкил- и N,N-диалкилариламины. Реакция протекает труднее в виду снижения нуклеофильных свойств атома азота.
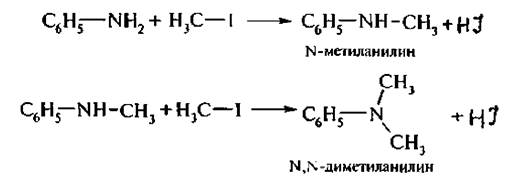
2. Реакция ацилирования. Первичные и вторичные амины при взаимодействии с хлоран гидридам и или ангидридами карбоновых кислот образуют N-замещенные амиды карбоновых кислот. N-Ацильные производные анилина и его гомологов называют анилидами.
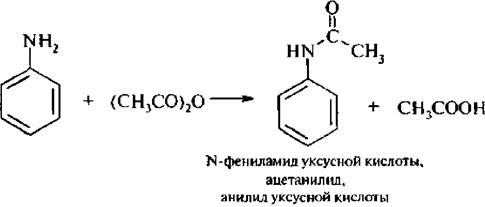
Амиды карбоновых кислот легко гидролизуются в кислой или щелочной среде с образованием исходного амина и карбоновой кислоты:
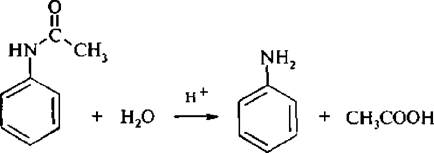
Способность ацильных производных легко подвергаться гидролизу позволяет применять эту реакцию в органическом синтезе для временной защиты аминогруппы от окисления и протекания по ней нежелательных реакций,
Ацильные производные аминов имеют большое значение как фармацевтические препараты. Например, ацетанилид – это жаропонижающий препарат, который долгое время применялся в медицинской практике, а в настоящее время – в ветеринарии.
3. Реакция образования изоцианидов (качественная реакция). Аналогично алифатическим аминам первичные ароматические амины при нагревании с хлороформом и щелочью в спиртовой среде образуют изоцианиды – вещества с неприятным тошнотворным запахом:
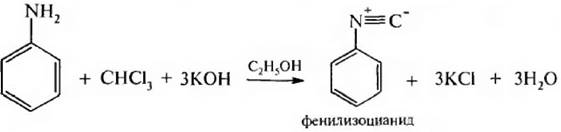
4. Реакция взаимодействия с азотистой кислотой. Алифатические и ароматические амины по-разному реагируют с азотистой кислотой» эту реакцию можно использовать для отличия первичных, вторичных и третичных аминов алифатического и ароматического рядов.
Первичные ароматические амины при действии азотистой кислоты в присутствии сильной минеральной киапоты образуют соли диа-зония. Эта реакция получила название реакции диазотирования.
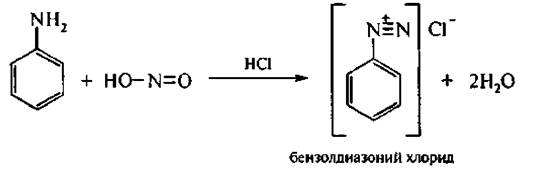
Вторичные ариламины и N-алкилариламины в этих условиях превышаются BN-нитрозоамины:
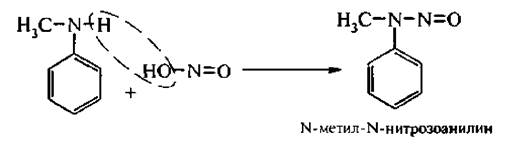
Третичные ароматические амины при взаимодействии с азотистой кислотой нитрозируются по бензольному кольцу обычно в пара-положение, если пара-положение занято, то нитрозогруппа занимает орто-подожение:
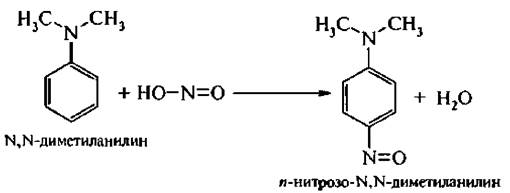
5. Реакция взаимодействия с ароматическими альдегидами. Первичные ароматические амины реагируют при нагревании с ароматическими альдегидами, образуя азометины (основания Шиффа):
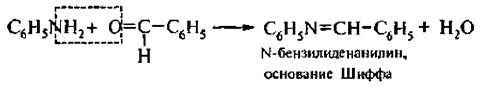
Реакции с участием атомов углерода ароматического ядра
Для ариламинов характерны реакции электрофильного замещения по ароматическому ядру
Аминогруппа проявляет +M-эффект и выступает в качестве сильного электронодонора по отношению к бензольному кольцу, тем самым активируя его в реакциях электрофильного замещения.
6. Реакция галогенирования.
Анилин взаимодействует с бромной водой в отсутствие катализатора, образуя сразу 2,4,6-триброманилин:
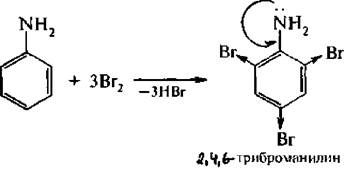
Для введения хлора в ароматическое ядро требуются особые условия (присутствие НCl, ССl4, С2Н5ОН, 16 °С).
7. Реакция нитрования. Поскольку аминогруппа чувствительна к действию окислителей, а ее влияние на ароматическое ядро обуславливает сравнительно легкую окисляемость аренаминов до хинонимина, нитрование ароматических аминов проводят предварительно их проацилировав. Это необходимо для защиты аминогруппы, а также для понижения реакционной способности ароматического ядра.
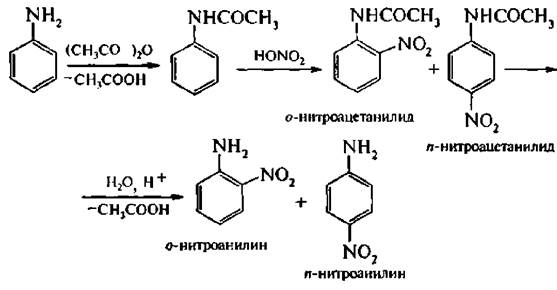
Образовавшееся ацильное производное подвергают гидролизу и выделяют свободные нитроанилины.
8. Реакции сульфирования. При взаимодействии анилина с концентрированной серной кислотой образуется пара-аминобензолсульфокислота, которую чаще называют сульфаниловой кислотой. Реакция протекает через стадию образования N-фенилсульфаминоьой кислоты, которая перегруппировывается впара-шинобензолсул ьфокислоту:
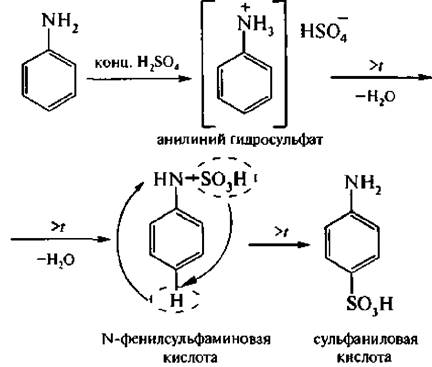
В сульфанилоной кислоте имеются две функциональные группы: -NH2 (основная) и -SO3H (кислотная). Это приводит к тому, что сульфаниловая кислота существует в виде биполярного иона (внутримолекулярной соли), называемого иногда цвиттер-ионом. Именно этим объясняется его высокая температура плавления.
Сульфаниловая кислота довольно сильная, с основаниями она легко образует соли:
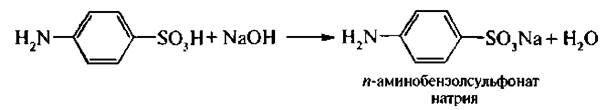
Из-за биполярной структуры сульфаниловая кислота не способна образовывать сод и с минеральными кислотами, т. е. несмотря на наличие аминогруппы, она не обладает основными свойствами.
Сульфаниловая кислота широко применяется в производстве красителей и лекарственных средств. Наибольший интерес представляет амид сульфаниловой кислоты (сульфаниламид, стрептоцид), структура которого лежит в основе сульфаниламидных препаратов, которые составили целую эпоху в лечении инфекционных заболеваний.
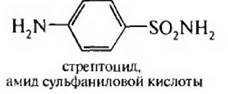
В качестве исходного вещества для получения стрептоцида используют анилин. Синтез осуществляют в четыре стадии:
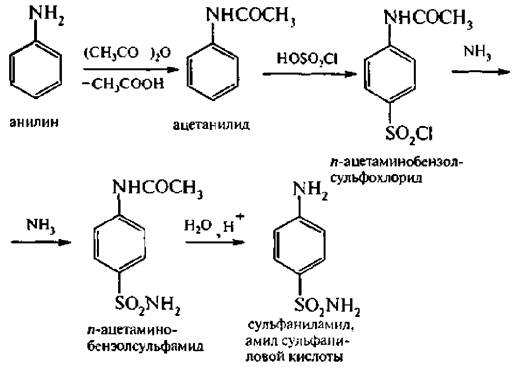
В молекуле стрептоцида содержится аминогруппа и сульфамидная группа. За счет NH2-группы стрептоцид растворяется в кислотах, а за счет SO2NН2 – растворяется в щелочах, т. е. обладает амфотерными свойствами:
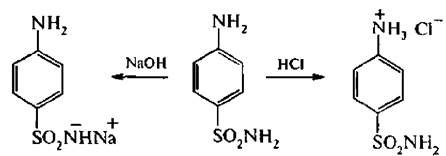
Стрептоцид был получен немецким студентом Гельмо. Но потребовалось 30 лет, чтобы его внедрить в медицинскую практику.
Стрептоцид и другие сульфаниламидные препараты действуют на стрептококковые микроорганизмы, отсюда и произошло название «стрептоцид». Однако сульфаниламиды действуют не бактерицидно, а бактериостатически, т. е. задерживают рост микроорганизмов.
В основе бактериостатического действия сульфаниламилов лежит их сходство с п-аминобензойной кислотой (ПАБК), которая участвует в биосинтезе фолиевой кислоты, необходимой для жизнедеятельности микроорганизмов.
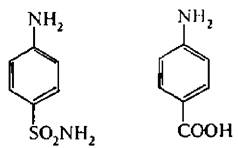
Подобие этих соединений как в структурном, так и в химическом отношении приводит к тому, что сульфаниламиды способны вступать в конкурентное замещение п-аминобензойной кислоты, препятствуя синтезу фолиевой кислоты, что и подавляет рост и размножение микроорганизмов.
Производные стрептоцида:
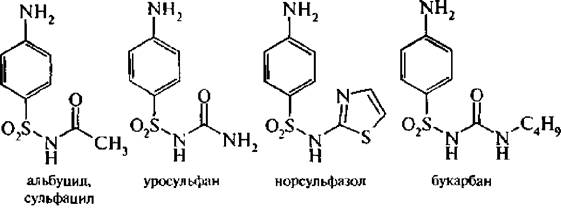
Конечно, нам не предоставляется возможным рассмотреть все сульфаниламидные препараты. Более длительно вы будете знакомиться с ними в курсе фармацевтической химии, только помните одно: что есть сульфамидные препараты и есть сульфаниламидные. Сульфамиды – это общее понятие, а сульфаниламидные обязательно содержат 4-NH2-C6H4-SO2-NHR.
Амины – промежуточные продукты в производстве красителей, пестицидов, полимеров, ингибиторов коррозии, ПАВ, адсорбентов, лекарственных препаратов.
Алифатические амины поражают нервную систему, вызывают нарушения проницаемости стенок кровеносных сосудов и клеточных мембран, функций печени и развитие дистрофии.
Ароматические амины вызывают образование метгемоглобина, угнетающего центральную нервную систему. Некоторые ароматические амины – канцерогены.
ДИАЗО- И АЗОСОЕДИНЕНИЯ
ДИАЗОСОЕДИНЕНИЯ
Диазосоединениями называют органические вещества, содержащие в своей структуре группировку из двух атомов азота, связанную с углеводородным радикалом и остатком минеральной кислоты.
По природе углеводородного радикала различают алифатические и ароматические диазосоелинения.
Ароматические диазосоединения имеют общую формулу ArN2X, где Аr – ароматический радикал, X – кислотный остаток.
Если X – остаток сильной минеральной кислоты (О-, Br-, HSO4-, NO3-), диазосоединения имеют ионное строение и называются соли диазония (Ar–N≡NX), а если X – остаток слабой минеральной кислоты (CN-, HSO3-, ОН-, SH-), то они имеют ковалентное строение – Ar–N≡N–X. Диазосоединения общей формулы Ar–N≡N–O–M, где М – металл, называют диазотаты.
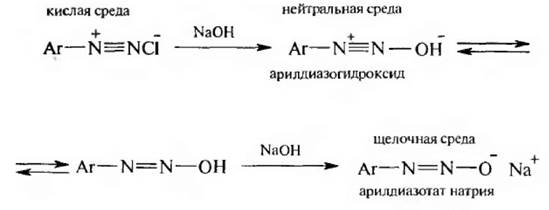
В зависимости от рН среды эти формы способны взаимопревращаться.
В кислой среде диазосоединения существуют в виде солей диазония, в щелочной – в виде диазотатов, близкой к нейтральной – в виде изомерных диазогидратов:
Дата добавления: 2015-09-29; просмотров: 8230;
