II. Реакции присоединения
Реакции присоединения не характерны для аренов, они протекают в жестких условиях.
1. Гидрирование. При повышенных температуре и давлении» в присутствии катализаторов (мелкопористый никель– никель Ренея) бензол и его гомологи присоединяют три молекулы водорода:
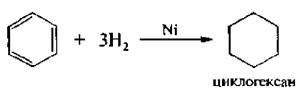
Остановить реакцию на стадии образования продуктов частичного гидрирования невозможно, поскольку они гидрируются значительно легче, чем сам бензол.
2. Хлорирование. При интенсивном солнечном освещении или под действием ультрафиолетового излучения бензол присоединяет хлор, Реакция протекает по радикальному механизму с образованием гексахлорциклогексана:
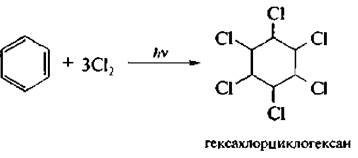
III. Реакции окисления
1. Окисление бензольного цикла. Бензольное кольцо устойчиво к действию окислителей. В обычных условиях ни перманганат калия, ни азотная кислота, ни оксид хрома (VI), ни другие сильные окислители не окисляют бензол. В жестких же условиях, например, при действии кислорода воздуха в присутствии оксида ванадия (V2O5), при температуре 400-500 °С бензольное ядро окисляется, образуя малеиновый ангидрид:
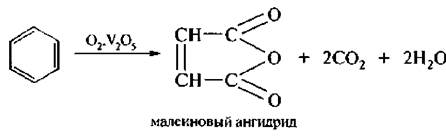
2. Окисление гомологов бензола. Алкилбензолы, в отличие от незамещенного бензола, окисляются значительно легче. В этом случае при действии сильных окислителей (КМnO4, К2Сr2O7 и др.) подвергаются окислению боковые цепи:
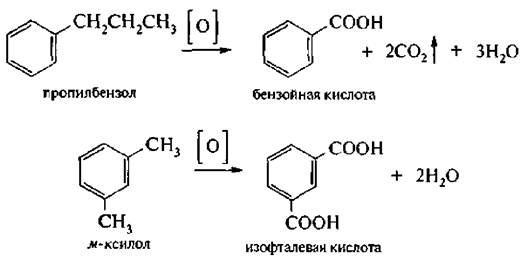
Продуктами реакции являются ароматические карбоновые кислоты. Каждый алкильный радикал в бензольном кольце, независимо от длины углеродной цепи, окисляется до карбоксильной группы.
3. Озонирование. Подобно алкенам, бензол и его гомологи реагируют с озоном, образуя продукты присоединения, – триозониды:
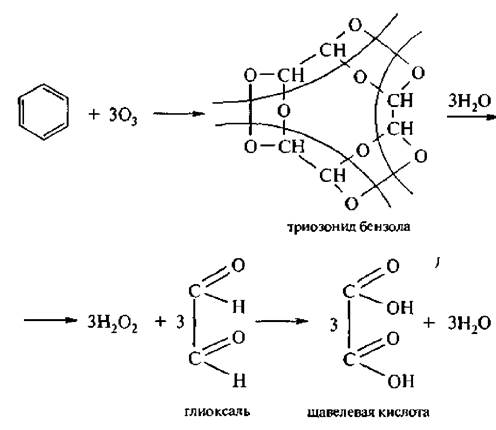
Триозониды взрывоопасны. Это маслянистые жидкости, они нестойкие и под действием влаги разрушаются с образованием дикарбонильных соединений и продуктов их дальнейшего окисления – дикарбоновых кислот
Правила ориентации в бензольном ядре
В молекуле незамещенного бензола электронная плотность распределена равномерно, поэтому электрофильный реагент может атаковать в равной степени любой из шести атомов углерода.
Если же в бензольном кольце содержится какой-либо заместитель, то под его влиянием происходит перераспределение π-электрон ной плотности и новый заместитель вступает в определенные положения по отношению к имеющемуся.
По влиянию на направление реакций электрофильного замещения и реакционную способность бензольного кольца заместители можно разделить на две группы – заместители I рода (орто-, пара-ориентанты) и заместители II рода (мета-ориентанты).
Заместители I рода – атомы и атомные группы, проявляющие положительный индуктивный (+I) или положительный мезомерный (+М) эффекты (доноры электронов):
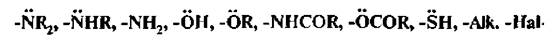
Заместители 1 рода (за исключением галогенов) увеличивают электронную плотность в бензольном кольце, тем самым активируют его в реакциях SE и направляют следующие заместители в орто- и пара-положения.
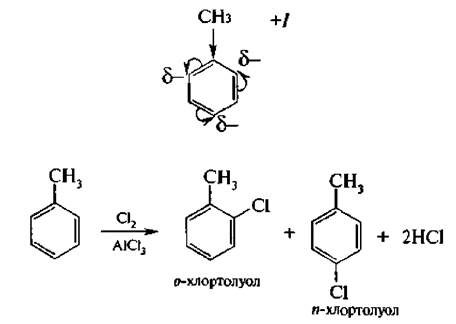
Заместители II рода – группы, проявляющие отрицательный индуктивный (-I) или отрицательный мезомерный (-М) эффекты (электроноакцепторы):
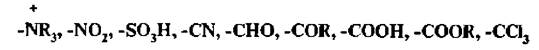
Заместители II рода уменьшают электронную плотность в бензольном ядре и снижают скорость реакций SE по сравнению с незамещенным бензолом. Вновь входящий заместитель направляется преимущественно в мета-положение.
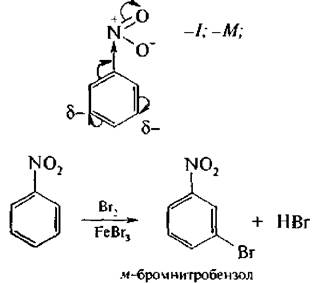
При введении третьего заместителя необходимо учитывать природу двух уже имеющихся в бензольном ядре.
Ориентация в дизамещенных производных бензола
В зависимости от электронной природы заместителей и их взаимного расположения различают согласованную и несогласованную ориентацию.
При согласованной ориентации оба заместителя направляют новый заместитель в одни и те же положения бензольного кольца. Согласованная ориентация характерна для дизамещенных производных бензола, в которых соблюдаются условия:
1) ориентанты одного и того же рода находятся в мета-положении относительно друг друга:
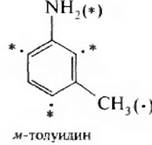
2) заместители находятся в орто- или пара-положении по отношению друг к другу; но один из них является ориентантом I рода, а другой – II рода:
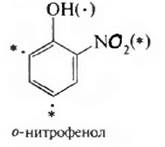
При несогласованной (несовпадающей) ориентации один из заместителей направляет новую группу в одни, а другой – в иные положения бензольного кольца. Предпочтительное направление замещения можно определить, используя следующие правила:
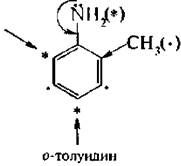
I) если один из заместителей является орнентантом I рода, он определяет направление замешения:
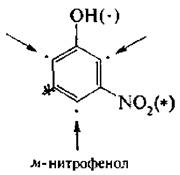
2) если оба заместителя являются ориентантамн 1 рода, направление замещения определяется более сильным ориентантом:
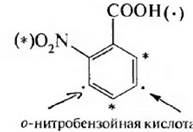
3) если оба заместителя являются ориентантамн II рода, замещение осуществляется с трудом, а место вхождения третьего заместителя определяется более сильным ориентантом:
Наряду с электронной природой заместителей на соотношение продуктов замещения оказывают влияние пространственные факторы.
Дата добавления: 2015-09-29; просмотров: 4790;
