Строение алкадиенов
Строение алкадиенов с кумулированным и двойными связями рассмотрим на примере аллена. В его молекуле центральный атом углерода находится в sp-гибридизации, а атомы углерода метиленовых групп – в sp2-гибридизации. Все три атома углерода расположены в пространстве линейно, а гг-связи находятся в двух взаимно перпендикулярных плоскостях.
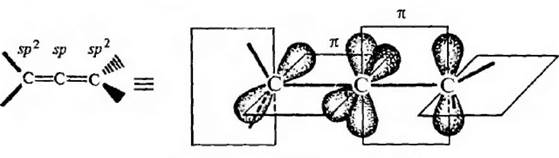
Рис. 9.1. Строение молекулы аллена
В молекулах алкадиенов с сопряженными двойными связями происходит дополнительное перекрывание p-электронных облаков соседних π-связей (π,π-сопряжение) и образуется единая π-электронная система. Ниже (рис. 9.2) показано образование единого π-электронного облака в молекуле бутадиена-1,3.
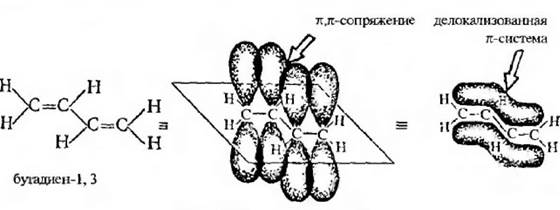
Рис. 9.2. Строение молекулы аллена
В результате π,π-сопряжения происходит укорачивание σ-связей.
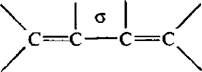
Так, в молекуле бутадиена-1,3 длина связи С2–С3 составляет 0.148 нм, тогда как длина связи С–С в этане – 0,154 нм. Энергия сопряжения бутадиена-1,3 составляет примерно 15 кДж/моль.
Алкадиены с изолированными двойными связями построены аналогично алкенам.
Особенности строения алкадиенов различных типов сказываются на их реакционной способности. Диены с кумулированными и изолированными связями напоминают по химическим свойствам алкены, вступая в реакции присоединения с участием двух двойных связей самостоятельно.
Для сопряженных диенов характерны некоторые особенности в химических свойствах.
Дата добавления: 2015-09-29; просмотров: 3473;
