Тепловой эффект реакции (ЛНР) не зависит от пути её протекания, а определяется только природой и физическим состоянием исходных веществ и конечных продуктов.
Этот закон был экспериментально установлен и имеет в настоящее время два практически важных следствия.
Согласно одному из них: Тепловой эффект реакции равен сумме теплот образования продуктов реакции 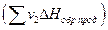 за вычетом суммы теплот образования исходных веществ
за вычетом суммы теплот образования исходных веществ 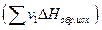 с учетом числа молей (v) всех участвующих в реакции веществ:
с учетом числа молей (v) всех участвующих в реакции веществ:
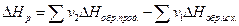 (1.10)
(1.10)
В общем случае тепловой эффект 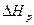 реакции типа:
реакции типа:
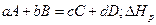
рассчитывается по уравнению
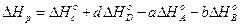
Согласно другому следствию, термохимические уравнения можно складывать, вычитать и умножать на численные множители.
В соответствии с законом сохранения энергии, система может самопроизвольно совершать "работу только за счёт собственной энергии, т.е. запас её внутренней энергии должен при этом уменьшаться или 𝛥U<0. В случае самопроизвольно протекающих химических реакций, это стремление к уменьшению запаса внутренней энергии может быть связано с выделением теплоты в виде экзотермического эффекта. Влияние этого фактора на направление самопроизвольного протекания различных процессов является одной из движущих сил химической реакции, а сам фактор называется энергетическим или энтальпийным. Но, наряду с ним, действует и другой фактор, иначе бы все химические реакции были экзотермическими. Этот фактор получил название структурного или энтропийного. Для понимания его природы необходимо рассмотреть ещё одну термодинамическую функцию состояния системы, получившую название «энтропия».
Мерой неупорядоченности или хаотичности системы в термодинамике служит энтропия (S). Обозначим энтропию исходного состояния данной системы как S1, энтропию конечного состояния как S2, а её изменение в процессе как 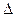 S = S2 - S1.Поскольку из опыта следует, что S2 > S1, то
S = S2 - S1.Поскольку из опыта следует, что S2 > S1, то 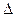 S >0. Стремление же различных термодинамических систем к увеличению энтропии называется структурным или энтропийным фактором и его преобладающим действием объясняется самопроизвольное протекание эндотермических процессов.
S >0. Стремление же различных термодинамических систем к увеличению энтропии называется структурным или энтропийным фактором и его преобладающим действием объясняется самопроизвольное протекание эндотермических процессов.
Энтропия зависит от всех видов движения частиц, составляющих систему, их количества, числа степеней свободы, агрегатного состояния и возрастает с повышением температуры. Поэтому в процессах, вызываемых увеличением движения частиц, т.е. при нагревании, испарении, плавлении, разрыве связей между атомами и т.п., энтропия возрастает. Наоборот, упрочнение связей, охлаждение, конденсация, кристаллизация, полимеризация, т.е. процессы, связанные с упорядочением системы, сопровождаются уменьшением энтропии.
Энтропия пропорциональна также массе вещества. Её обычно относят к одному моль вещества и выражают в Дж/моль*К.
Энтропия является функцией состояния системы.
Энтропия, отнесенная к стандартной температуре 25°С (298К) и стандартному давлению (1 атм), называется стандартной (S°298).
Одной из характерных особенностей энтропии в отличие от других термодинамических функций состояния является то, что можно определить её абсолютное значение. В термодинамических справочниках приводятся абсолютные значения стандартной энтропии веществ при 298 К на основании которых можно рассчитать стандартные энтропии тех или иных реакций.
Изменение энтропии системы в результате протекания химической реакции ( 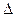 S) или энтропия реакции, как любой функции состояния системы, также не зависит от пути процесса, а определяется лишь энтропией начального и конечного состояний:
S) или энтропия реакции, как любой функции состояния системы, также не зависит от пути процесса, а определяется лишь энтропией начального и конечного состояний:
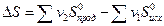 (1.26)
(1.26)
При суммировании следует учитывать число молей (V) всех участвующих веществ. В общем случае изменение энтропии 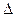 Sp в результате протекания химической реакции типа:
Sp в результате протекания химической реакции типа:
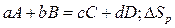
рассчитывается по уравнению
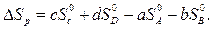 (1.27)
(1.27)
Дата добавления: 2015-09-29; просмотров: 923;
