Макрохарактеристики и статистический интеграл
Термодинамические макрохарактеристики газа – свободную энергию, внутреннюю энергию, давление и энтропию выразим через статистический интеграл. Докажем, что ранее введенная величина F является свободной энергией.
Свободная энергия 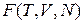 выражается через статистический интеграл согласно (2.79)
выражается через статистический интеграл согласно (2.79)
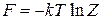 ,
,
где
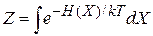 .
.
Подставляем (2.80)
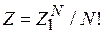
и получаем
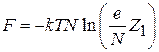 , (2.91)
, (2.91)
где при 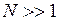 использована формула Стирлинга
использована формула Стирлинга
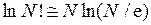 .
.
Подстановка (2.90) в (2.91) выражает термодинамическую величину через энергетический спектр частицы
 , (2.92)
, (2.92)
где 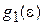 – энергетическая плотность состояний частицы.
– энергетическая плотность состояний частицы.
Внутренняя энергия 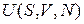 является средним по фазовому ансамблю значением полной энергии системы
является средним по фазовому ансамблю значением полной энергии системы
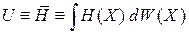 .
.
Используем (2.77)
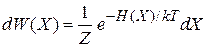
и (2.78)
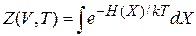 ,
,
находим
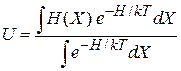 .
.
Интеграл в числителе выражаем через интеграл в знаменателе путем дифференцирования по параметру 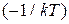
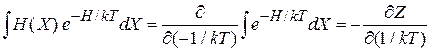 .
.
Учитываем
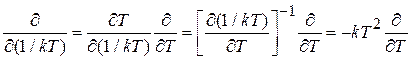 ,
,
и получаем выражение внутренней энергии газа через статистический интеграл газа
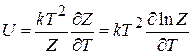 . (2.93)
. (2.93)
Среднюю энергию частицы 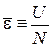 выразим через статистический интеграл частицы
выразим через статистический интеграл частицы 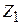 . Используем (2.80)
. Используем (2.80)
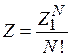 ,
, 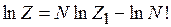 ,
,
тогда
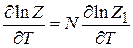
и из (2.93) находим
 . (2.94)
. (2.94)
В (2.94) подставляем (2.90)
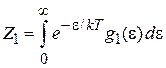 ,
,
получаем
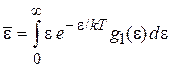 , (2.94а)
, (2.94а)
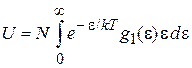 . (2.95)
. (2.95)
Средняя энергия частицы и внутренняя энергия газа выражены через энергетический спектр частицы 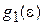 .
.
Уравнение Гиббса–Гельмгольца связывает внутреннюю энергию U со свободной энергией F. Используем связь обеих энергий со статистическим интегралом. Выражаем статистический интеграл из (2.79)
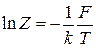
и подставляем в (2.93)
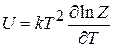 ,
,
находим
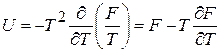 . (2.96)
. (2.96)
Получено известное в термодинамике уравнение Гиббса–Гельмгольца в дифференциальной форме, следовательно, ранее введенная величина F является свободной энергией.
В первом равенстве (2.96) перегруппировываем сомножители
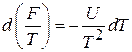 .
.
Интегрируем в пределах 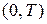 , учитываем
, учитываем 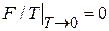 , и выражаем свободную энергию через внутреннюю энергию
, и выражаем свободную энергию через внутреннюю энергию
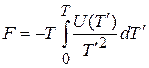 (2.97)
(2.97)
– уравнение Гиббса–Гельмгольца в интегральной форме.
Давление и статистический интеграл. В (2.44)
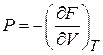
подставляем (2.79)
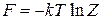
и выражаем давление через статистический интеграл
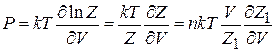 , (2.98)
, (2.98)
где 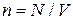 – концентрация частиц. В последнем равенстве использовано
– концентрация частиц. В последнем равенстве использовано
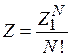 ,
, 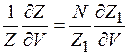 ,
,
При отсутствии потенциального поля энергия частицы не зависит от координат 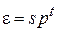 . Из (2.26) и (2.90)
. Из (2.26) и (2.90)
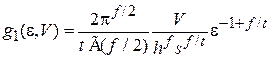 ,
, 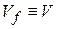 ,
,
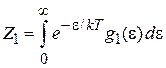
получаем
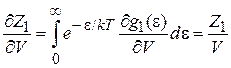 ,
,
где учтено
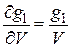 .
.
В результате (2.98)
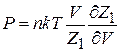
дает уравнение идеального газа
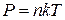 . (2.99)
. (2.99)
Энтропия и статистический интеграл. В (2.45)
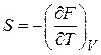
подставляем (2.79)
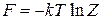
и выражаем энтропию через статистический интеграл
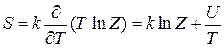 , (2.100)
, (2.100)
где учтено (2.93)
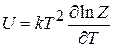 .
.
Для системы и ее независимых подсистем 1 и 2 выполняется
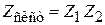 ,
,
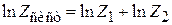 ,
,
тогда из (2.79)
 ,
,
из (2.93)
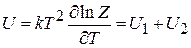
и из (2.100)
 .
.
Следовательно, для статистически независимых подсистем и видов движений свободная энергия, внутренняя энергия и энтропия являются аддитивными величинами.
Статистический смысл энтропии в рамках канонического распределения. Используем внутреннюю энергию
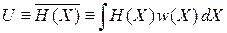
и функцию распределения (2.75)
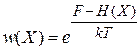
с условием нормировки
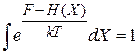 .
.
Результаты подставляем в (2.39)
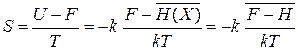 ,
,
находим
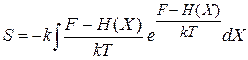 .
.
Получаем формулу Больцмана(1872 г.)
 . (2.101)
. (2.101)
Энтропия пропорциональна среднему по фазовому ансамблю от логарифма плотности вероятности реализации микросостояний.

Людвиг Больцман (1844–1906)
При приближении системы к состоянию равновесия уменьшается ее упорядоченность, увеличивается число микросостояний
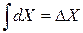 ,
,
реализующих ее макросостояние. Согласно условию нормировки вероятности
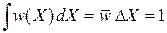
среднее значение функции распределения обратно объему фазового ансамбля
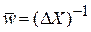 .
.
При приближении к состоянию равновесия  растет,
растет, 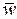 уменьшается, тогда согласно (2.101)
уменьшается, тогда согласно (2.101)
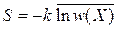
энтропия увеличивается. В равновесном состоянии число микросостояний и энтропия достигают максимума. Энтропия является мерой хаотичности состояния системы.
С учетом
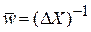
из
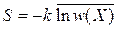
находим
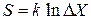 . (2.102)
. (2.102)
Энтропия пропорциональна логарифму числа микросостояний системы. Этот же результат (2.71) был получен в рамках микроканонического распределения.
Дата добавления: 2015-09-21; просмотров: 974;
