Этиология и патогенез. Этиология ССД сложна и недостаточно изучена
Этиология ССД сложна и недостаточно изучена. Предполагается мультифакториальный генез ССД, обусловленный взаимодействием неблагоприятных экзо- и эндогенных факторов с генетической предрасположенностью к заболеванию.
Наряду с ранее обсуждавшейся ролью инфекции (вирусной и др.), охлаждения, вибрации, травм, стресса и эндокринных сдвигов в последнее время особое внимание обращено на триггерное действие химических агентов (промышленных, бытовых, алиментарных) и отдельных лекарственных средств, наиболее демонстративное в случаях индуцированной склеродермии.
Благодаря современным исследованиям расшифрованы и некоторые генетические механизмы предрасположенности к ССД, что ранее аргументировалось наличием семейных случаев ССД и близких заболеваний, увеличением иммунных и других сдвигов у здоровых родственников пробандов. Подтверждено наличие хромосомной нестабильности у больных ССД. Выявлено сочетание определенных антигенов и аллелей системы гистосовместимости (HLA) с ССД: HLA-A9, В8, В35, DR1, DR3, DR5, DR11, DR52 и С4А, варьирующее в разных популяциях, что, по современным данным, может быть связано с хромосомным дефектом теломер.
Среди различных групп вирусов обращено внимание на цитомегаловирусную инфекцию как возможный триггер васкулопатии при ССД и других аутоиммунных болезнях. Новая теория микрохимеризма о роли фетальных прародительских клеток в генезе ССД рассматривает развитие аутоиммунных болезней с позиций трансплантационной биопсии.
С точки зрения патогенеза, ССД представляет типичное аутоиммунное заболевание, при котором выявляются уатоантитела к собственным элементам соединительной ткани, в частности, к фибробластам. При этом повреждение фибробластов происходит таким образом, что они начинают продуцировать избыточное количество коллагена, который и приводит к склерозу органов.
Основу патогенеза ССД составляют нарушения иммунитета, фиброзообразования и микроциркуляции, взаимодействующие на уровне основных клеточных (иммунокомпетентные клетки – фибробласты – эндотелий – клетки крови) и рецепторно-лигандных систем (молекулы адгезии, факторы роста, интерлейкины и др.).
У больных ССД выявляется широкий спектр разнообразных нарушений клеточного и гуморального иммунитета, включая признаки Т-клеточной активации и дисрегуляции в системе Тh1- и Th2-клеток, повышение экспрессии отдельных иммунорегуляторных и фиброгенных цитокинов; обнаружение специфических антинуклеарных и антинуклеолярных аутоантител – антицентромерных (АЦА), антитопоизомеразных (АТА) или анти-РНК-антител, а также антинейтрофильных цитоплазматических (АНЦА), антиэндотелиальных, антител к различным компонентам соединительной ткани и др.
Изменения метаболизма соединительной ткани с повышением коллагено- и фиброзообразования определяют по существу нозологическую специфику заболевания. Выявлены фенотипически устойчивая гиперактивность фибробластов, структурные и функциональные аномалии клеточных мембран и рецепции, что позволяет предполагать также системную мембранную патологию. Обсуждается возможность первичного, или индуцированного, метаболического дефекта фибробластов, реализующегося при воздействии дополнительных экзогенных стимулов. Таким дефектом может быть недавно идентифицированный у Tsk-1 мышей (экспериментальная модель ССД) мутантный ген фибриллина, что нашло косвенное подтверждение при обследовании полуизолята индейского племени в Оклахоме, у которого распространенность ССД в 50 раз выше, чем в популяции.
Привлекают внимание и современные исследования нарушений апоптоза при ССД как возможного фактора селекции фенотипа фибробластов с повышенным биосинтезом коллагена и других компонентов соединительной ткани. Как известно, ССД является уникальной природной моделью генерализованного фиброза, изучение механизмов которого имеет общее клиническое значение.
Важным звеном патогенеза и морфогенеза ССД является нарушение микроциркуляции с активацией и пролиферацией эндотелия и гладкомышечных клеток, редупликацией базальных мембран, утолщением стенки и сужением просвета микрососудов, вазоспазмом, агрегацией форменных элементов, стазом, деформацией и редукцией капиллярной сети (облитерирующая микроангиопатия). Повреждение эндотелия в свою очередь ведет к дальнейшей активации иммунной системы и фибробластов, что наряду с каскадными нарушениями микроциркуляции лежит в основе развития порочного круга патологических реакций и прогрессирования болезни. Полипотентные функции эндотелия и гладкомышечных клеток сосудов требуют дальнейшего изучения как и проблема сложных межклеточных коопераций, осуществляющихся с участием молекул адгезии (селектины, ELAM-1, VCAV-1 и ТСАМ-1), факторов роста – трансформирующего, тромбоцитарных и фибробластных (TGFp, PDGF, pFGF); фактора некроза опухоли (TNF), эндотелина-1 и других вазоактивных пептидов, интерферонов и интерлейкинов -1, -2, -4, -6, -8 и -17, часть из которых обладает фиброгенным эффектом.
Схематически патогенез ССД можно представить следующим образом:
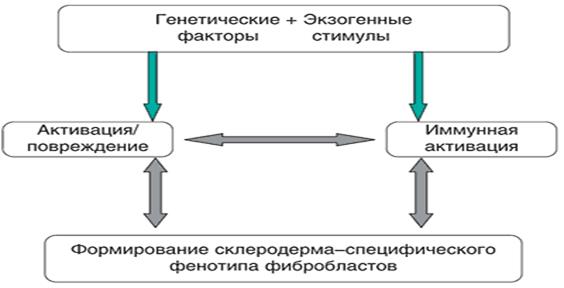
Большую научную и практическую значимость представляют установленные ассоциации между специфическими для ССД аутоантителами, генетическими маркерами и определенными клиническими характеристиками ССД. Так, АЦА сочетаются с маркерами HLA-DR1, DR4, лимитированным поражением кожи, легочной гипертензией и хроническим течением, а АТА – с DR3, DR5, DQ7, диффузным поражением кожи, фиброзом легких и быстропрогрессирующим течением ССД. Антитела к РНП часто встречаются при подостром течении и перекрестных формах ССД. Выявленные клиникоиммунологические ассоциации позволяют предполагать, что носительство определенных антигенов HLA предрасполагает к продукции свойственных ССД аутоантител и формированию клинических синдромов и субтипов заболевания.
Дата добавления: 2015-08-14; просмотров: 1030;
