Эффект Джоуля-Томсона для газа Ван-дер-Ваальса
Эффект Джоуля-Томсона наблюдается, поскольку реальный газ отличается от идеального, а именно, внутренняя энергия моля реального газа есть сумма кинетической энергии его молекул WK с потенциальной энергией их взаимодействия Wп: U = WK + Wп. Эта последняя зависит от среднего межмолекулярного расстояния, а значит, от объема моля газа Vμ. Значит внутренняя энергия реального газа зависит не только от температуры (как у идеального), но и от объема.
Предположим, что перепады давления в течении Джоуля-Томсона ∆р = р2 — p1 и температуры ∆T = Т2 – T1= малы. Считая газ довольно разреженным, а величины а и b в (5) малыми поправками, можно получить из условия постоянства энтальпии (выкладки опускаем):
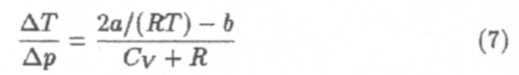
Пусть газ расширяется (∆р < 0). Знак эффекта Джоуля-Томсона зависит от того, какая из поправок, а или b уравнения Ван-дер-Ваальса (5) доминирует. Если 2a/(RT) > b (доминирует а), то ∆Т/∆р > 0 и газ охлаждается (положительный эффект). Например, газ всегда охлаждается, если b = 0, а ≠ 0: при расширении энергия теплового движения молекул расходуется на работу против сил межмолекулярного притяжения.
В противном случае (2а/RТ < b — доминирует b) газ нагревается (отрицательный эффект). Этот результат особенно легко объяснить в предельном случае а = 0, 6 ≠ 0. В самом деле, условие а = 0 приводит к отсутствию сил притяжения между молекулами (ведь поправка а как раз и появляется из-за этих сил). Силы же отталкивания остаются и при расширении газа совершают работу, увеличивающую кинетическую энергию молекул, а значит, и температуру.
При Т = 2а/Rb изменение температуры равно нулю и эта температура называется температурой инверсии эффекта Джоуля-Томсона. Для большинства газов температура инверсии лежит значительно выше комнатной и они в опыте Джоуля-Томсона охлаждаются. Для водорода и гелия температура инверсии значительно ниже комнатной и для них наблюдается отрицательный эффект (нагревание при расширении). Для плотных газов полученные результаты верны лишь качественно. На самом деле, знак эффекта зависит еще и от давления.
При очень высоких давлениях главную роль играют собственные размеры молекул газа (поправка 6) и все газы показывают отрицательный эффект. Таким образом, температура инверсии не постоянна, а зависит от давления. На рис. 9 качественно изображена эта зависимость — кривая инверсии. Она разбивает плоскость (р, Т) на две области с противоположными знаками эффекта Джоуля-Томсона.
Лекция №16
Дата добавления: 2015-08-11; просмотров: 4120;
