Поверхностное натяжение. Как уже указывалось ранее, молекулы жидкости (и газа) притягиваются друг к другу (только на очень малых расстояниях начинают преобладать силы отталкивания)
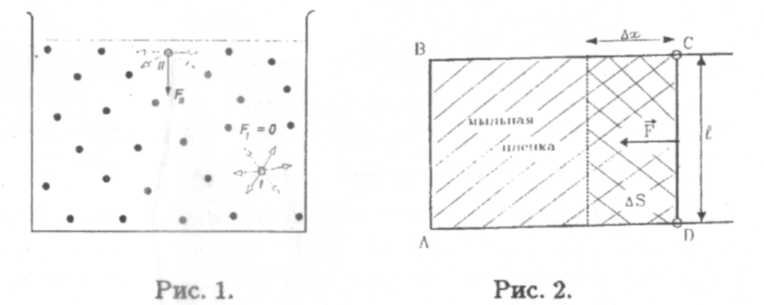
Как уже указывалось ранее, молекулы жидкости (и газа) притягиваются друг к другу (только на очень малых расстояниях начинают преобладать силы отталкивания). Молекула, находящаяся в глубине объема жидкости, равномерно окружена другими молекулами со всех сторон (молекула I на рис. 1) и сумма всех действующих на нее сил притяжения F1 равна нулю. Молекулы тонкого поверхностного слоя (II на рис. 1) имеют соседей лишь с внутренней стороны. Поэтому на них действует некоторая ненулевая сила FII, направленная внутрь объема жидкости. Таким образом, молекулы поверхностного слоя, стремясь уйти внутрь объема, создают в жидкости дополнительное давление, называемое молекулярным или внутренним давлением.
Жидкость стремится, насколько возможно, сократить свою поверхность (например, в невесомости жидкость принимает форму шара как тела с наименьшей плошадыо поверхности при заданном объеме). Поверхностный слой ведет себя как тонкая растянутая упругая пленка, поэтому говорят о явлении поверхностного натяжения. Такая "пленка", будучи натянута на некий контур, действует на каждую точку этого контура с силой, касательной поверхности жидкости и направленной внутрь контура.
Сумма сил притяжения F, действующих на контур, ограничивающий честь поверхности жидкости, называется силой поверхностного натяжения. Она пропорциональна длине контура l:

где а — коэффициент поверхностного натяжения. Из (1) следует а = F/l, то есть
коэффициент поверхностного натяжения равен отношению силы поверхностного натяжения, действующей на контур, к длине этого контура
Измеряется коэффициент ав Н/м и может быть равен 0.01 / 0.54 Н/м. С ростом температуры ауменьшается из-за увеличения средних расстояний между молекулами. При комнатной температуре для этилового спирта аравно 0.025, для воды — 0.073, для ртути — 0.54 Н/м.
Чтобы найти работу силы поверхностного натяжения, поставим следующий эксперимент (см. рис. 2). Пусть мыльная пленка натянута на прямоугольную проволочную рамку ABCD, причем сторона CD длины l может свободно скользить по сторонам ВС и AD как по направляющим. При сдвиге CD по направлению к АВ на расстояние ∆х сила поверхностного натяжения F совершит работу:
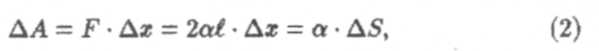
|
где ∆S = 2l * ∆х — уменьшение площади поверхности пленки; оно вдвое больше уменьшения площади самой пленки l * ∆х, так
совершена за счет уменьшения потенциальной энергии поверхности жидкости.
Та часть потенциальной энергии поверхности жидкости, которая может перейти в работу при изотермическом сокращении поверхности, называется свободной энергией поверхности жидкости.
Изменение свободной энергии ∆W должно быть равно совершенной работе ∆А. А так как, согласно (2), ∆W = ∆А = а * ∆S,
то:
Свободная энергия поверхности жидкости равна произведению коэффициента поверхностного натяжения на площадь этой поверхности:

Из (3) находим: а = W/S, что дает другое определение коэффициента поверхностного натяжения:
коэффициент поверхностного натяжения равен отношению свободной энергии поверхности жидкости к площади ее поверхности,
а значит аможно измерять в Дж/м2, что, впрочем, равно Н/м.
Поверхностное натяжение играет большую роль в природе. Некоторые насекомые и личинки используют поверхностную пленку водоема для передвижения. Мокрые песчинки слипаются в комок, так как площадь обволакивающей комок водяной пленки меньше суммы площадей водяных оболочек отдельных песчинок. А пена на воде и мыльные пузыри всем хорошо известны. На величину коэффициента поверхностного натяжения сильно влияет наличие в жидкости примесей, так как молекулы примеси взаимодействуют друг с другом и с молекулами жидкости иначе, чем сами жидкостные молекулы. Вещество, уменьшающее а растворителя, называется поверхностно-активным. Для воды таковыми являются, например, нефть, спирт, мыло и другие.
Молекулы жидкости притягиваются друг к другу сильнее, чем к молекулам поверхностно-активного вещества и поэтому покидают поверхность раствора, на которую вытесняются молекулы примеси. Так, поверхность раствора мыла в воде состоит в основном из молекул мыла.
Дата добавления: 2015-08-11; просмотров: 1647;
