Энтропия по Больцману
 Подход Больцмана к понятию энтропии помог прояснить ее физический смысл. Энтропия при этом выступает как мера беспорядка. Чембольше беспорядка в системе, тем выше ее энтропия. Более строго энтропия вводится с помощью соотношения
Подход Больцмана к понятию энтропии помог прояснить ее физический смысл. Энтропия при этом выступает как мера беспорядка. Чембольше беспорядка в системе, тем выше ее энтропия. Более строго энтропия вводится с помощью соотношения
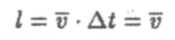 где к— постоянная Больцмана, W — термодинамическая вероятность состояния, т.е. величина, показывающая сколькими способами может быть реализовано данное состояние. Следует отметить, что равномерное распределение молекул по объему является одновременно наиболее вероятным и наиболее беспорядочным их состоянием, обладающим наибольшей энтропией. Например, если имеется сосуд, разделенный на две части, в одной из которых находится кислород, а в другой водород, то после устранения перегородки газы равномерно перемешаются и величина энтропии системы возрастет. Обратный процесс практически невозможен, так как его вероятность чрезвычайно мала.
где к— постоянная Больцмана, W — термодинамическая вероятность состояния, т.е. величина, показывающая сколькими способами может быть реализовано данное состояние. Следует отметить, что равномерное распределение молекул по объему является одновременно наиболее вероятным и наиболее беспорядочным их состоянием, обладающим наибольшей энтропией. Например, если имеется сосуд, разделенный на две части, в одной из которых находится кислород, а в другой водород, то после устранения перегородки газы равномерно перемешаются и величина энтропии системы возрастет. Обратный процесс практически невозможен, так как его вероятность чрезвычайно мала.
Понятия энтропии по Больцману и по Клаузиусу физически эквивалентны между собой. В качестве третьего начала термодинамики иногда рассматривают теорему Нернста, согласно которой при нуле градусов Кельвина энтропия системы равна нулю (S = 0 при T = 0).
В заключение перечислим некоторые важные свойства энтропии:
1. Энтропия системы, состоящей из нескольких тел, равна сумме энтропии этих тел.
2. Если в изолированной системе происходят обратимые процессы, то ее энтропия остается неизменной.
3. Если в изолированной системе происходят необратимые процессы, то ее энтропия возрастает. Возможны лишь такие процессы, которые ведут к увеличению энтропии изолированной системы.
Лекция № 14
Дата добавления: 2015-08-11; просмотров: 2427;
