Агрегатные состояния
Каждое вещество может находиться в одном из трех агрегатных состояний: твердом, жидком или газообразном. Различные агрегатные состояния называются также фазами вещества. Агрегатное состояние, в котором находится вещество, определяется соотношением кинетической и потенциальной энергий его молекул.
Рассмотрим силу взаимодействия F двух молекул как функцию расстояния R между ними (см. рис. 1). Видно, что притяжение, преобладающее на больших расстояниях (F < 0), при
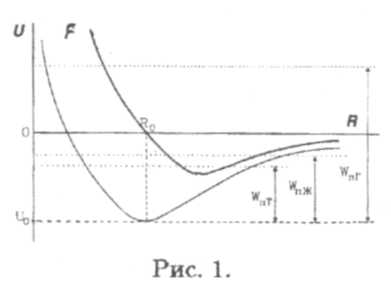
сближении молекул сменяется отталкиванием (F > 0). Значение R = Ro, при котором сила взаимодействия равна нулю, называется равновесным расстоянием: таково было бы среднее расстояние между молекулами, если бы они не двигались.
На том же рисунке изображена зависимость потенциальной энергии взаимодействия молекул U(R).
Эта кривая имеет минимум в точке R = Ro. Глубина его Uo = U(Ro) называется энергией связи.
Средняя кинетическая энергия молекул газа W значительно больше энергии связи Uo. Говоря другими словами, молекулы газа очень слабо взаимодействуют друг с другом. Поэтому поведение газов хорошо описывается в рамках молекулярно-кинетической теории, где таким взаимодействием вовсе пренебрегают. Молекулы газа летают почти свободно, и газ занимает весь предоставленный ему объем.
В жидкости молекулы взаимодействуют гораздо сильнее, и расстояния между ними значительно меньше, чем в газе (кинетическая энергия W сравнима с потенциальной). Молекулы жидкости находятся, в основном, вблизи своих положений равновесия и лишь изредка переходят в другие места. Поэтому плотность жидкости значительно больше, а сжимаемость очень мала. Жидкость сохраняет свой объем, но не форму.
Наконец, в твердом теле частицы связаны так сильно, что оно сохраняет не только свой объем, но и форму (если, конечно, напряжения в образце не превышают предел упругости данного материала). Частицы совершают малые колебания вблизи своих положений равновесия, крайне редко покидая их. Положения равновесия частиц твердого тела образуют упорядоченную структуру, носящую название кристаллической, а сами твердые тела называются кристаллами (см. далее).
Впрочем, существуют тела (например, стекло), на первый взгляд твердые, то есть, сохраняющие форму. Однако более подробный анализ показывает, что они лишены кристаллической структуры. В частности, у них совершенно отличная от кристаллов диаграмма плавления. Такие вещества называются аморфными. По существу это переохлажденная жидкость, настолько густая, что она полностью потеряла текучесть. С течением времени аморфные тела кристаллизуются — в них появляются кристаллические фрагменты. В этом, например, причина помутнения стекол в окнах старых домов.
Дата добавления: 2015-08-11; просмотров: 2516;
