Энтропия по Клаузиусу
Клаузиус в 1865 году ввел в рассмотрение новую термодинамическую функцию 5, названную им энтропией. Изменение этой функции определяется с помощью соотношения

где dQ — количество теплоты, переданное телу при температуре T.
Изменение энтропии зависит от того, какие процессы происходят с телом — обратимые или необратимые. Термодинамический процесс называется обратимым, если при совершении его сначала в прямом, а затем в обратном направлении как сама система, так и все внешние тела, возвращаются в первоначальное состояние. Если это не выполнено, то процесс называется необратимым. Не вдаваясь в детали доказательства, отметим, что для обратимости процесса необходимо и достаточно, чтобы на любой его стадии система находилась в состоянии термодинамического равновесия.
Можно показать, что для обратимого цикла 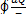 = 0, а для необратимого
= 0, а для необратимого 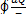 < 0.
< 0.
 При переходе системы из начального состояния (1) в конечное состояние (2) изменение энтропии может быть найдено по формуле:
При переходе системы из начального состояния (1) в конечное состояние (2) изменение энтропии может быть найдено по формуле:
 Второе начало термодинамики (ФЗ). Энтропия замкнутой системы материальных тел есть неубывающая функция времени
Второе начало термодинамики (ФЗ). Энтропия замкнутой системы материальных тел есть неубывающая функция времени
Дата добавления: 2015-08-11; просмотров: 2522;
