Расчет изменения энергии Гиббса для химических реакций.
Первый способ расчета аналогичен методу оценки изменения энтальпии реакции по табулированным энтальпиям образования различных веществ. В сходные таблицы сведены и величины G и точно так же принято, что для простых веществ G = 0.
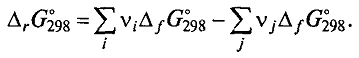
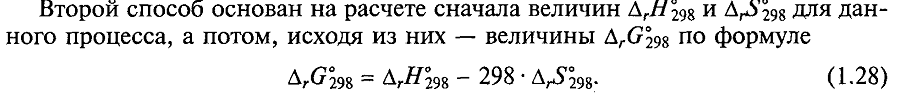
Для марганца наиболее характерны соединения со степенями окисления
+2, +4, +7. Вместе с тем легко доступны и производные марганца в степенях
окисления 0, +3, +6. Для технеция типичные степени окисления +4, +6, +7;
для рения +6, +7. Химия технеция и рения характеризуется легкостью взаимных превращений соединений с разными степенями окисления. В высшей степени окисления марганец значительно более сильный окислитель по сравнению с технецием(VII) и рением(VII). В этом отношении он даже превосходит соседний элемент хром(VI). Благодаря возможности спаривания d-электронов под действием лигандов сильного поля создаются условия для акцептирования электронных пар лигандов на освободившиеся орбитали центрального атома с образованием отрицательных степеней окисления -3, -2, -1 в карбонильных и нитрозильных производных.
Дата добавления: 2015-08-11; просмотров: 1307;
